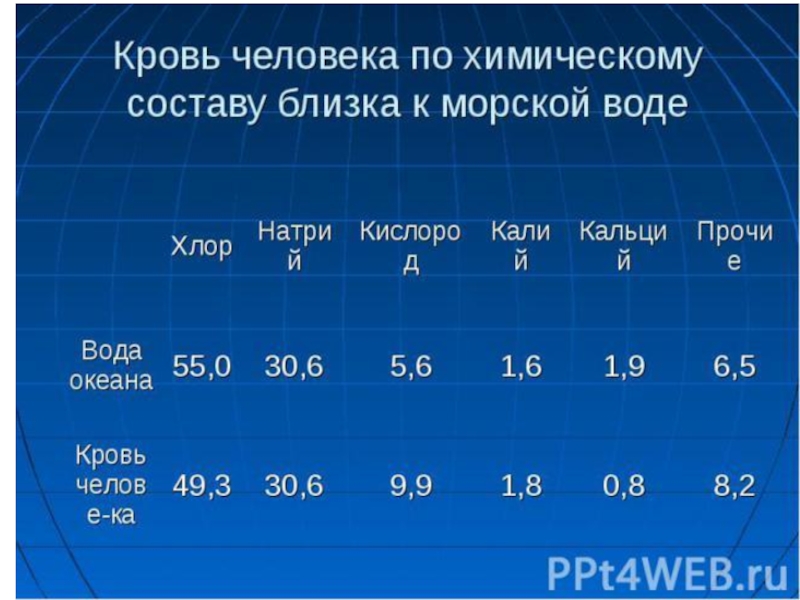
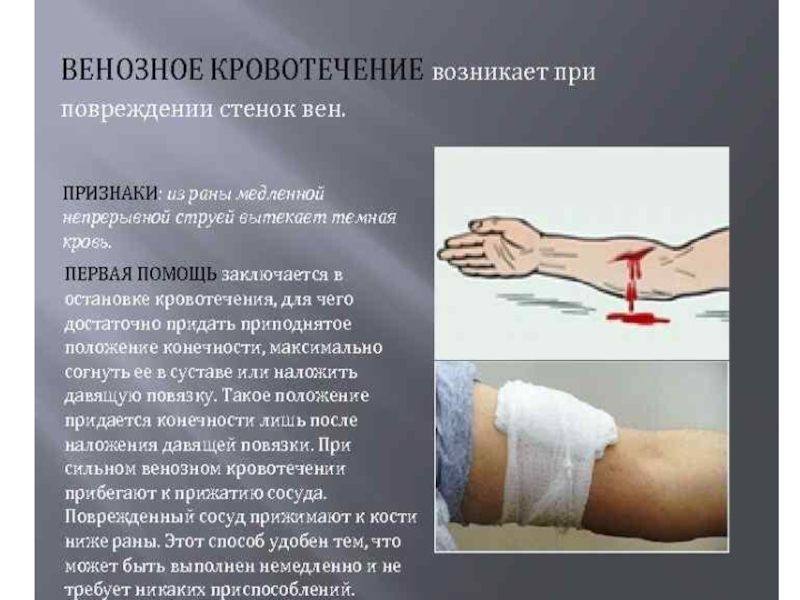
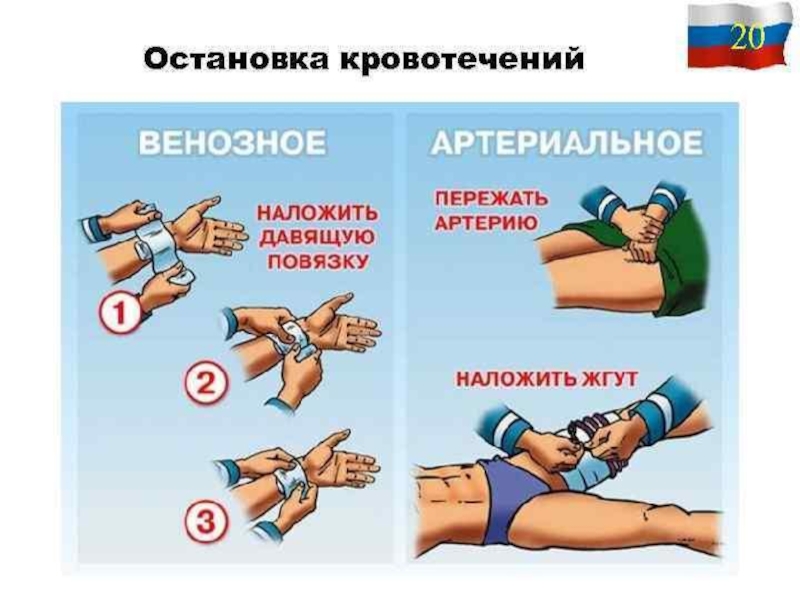
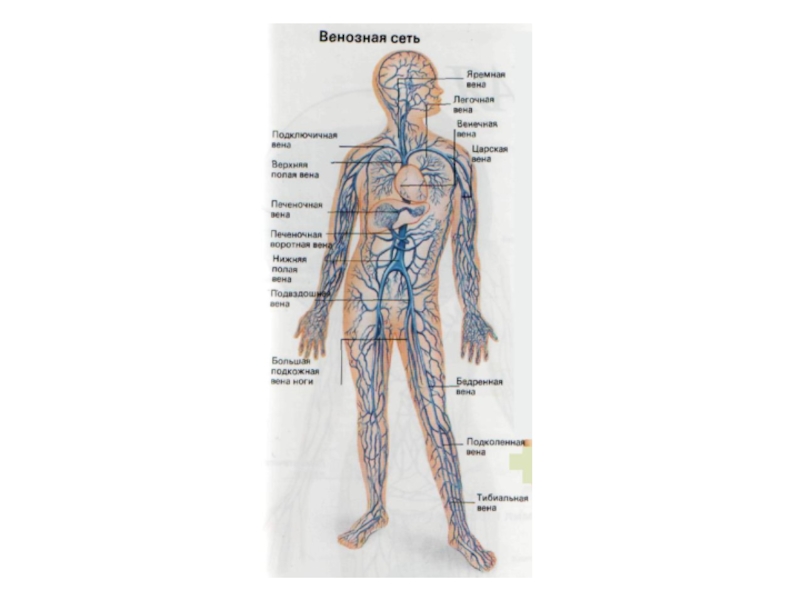
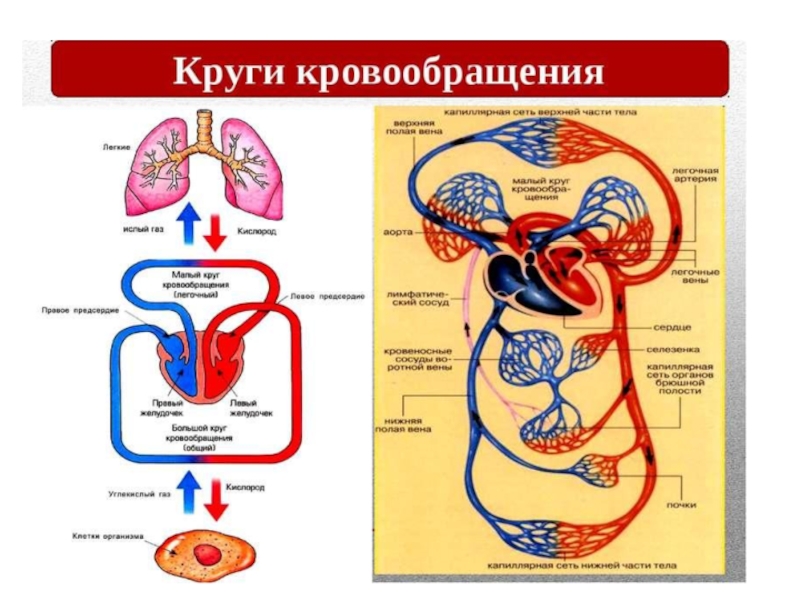
что жизнь зародилась в море. Он утверждал, что животные, живущие сегодня, унаследовали от своих прародителей неорганический состав крови. Ученые, так же, вывели формулу морской воды времен палеозоя. Знаете, что удивительно? По составу эта древняя вода полностью идентична минеральному составу нашей крови. Что же получается. В нас текут воды древнего моря? Так может поэтому нас так и тянет к морю.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
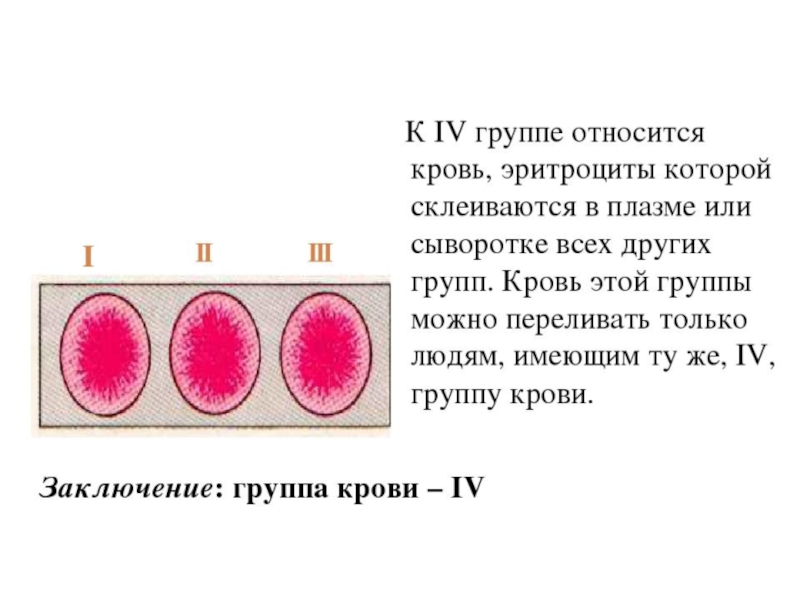
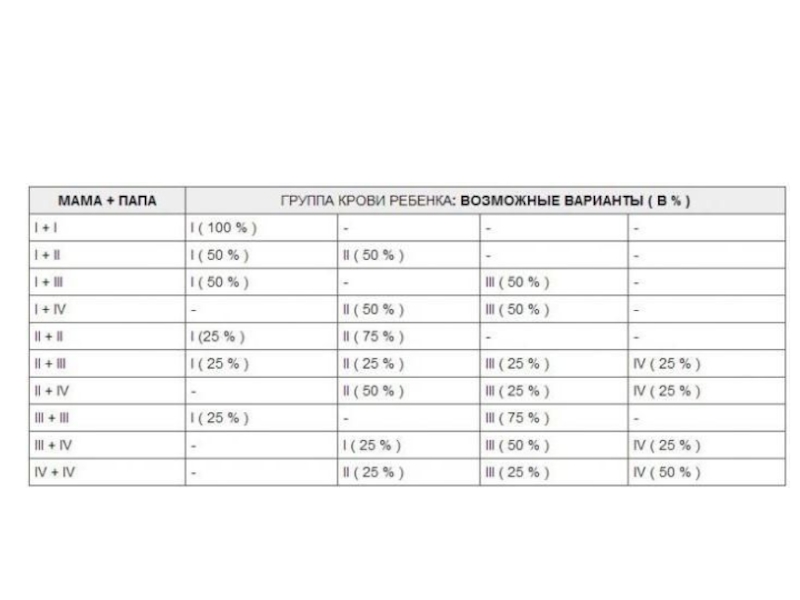
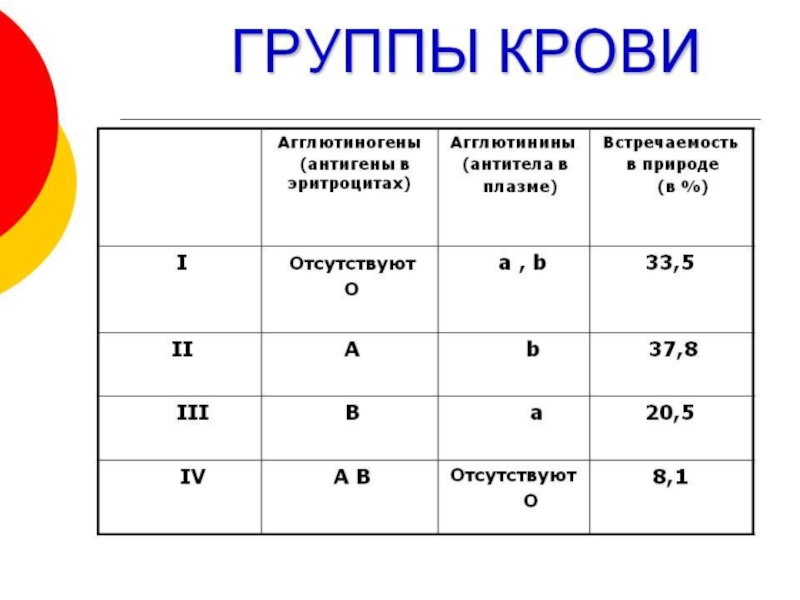
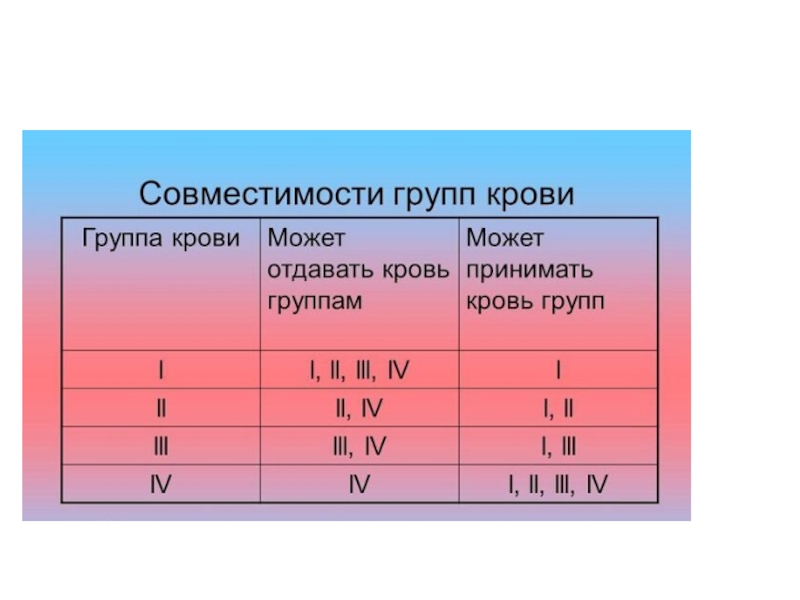
Презентация, доклад Кровь. Химические свойства
Содержание
- 1. Презентация. Кровь. Химические свойства
- 2. В 1898 году ученый по фамилии Бунге,
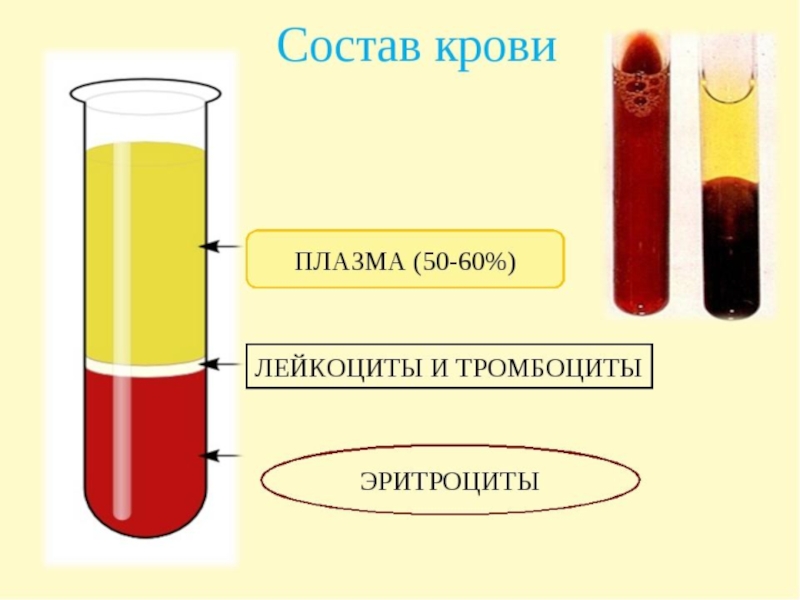
- 3. Слайд 3
- 4. Во времена второй мировой войны А. Бабкиным
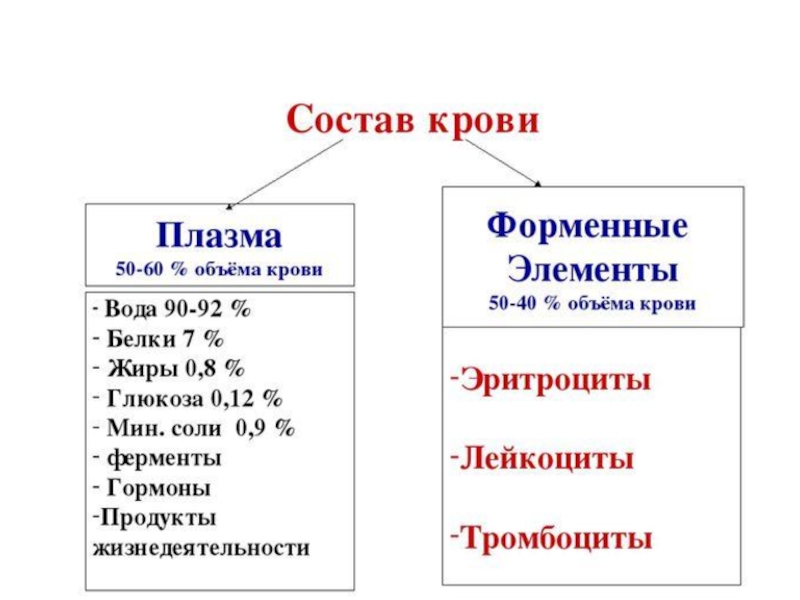
- 5. Слайд 5
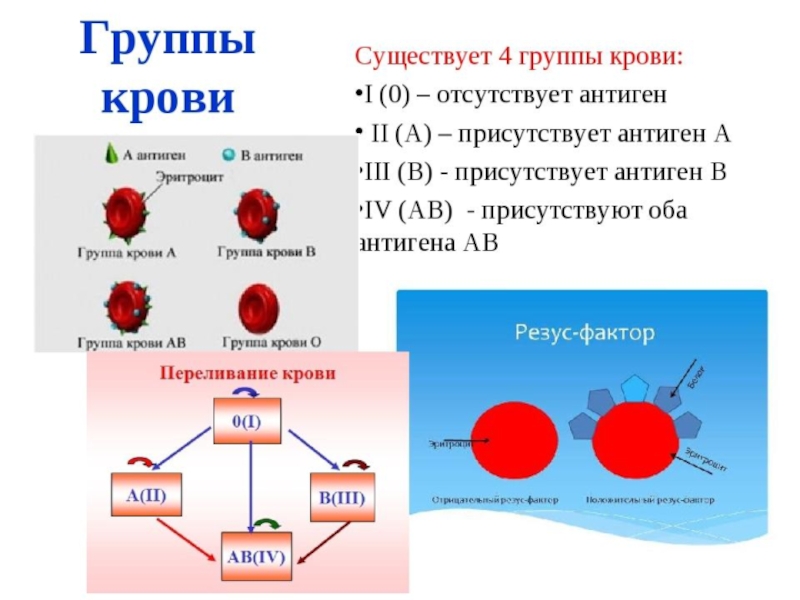
- 6. Слайд 6
- 7. Слайд 7
- 8. Слайд 8
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
- 17. Слайд 17
- 18. Слайд 18
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
- 23. Слайд 23
- 24. Слайд 24
- 25. Слайд 25
- 26. Слайд 26
- 27. Слайд 27
- 28. Слайд 28
- 29. Слайд 29
- 30. Слайд 30
- 31. Слайд 31
- 32. Слайд 32
- 33. Слайд 33
- 34. Слайд 34
- 35. Слайд 35
- 36. Слайд 36
- 37. Хлори́д на́трия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту
- 38. Слайд 38
- 39. Слайд 39
- 40. Слайд 40
- 41. Пример расчета и методика приготовления раствораЗадание: Приготовить 100
- 42. при изменении концентрации раствора на 2 %
- 43. Выполнение опыта.В мерный цилиндр наливают раствор хлорида
- 44. Слайд 44
- 45. Слайд 45
- 46. Слайд 46
- 47. Слайд 47
- 48. Слайд 48
- 49. Слайд 49
- 50. Слайд 50
- 51. Слайд 51
- 52. Слайд 52
- 53. Слайд 53
- 54. Слайд 54
- 55. Слайд 55
- 56. Слайд 56
- 57. Слайд 57
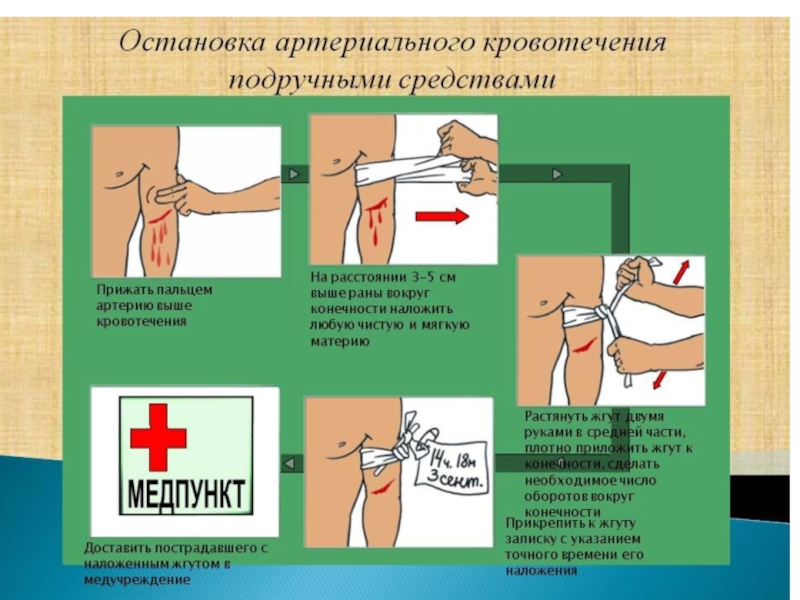
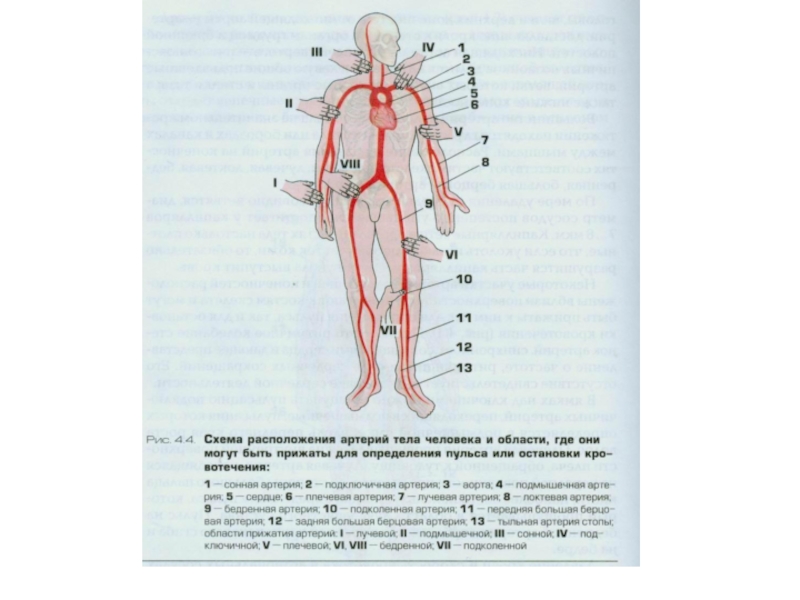
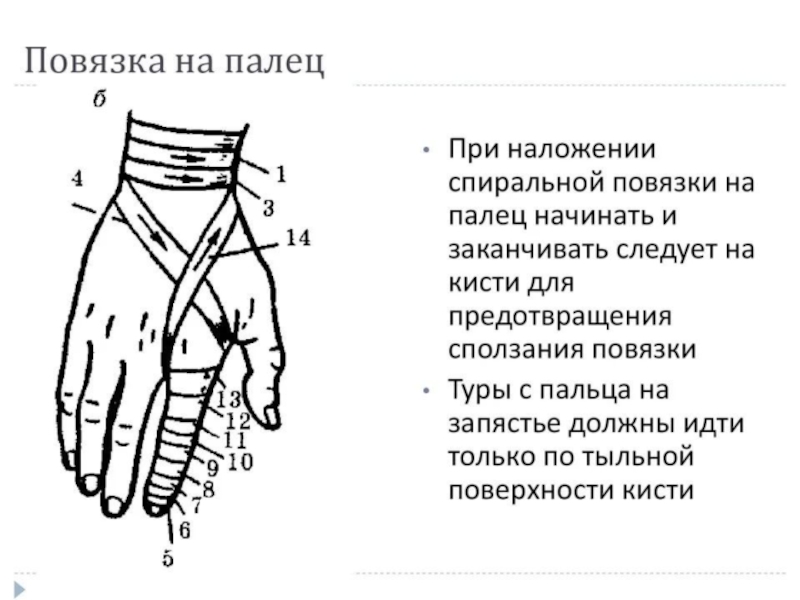
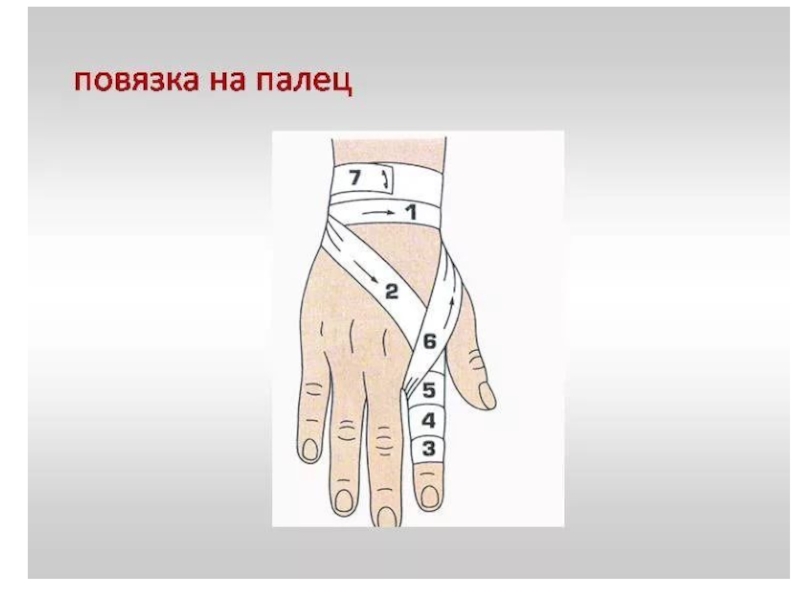
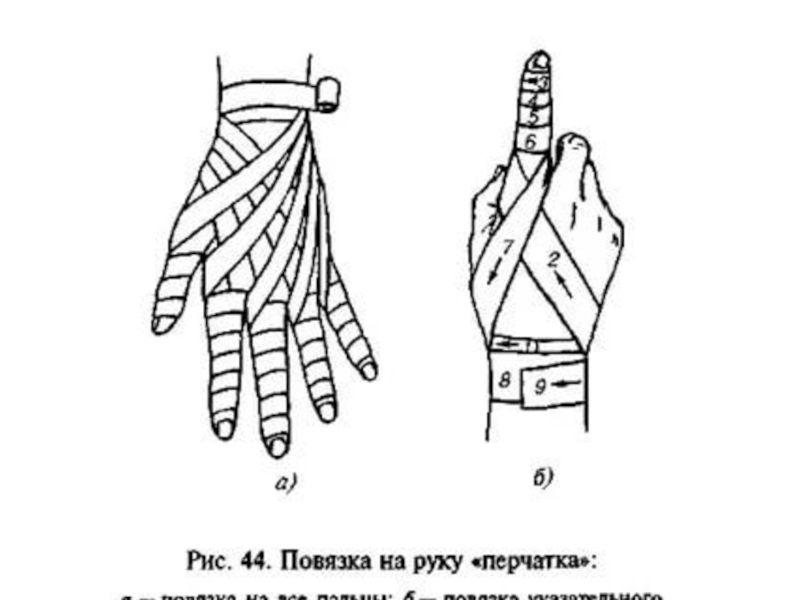
- 58. Бинт (нем. Binde — тесьма, повязка) — полоска ткани (марли, холста, полотна, фланели), используемая для перевязки ран, наложения повязки, переплетения книг.
- 59. Структура медицинского бинта заключается в сложном переплетении
В 1898 году ученый по фамилии Бунге, высказал гипотезу о том, что жизнь зародилась в море. Он утверждал, что животные, живущие сегодня, унаследовали от своих прародителей неорганический состав крови. Ученые, так же, вывели формулу морской воды
Слайд 4Во времена второй мировой войны А. Бабкиным и В. Сосновским был
предложен препарат морской воды для восполнения кровопотери раненых. Этот препарат вошел в историю под названием раствора АМ-4 Бабского.
Каков же состав морской воды и как он действует на нас?
Морская соль – обычный хлорид натрия. В процентном соотношении в морской воде его содержится столько же, сколько и в теле здорового человека. Поэтому купание в море способствует поддержанию нормального кислотно-щелочного баланса в нашем организме и благотворно воздействует на кожу.
Кальций прогоняет депрессию, способствует хорошему сну и гарантирует отсутствие судорог, принимает участие в свертываемости крови, играет большую роль в заживлении ран, предупреждении инфекций и укрепляет соединительные ткани.
Магний защищает от аллергии, нервозности, снимает отёчность, участвует в клеточном обмене и расслаблении мышц.
Бром успокаивает нервную систему.
Сера благотворно влияет на кожу и борется с грибковыми заболеваниями.
Йод необходим для щитовидной железы, влияет на интеллектуальные способности, гормональный обмен, понижает уровень холестерина в крови , омолаживает клетки кожи.
Калий участвует в регулировании питания и очистке клетки.
Хлор участвует в образовании желудочного сока и плазмы крови.
Марганец участвует в формировании костной ткани и укрепляет иммунную систему.
Цинк участвует в формировании иммунитета, поддержании функции половых желез, препятствует росту опухолей.
Железо участвует в транспортировке кислорода и в процессе образования эритроцитов.
Селен предотвращает онкологические заболевания.
Медь препятствует развитию анемии.
Кремний придает эластичность сосудам и укрепляет ткани.
Слайд 37Хлори́д на́трия или хлористый натрий (NaCl) — натриевая соль соляной кислоты. Известен в быту под названием поваренной соли, основным
компонентом которой и является. Хлорид натрия в значительном количестве содержится в морской воде, придавая ей солёный вкус. Встречается в природе в виде минералагалита (каменной соли). Чистый хлорид натрия представляет собой бесцветные кристаллы, но с различными примесями его цвет может принимать голубой, фиолетовый, розовый, жёлтый или серый оттенок.
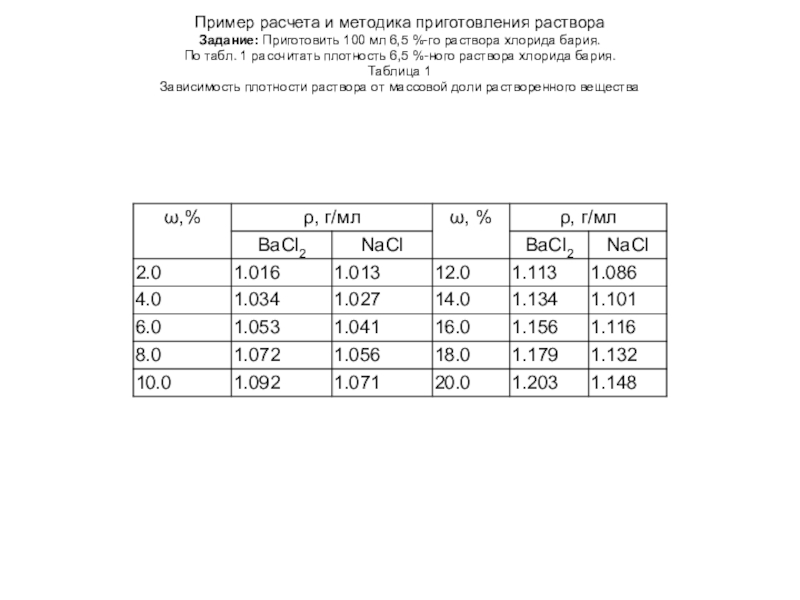
Слайд 41Пример расчета и методика приготовления раствора
Задание: Приготовить 100 мл 6,5 %-го раствора
хлорида бария.
По табл. 1 рассчитать плотность 6,5 %-ного раствора хлорида бария.
Таблица 1
Зависимость плотности раствора от массовой доли растворенного вещества
По табл. 1 рассчитать плотность 6,5 %-ного раствора хлорида бария.
Таблица 1
Зависимость плотности раствора от массовой доли растворенного вещества
Слайд 42при изменении концентрации раствора на 2 % плотность изменяется на 0,019
г/мл (1,072-1,053)
при изменении концентрации раствора на 0,5 % плотность изменяется на х г/мл
х = 0,005 г/мл.
Плотность 6,5 %-ного раствора равна: сумме 6,0 %-ного раствора и х.
ρ6,5% = ρ6% + ρ0,5% = 1,053 + 0,005 = 1,058 г/мл.
2. Рассчитать массу заданного раствора:
mp-pa= V ∙ p = 100 ∙ 1,058 = 105,80 г.
3. Рассчитать массу растворенного вещества:
m(ВаС12) = mр-ра ∙ ω = 105,80 ∙ 0,065 = 6,88 г.
4. На технохимических весах взвесить 6,88 г ВаС12.
5. С помощью стеклянной воронки перенести соль в мерную колбу на 100 мл, смыть дистиллированной водой остатки соли с воронки и довести объем до метки. Закрыть колбу пробкой и перемешать раствор, переворачивая колбу до исчезновения кристаллов соли.
6 . С помощью ареометра измерить плотность полученного раствора (рис. 1). Для этого перелить раствор в цилиндр, подобрать ареометр по плотности раствора. Измерение плотности проводить под руководством преподавателя. Предположим, что плотность полученного раствора ρэксп = 1,059 г/мл.
7. Определить концентрацию полученного раствора ωэксп, используя метод интерполяции
при изменении концентрации раствора на 0,5 % плотность изменяется на х г/мл
х = 0,005 г/мл.
Плотность 6,5 %-ного раствора равна: сумме 6,0 %-ного раствора и х.
ρ6,5% = ρ6% + ρ0,5% = 1,053 + 0,005 = 1,058 г/мл.
2. Рассчитать массу заданного раствора:
mp-pa= V ∙ p = 100 ∙ 1,058 = 105,80 г.
3. Рассчитать массу растворенного вещества:
m(ВаС12) = mр-ра ∙ ω = 105,80 ∙ 0,065 = 6,88 г.
4. На технохимических весах взвесить 6,88 г ВаС12.
5. С помощью стеклянной воронки перенести соль в мерную колбу на 100 мл, смыть дистиллированной водой остатки соли с воронки и довести объем до метки. Закрыть колбу пробкой и перемешать раствор, переворачивая колбу до исчезновения кристаллов соли.
6 . С помощью ареометра измерить плотность полученного раствора (рис. 1). Для этого перелить раствор в цилиндр, подобрать ареометр по плотности раствора. Измерение плотности проводить под руководством преподавателя. Предположим, что плотность полученного раствора ρэксп = 1,059 г/мл.
7. Определить концентрацию полученного раствора ωэксп, используя метод интерполяции
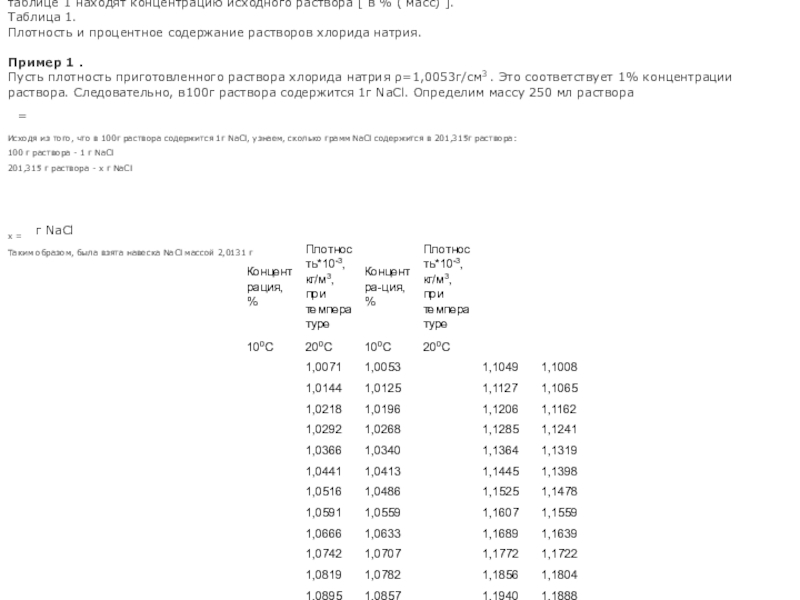
Слайд 43Выполнение опыта.В мерный цилиндр наливают раствор хлорида натрия и ареометром определяют
его плотность. По таблице 1 находят концентрацию исходного раствора [ в % ( масс) ].
Таблица 1.
Плотность и процентное содержание растворов хлорида натрия.
Пример 1 .
Пусть плотность приготовленного раствора хлорида натрия ρ=1,0053г/см3 . Это соответствует 1% концентрации раствора. Следовательно, в100г раствора содержится 1г NaCl. Определим массу 250 мл раствора
=
Исходя из того, что в 100г раствора содержится 1г NaCl, узнаем, сколько грамм NaCl содержится в 201,315г раствора:
100 г раствора - 1 г NaCl
201,315 г раствора - х г NaCl
х = г NaCl
Таким образом, была взята навеска NaCl массой 2,0131 г
Таблица 1.
Плотность и процентное содержание растворов хлорида натрия.
Пример 1 .
Пусть плотность приготовленного раствора хлорида натрия ρ=1,0053г/см3 . Это соответствует 1% концентрации раствора. Следовательно, в100г раствора содержится 1г NaCl. Определим массу 250 мл раствора
=
Исходя из того, что в 100г раствора содержится 1г NaCl, узнаем, сколько грамм NaCl содержится в 201,315г раствора:
100 г раствора - 1 г NaCl
201,315 г раствора - х г NaCl
х = г NaCl
Таким образом, была взята навеска NaCl массой 2,0131 г
Слайд 58Бинт (нем. Binde — тесьма, повязка) — полоска ткани (марли, холста, полотна, фланели), используемая для перевязки ран, наложения
повязки, переплетения книг.
Слайд 59Структура медицинского бинта заключается в сложном переплетении хлопчатобумажных нитей, вида — полотняное
переплетение нитей. Ткань бинта состоит из двух переплетающихся систем нитей, расположенных взаимно перпендикулярно. Систему нитей, идущих вдоль ткани, называют основой, а систему нитей, расположенных поперек ткани, — утком. Соответствующие нити называют основными и уточными. Переплетение нитей в ткани бинта является одним из основных показателей. Нити основы и утка последовательно переплетаются друг с другом в определенном порядке, в зависимости от минимального числа нитей — раппорта, влияющих на плотность и вид медицинского средства — бинта.
Классификация
Классификация