- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок. Презентация Гидролиз солей
Содержание
- 1. Урок. Презентация Гидролиз солей
- 2. Слайд 2
- 3. Гидролиз — это реакция обменного разложения веществ водой.
- 4. Классификация солейсоли1 тип: образованы сильным основанием и
- 5. Соли, образованные сильным основанием и сильной кислотойNaNO3
- 6. CuCl2 Cu2+ + 2Cl-Cu2+ + 2Cl-
- 7. Соли, образованные сильным основанием и слабой кислотойNa2
- 8. Соли, образованные слабым основанием и слабой
- 9. Проверь себяЗадание 2:Определите окраску лакмуса в растворах
- 10. Проверь себя Задание 3:Исключите лишнюю соль из списка:А)
- 11. Гидролиз органических веществ.1. Гидролиз галогеналканов. С2Н5Сl +
- 12. https://learningapps.org/display?v=pbj0srr1ahttps://learningapps.org/display?v=pbj0srr1a
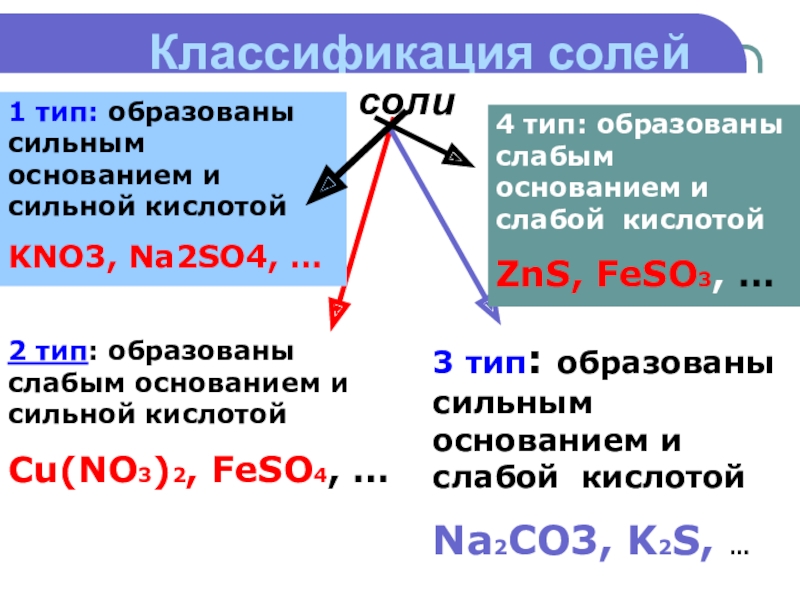
Слайд 4Классификация солей
соли
1 тип: образованы сильным основанием и сильной кислотой
KNO3, Na2SO4, …
2
Сu(NO3)2, FeSO4, …
3 тип: образованы сильным основанием и слабой кислотой
Na2CO3, K2S, …
4 тип: образованы слабым основанием и слабой кислотой
ZnS, FeSO3, …
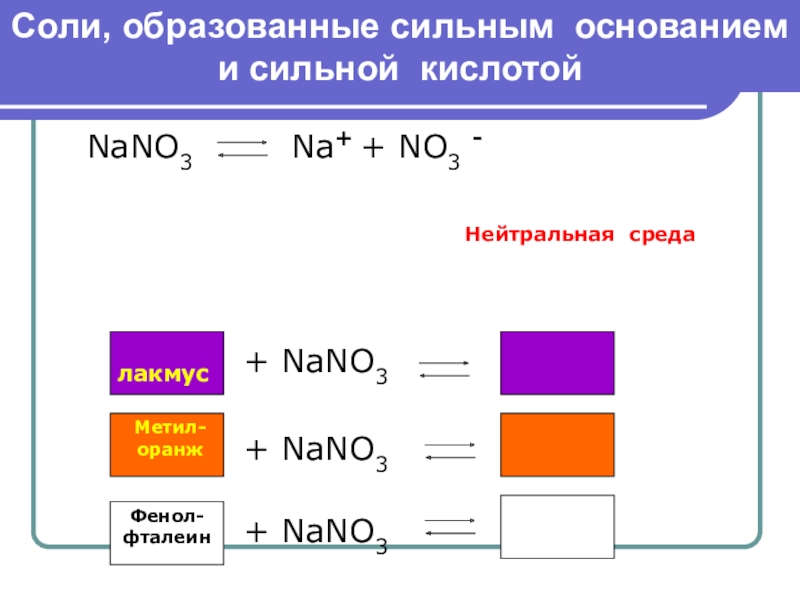
Слайд 5Соли, образованные сильным основанием и сильной кислотой
NaNO3
Нейтральная среда
лакмус
+ NaNO3
+ NaNO3
+ NaNO3
Метил-
оранж
Фенол-
фталеин
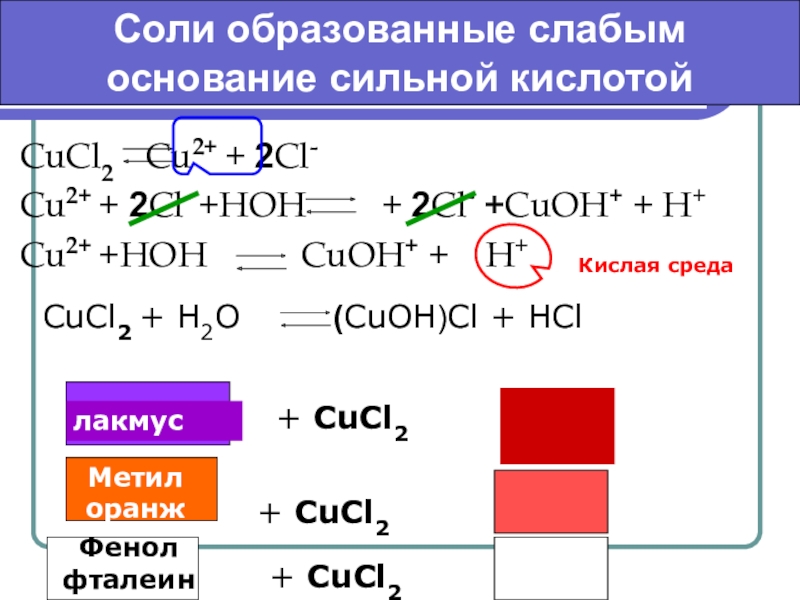
Слайд 6CuCl2 Cu2+ + 2Cl-
Cu2+ + 2Cl- +HOH
Cu2+ +HOH CuOH+ + H+
Кислая среда
CuCl2 + H2O (CuOH)Cl + HCl
лакмус
+ CuCl2
+ CuCl2
+ CuCl2
Метил
оранж
Фенол
фталеин
Соли образованные слабым
основание сильной кислотой
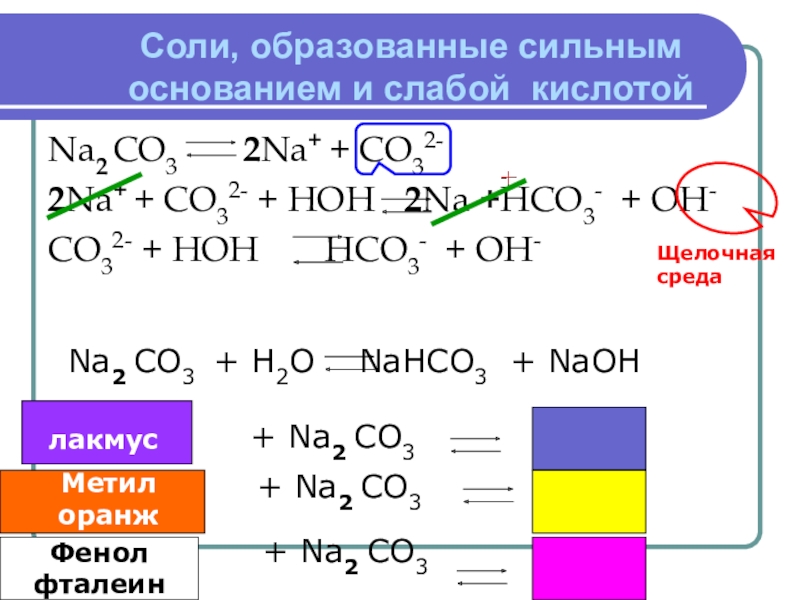
Слайд 7Соли, образованные сильным основанием и слабой кислотой
Na2 CO3
2Na+ + CO32- + HOH 2Na +HCO3- + OH-
CO32- + HOH HCO3- + OH-
Щелочная среда
Na2 CO3 + H2O NaHCO3 + NaOH
лакмус
+ Na2 CO3
+ Na2 CO3
+ Na2 CO3
Метил
оранж
Фенол
фталеин
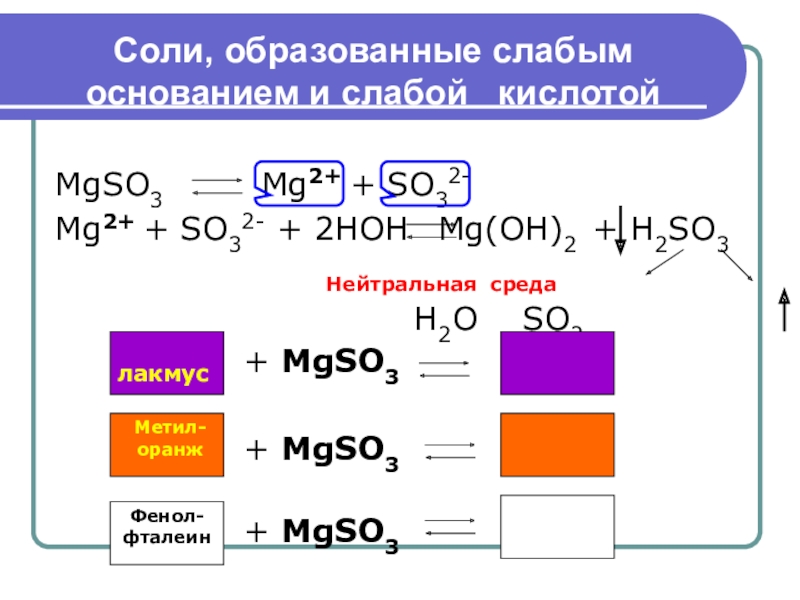
Слайд 8Соли, образованные слабым основанием и слабой кислотой
MgSO3
Mg2+ + SO32- + 2HOH Mg(OH)2 + H2SO3
H2O SO2
Нейтральная среда
лакмус
+ MgSO3
+ MgSO3
+ MgSO3
Метил-
оранж
Фенол-
фталеин
Слайд 9Проверь себя
Задание 2:
Определите окраску лакмуса в растворах солей:
Ba(NO3)2, FeCl3, LiNO2, CoSO4,
Приведите примеры возможных реакций (по одному для каждого типа соли)
Слайд 10Проверь себя
Задание 3:
Исключите лишнюю соль из списка:
А) ZnCl2, CuSO4, KNO3, Ni(NO3)2
Б)
В) Na2S, CaCl2, Li3PO4, K2CO3
Г) KNO3, MgBr2, Na2SO4, CaI2
Д) SnCl2, Al(NO3)3, PbSO4, Fe2(SO4)3
Напишите уравнения реакций гидролиза выбранных вами солей
Слайд 11Гидролиз органических веществ.
1. Гидролиз галогеналканов.
С2Н5Сl + Н2О →С2Н5ОН + НСl
2.
СН3-СОО-С2Н5 + Н2О → СН3-СООН +С2Н5ОН
3. Гидролиз дисахаридов.
С12Н22О11 + Н2О →С6Н12О6 + С6Н12О6
4. Гидролиз полисахаридов.
(С6Н10О5)n + nН2О →nС6Н12О6