- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Проект на тему Методика изучения темы Углеводороды школьного курса химии
Содержание
- 1. Проект на тему Методика изучения темы Углеводороды школьного курса химии
- 2. Слайд 2
- 3. Слайд 3
- 4. Слайд 4
- 5. Возможности содержания темы для воспитания и развития
- 6. - Решение задач при обобщении знаний учащихся для
- 7. В начале и конце учебного года можно
- 8. Во внеурочное время-проведение экологической конференции «Сохраним мир
- 9. Патриотическое воспитание через -
- 10. В теме «Алканы» при рассмотрении процессов переработки
- 11. Рассматривая применение нефтепродуктов, можно сообщить учащимся, что
- 12. Разбирая применение углеводородов и их производных, можно
- 13. Развитие коммуникативных качеств у учащихся на уроке
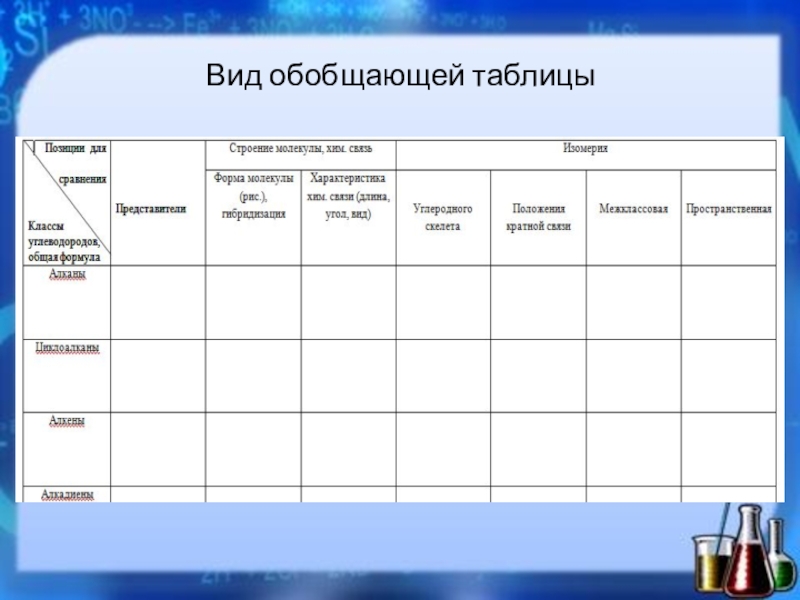
- 14. Вид обобщающей таблицы
- 15. Карточка с заданием
- 16. Проблемный подход в изучении темы.
- 17. - при изучении непредельных
- 18. -
- 19. Ведущим противоречием при изучении бензола является несоответствие
- 20. Дидактические материалы к темеТема
- 21. На уроках химии рекомендовано проведение лабораторных
- 22. Карточки с текстом задач
- 23. Раздаточный материал
- 24. Слайд 24
- 25. Слайд 25
- 26. Химический диктантДиктант №_ «УГЛЕВОДОРОДЫ» Вариант №1
- 27. Ситуационные задачиВы решили обработать дихлорэтаном пустой склад
- 28. материалы для контроля знаний- текущий контроль
- 29. Слайд 29
- 30. итоговый контроль
- 31. Тематическое планирование
- 32. Цели и задачи изучения темы
- 33. Анализ
- 34. Анализ структуры урока Структура
- 35. Анализ содержания урокаСодержание урока соответствует программе –
- 36. Межпредметные связи: физика (агрегатные
- 37. Анализ методов и средств обученияНа уроке
- 38. На
- 39. Шаростержневые модели (для изучения строения молекул алканов)
- 40. Слайд 40
- 41. Вывод формул органических веществ по общим формулам.
- 42. Алгоритм составления названия алканов.1.В структурной формуле выбирают
- 43. Карта- инструкция демонстрационного опыта(изучение способов получения алканов)
- 44. для первичного закрепления знаний
- 45. Слайд 45
- 46. Список литературы:Методические основы обучения химии – И.М.
- 47. СПАСИБО ЗА ВНИМАНИЕ!
Слайд 2
Данная тема относится к разделу «Органическая химия» школьного курса химии.
Начинает изучаться с 10го класса с темы «Алканы».
Изучение проходит на следующей теоретической основе: теория строения органических соединений А.М. Бутлерова, понятие химической связи в орг.соединениях, гибридизация орбиталей, типы химических реакций орг. соединений.
Слайд 3
1.Образовательные:
- сформировать знания об общей характеристике углеводородов и их классификации, физических и химических свойствах алканов, алкенов, алкинов, аренов, циклоалканов, алкадиенов;
- сформировать представление об областях применения углеводородов;
- сформировать навыки решения задач на вывод химических формул органических веществ.
2.Развивающие:
-развить умения анализировать, сравнивать;
- развивать умение работать с учебником, дополнительной литературой, умение решать задачи;
- развивать интеллектуальные способности учащихся.
3.Воспитательные:
воспитывать умение выступать, слушать своих товарищей, работать в группе.
Слайд 4
знать: - понятия - углеродный скелет; изомерия, виды изомерии; гомология; гибридизация, сигма и пи-связи; мономер, полимер, структурное звено, степень полимеризации.
-физические свойства углеводородов;
- химические свойства углеводородов;
- типовые механизмы химических реакций;
- промышленные и лабораторные способы получения УВ.
уметь: - определять класс органического соединения, принадлежность веществ к этим классам по формулам, химические свойства вещества по его строению
- составлять формулы изомеров и гомологов; составлять уравнения химических реакций, характеризующих свойства углеводородов разных классов, уравнения реакций, характеризующие основные способы получения углеводородов;
- писать электронную и графическую формулу атома углерода;
- объяснять три валентных состояния атома углерода;
- приводить примеры химических реакций подтверждающих взаимосвязь различных классов углеводородов.
владеть: - алгоритмами решения задач на вывод формул органических соединений, составления названий орг. соединений изученных классов.
Слайд 5Возможности содержания темы для воспитания и развития учащихся
Экологическое воспитание через:
На уроках
Обсуждение
Включение в материал сведений о розливе в результате аварий нефти и ее отрицательного влияния на живые организмы
Слайд 6
- Решение задач при обобщении знаний учащихся для более глубокого понимания природных
Карточка- задание №_
Решите задачу:
▪ Накопление углекислого газа в атмосфере становится опасным загрязнением – приводит к парниковому эффекту. Какой объем CO2 попадает в атмосферу при сжигании 100 г полиэтилена (100 шт. использованных пакетов)?
Слайд 7В начале и конце учебного года можно провести эколого-психологический тест
Экспресс-методика оценки развитости экологического сознания позволяет определить склонность к экоцентризму или антропоцентризму.
Слайд 8Во внеурочное время
-проведение экологической конференции «Сохраним мир вокруг нас»
Темы докладов:
«Мусорный шанс»
«Пути
«Планета бушует»
«Проблема загрязнения воздуха городским транспортом»
«Проблема очистки питьевой воды»
«Влияние загрязнений на поведение животных»
«Исследование состояния водных объектов/воздуха Тулы/ТО»
Слайд 9
Патриотическое воспитание через
- сообщение учителем на
В теме «Ароматические УВ» рассматривая применение
Толуол является сырьем для получения тринитротолуола, торговое название которого - тротил. Тротил применяется в качестве заряда в разрывных снарядах, подводных минах, торпедах и т.д. В мирной технике применяется как примесь к горным взрывчатым веществам. Синтез толуола, из которого был получен тротил, выполнил в 1941г. академик Ю.Г. Мамедалиев.
Слайд 10
В теме «Алканы» при рассмотрении процессов переработки нефти можно отметить роль
Благодаря работам Зелинского Н.Д. был получен синтетический бензин с более высоким октановым числом, чем природный. Новый бензин дал возможность резко увеличить мощность моторов и скорость самолетов. Самолет смог взлетать с меньшего разбега, подниматься на большую высоту, с большим грузом. Эти исследования оказали неоценимую помощь нашей авиации в годы ВОВ. За работы по химии нефти академику Н.Д. Зелинскому в 1946г. была присуждена Государственная премия.
Слайд 11
Рассматривая применение нефтепродуктов, можно сообщить учащимся, что на основе бензина изготовляют
Напалм - зажигательное оружие, предназначенное для поражения живой силы и объектов. Состоит из живого горючего (бензина, керосина и др.) и порошка загустителя. Напалм был одним из главных видов химического оружия армии США в Корее в 1968-1970гг. На земле Южного Вьетнама американские наемники сбросили 200 тысяч тонн напалма.
Слайд 12
Разбирая применение углеводородов и их производных, можно сообщить учащимся
Слайд 13Развитие коммуникативных качеств у учащихся на уроке обобщения
«Строение УВ,
Для проведения данного урока можно воспользоваться методом обучение в малых группах сотрудничества.
В аспекте развития цель урока- научить школьников эффективно работать в группе, а основная задача развить коммуникативные навыки.
Слайд 16
Проблемный подход в изучении темы.
Изучение всего основного содержания органической
- при изучении предельных углеводородов :
ознакомление с тетраэдрическим строением молекулы метана требует выяснения причин такой геометрической формы, а позднее возникает вопрос о причине зигзагообразного строения углеродной цепи.
Слайд 17 - при изучении непредельных
Выяснение молекулярного состава этилена приводит к противоречию с валентностью элементов и требует обратиться к выяснению строения молекулы. Двойная связь между атомами углерода не может быть понята на основе только что введения в курс электронных представлений и требует более глубокого рассмотрения электронного строения. (возникает понятие о механизме образования пи-связи, о влиянии ее на свойства вещества, затем возникает проблема проверки этих причинно-следственных связей на других веществах)
Слайд 18 - при изучении
реакция полимеризации этилена приводит к установлению химического строения полимера и его сходства, в этом отношении с парафинами. На этой основе возникает мысль о проверке сходства их химических свойств, затем встает проблема их практического использования.
Специфическое свойство, обнаруженное у полимеров термопластичность, порождает новую проблему – как на его основе можно осуществить производство разного рода изделий из полимеров.
Слайд 19Ведущим противоречием при изучении бензола является несоответствие его молекулярного состава наблюдаемым
Слайд 20 Дидактические материалы к теме
Тема Углеводороды предполагает использование большого
Наглядным и эффективным является использование презентаций и видеофрагментов
углеводороды.углеводороды.pptx
Полиэтилен.Полиэтилен.mp4
Слайд 21 На уроках химии рекомендовано проведение лабораторных работ.
Необходимым является предоставление
Лабораторная работа 1. Лабораторная работа 1.docx
Слайд 22
Карточки с текстом задач
Вывод молекулярной формулы углеводородов на основе массовой доли элементов и его плотности.
Задание: Решите следующие задачи, пользуясь алгоритмом.
1.Выведите молекулярную формулу органического соединения, содержащего 80% углерода и 20% водорода, если его плотность по водороду равна 15. (C2Н6)
2.Выведите формулу вещества, содержащего 93.75% углерода и 6.25% водорода, если плотность паров его по воздуху равна 4.41. (C6Н6)
3.Найдите молекулярную формулу углеводорода, массовая доля углерода в котором составляет 92.3%. Относительная плотность паров этого вещества по водороду 39. (C6Н6)
Слайд 23Раздаточный материал
Алгоритм решения задач на вывод формулы вещества.
Обозначить формулу вещества с помощью индексов x, y, z и т. д. по числу элементов в молекуле.
Если в условии не дана массовая доля одного элемента, вычислить ее как разность 100% и массовых долей всех остальных элементов.
Найти отношение индексов x : y : z как отношение частных от деления массовой доли элемента на его относительную атомную массу. Привести частные от деления к отношению целых чисел. Определить простейшую формулу вещества.
В задачах на нахождение формул органических веществ часто требуется сравнить относительную молекулярную массу простейшей формулы Mr с истинной, найденной по условию задачи (чаще всего плотности по воздуху или по водороду). Отношение этих масс дает число, на которое надо умножить индексы простейшей формулы.
Слайд 24
Установление молекулярной формулы вещества по продуктам сгорания.
Задание: Решите следующие задачи.
1. При сгорании 5.6л газа получен оксид углерода IV объемом 16.8л и вода массой 13.5 г. 1л газа при н.у. имеет массу 1.875г. Выведите формулу газа (С3H6).
2. При сгорании углеводорода массой 4.3г образовался оксид углерода IV массой 13.2г. Плотность паров его по водороду равна 43. Выведите формулу углеводорода (С6H14).
3. При сгорании алкена массой 0.7г образовались углекислый газ и вода количеством вещества по 0.05 моль каждое. Плотность паров его по азоту равна 2.5. Вывести ф-лу вещества (С5Н10).
Слайд 25
Генетическая связь классов УВ.
Задание: Напишите уравнения реакций, с помощью которых можно осуществить цепочку превращений: алкан → алкен → алкин → арен → циклоалкан → алкан.
Слайд 26Химический диктант
Диктант №_ «УГЛЕВОДОРОДЫ»
Вариант №1
1. Напишите общую формулу аренов.
2. К какому
Слайд 27Ситуационные задачи
Вы решили обработать дихлорэтаном пустой склад для овощей площадью 100
2. У сельскохозяйственных животных при недостатке каких-либо компонентов питания в рационе появляются отклонения в поведении: они пытаются поедать несъедобные предметы. Так животные инстинктивно пытаются восполнить недостающие им элементы питания. Например, животноводы замечают, что дефицит серы в организме крупного рогатого скота проявляется не только в уменьшении прочности копыт, выпадении шерсти, но и в том, что животные пытаются жевать резиновые сапоги работников фермы. Почему именно в резине ищут животные источник недостающего элемента?
Слайд 31 Тематическое планирование
Темы школьного
(учебник : Химия 10 класс О.С. Габриелян, Ф.Н. Маскаев, С.Ю. Пономарев, В.И. Теренин- Москва, Дрофа 2000.)
Составлено на основе
«Программа курса химии для 8 – 11 классов общеобразовательных учреждений. Габриелян О.С»
Общее число на изучение темы: 10 ч.
Тематическое планирование.Тематическое планирование.docx
Слайд 32
Цели и задачи изучения темы
Цель:
сформировать знания и
основные понятия об
общей характеристике углеводородов
Задачи:
развить умения определять класс органического соединения, составлять формулы изомеров и гомологов; составлять уравнения химических реакций, характеризующих свойства углеводородов разных классов, основные способы получения углеводородов, навыки решения задач на вывод формул.
Слайд 33 Анализ урока
Тема урока:
Тип: урок усвоения новых знаний
Проводится 1ым уроком в теме «Углеводороды»
Конспект урока для учителя выглядит следующим образом
Конспект урока- Алканы.Конспект урока- Алканы.docx
Слайд 34Анализ структуры урока
Структура урока (основные этапы):
1. Организационный
2. Сообщение темы и цели урока - 1 мин.
3. Формирование мотивации - 5 мин.
4. Актуализация опорных знаний - 5 мин.
5. Изучение нового материала - 20 мин.
6. Первичное закрепление знаний - 5мин.
7. Подведение итогов работы на уроке - 5 мин.
8. Комментирование домашнего задания - 2 мин.
Слайд 35Анализ содержания урока
Содержание урока соответствует программе –
в изучаемый материал
гомологический ряд, изомерия, номенклатура алканов, физ. свойства алканов.
Слайд 36Межпредметные
связи:
физика (агрегатные состояния веществ),
геометрия
(пространственная
Внутрипредметные связи:
Строение атома углерода(сигма- связь, sp3- гибридизация), теория строения орг.соединений, классификация орг. соединений
Слайд 37 Анализ методов и средств обучения
На уроке использованы методы:
Беседа,
рассказ,
работа с доской, книгой,
демонстрационный эксперимент
«Получение метана»
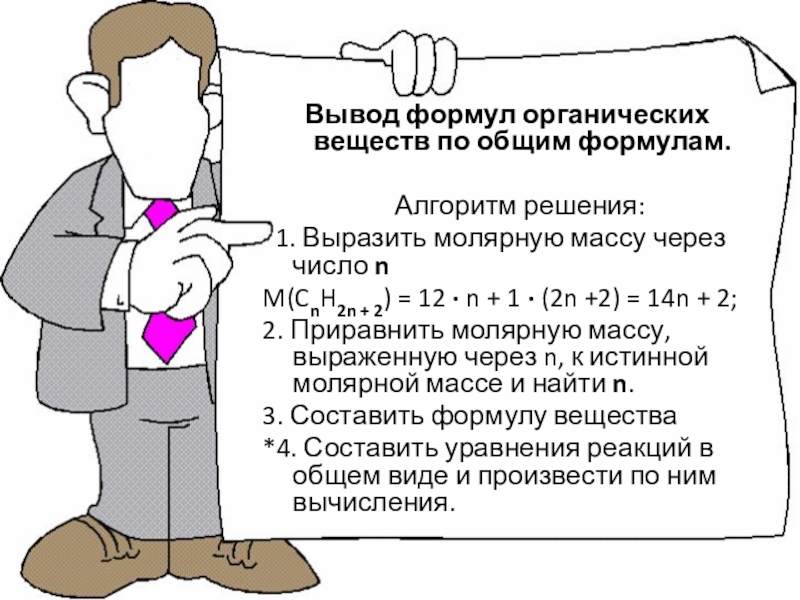
Слайд 41Вывод формул органических веществ по общим формулам.
1. Выразить молярную массу через число n
M(CnH2n + 2) = 12 ∙ n + 1 ∙ (2n +2) = 14n + 2;
2. Приравнить молярную массу, выраженную через n, к истинной молярной массе и найти n.
3. Составить формулу вещества
*4. Составить уравнения реакций в общем виде и произвести по ним вычисления.
Слайд 42Алгоритм составления названия алканов.
1.В структурной формуле выбирают самую длинную цепь атомов
2.Атомы углерода главной цепи нумеруют, начиная с того конца, к которому ближе стоит заместитель.
3.В начале названия указывают цифры- номера атомов углерода, при которых находятся заместители. После номера через дефис указывают количество заместителей (ди- два, три-три, тетра- четыре пента- пять).
4.Затем без пробеллов и дефисов указывают название главной цепи. Главная цепь называется как углеводород- член гомологического ряда метана.
Слайд 45
Вцелом урок
пониманием материала в
доброжелательной и
спокойной обстановке.
Учащиеся в ходе урока были
внимательны и активны.
Слайд 46Список литературы:
Методические основы обучения химии – И.М. Ахромушкина, Т.Н. Валуева, Е.Н
Чернобельская Г.М. Методика обучения химиив средней школе – М.,2000
Программа курса химии для 8 – 11 классов общеобразовательных учреждений. Габриелян О.С – М.: Дрофа, 2011.
Химия 10 класс – учебник для ОУЗ. Габриелян О.С. – М., Дрофа, 2000
Габриелян О. С. и др. «Химия. Контрольные и проверочные работы. 10 класс»
Габриелян О.С., Решетов П.В., Остроумов И.Г. «Задачи по химии и способы их решения. 10—11 классы»
Типы химических задач и способы их решения, 8-11 класс, Новошинский И.И., Новошинская Н.С., 2005.
Сборник ситуационных задач Жулькова Н.В.
https://infourok.ru/
http://www.pomochnik-vsem.ru/load/publikacii_pedagogov/khimija/sistema_diktantov_po_khimii_v_8_9_10_klassakh/21-1-0-3014
http://pedsovet.su/chemistry/