- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Строение атома 8 класс
Содержание
- 1. Презентация Строение атома 8 класс
- 2. 1891 годИрландский физик Стони вел понятие
- 3. 1897 годДЖ. Томсон предложил модель атома – «Пудинг с изюмом»электрон+
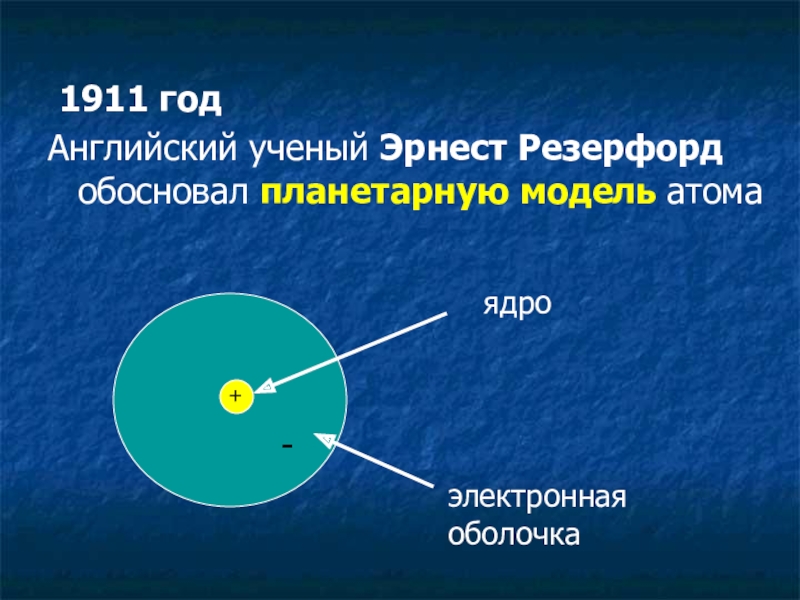
- 4. 1911 год Английский ученый Эрнест Резерфорд обосновал планетарную модель атома+ ядроэлектронная оболочка-
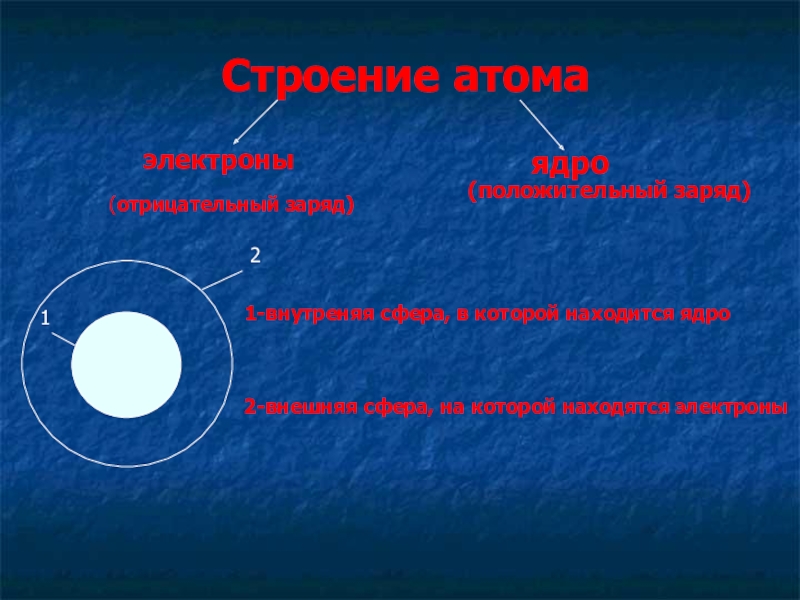
- 5. Строение атомаэлектроныядро1-внутреняя сфера, в которой находится ядро2-внешняя сфера, на которой находятся электроны(отрицательный заряд)(положительный заряд)
- 6. Планетарная модель атомаэлектрон+Общий заряд атома равен 0-3--
- 7. Слайд 7
- 8. ++ Строение
- 9. Строение атома водорода+-Протон (p+)Электрон (ē)Атом электронейтрален
- 10. Современная модель атомаАтом – электронейтральная частицаЯдро атома
- 11. Число протонов = заряду атомного ядра =
- 12. Состав ядра атомаПротоны. Масса = 1,
- 13. Масса атома – это масса его ядра.Число
- 14. ЗаданиеУкажите состав атома натрия Na1123p+ = 11ē
- 15. Изменения в составе ядер атомов1. Изменение числа протонов:+++++1НР+2He+Превращение одного химического элемента в другой – ядерная реакция
- 16. Химический элемент – это вид атомов с одинаковым зарядом ядра (с одинаковым числом протонов в ядре)
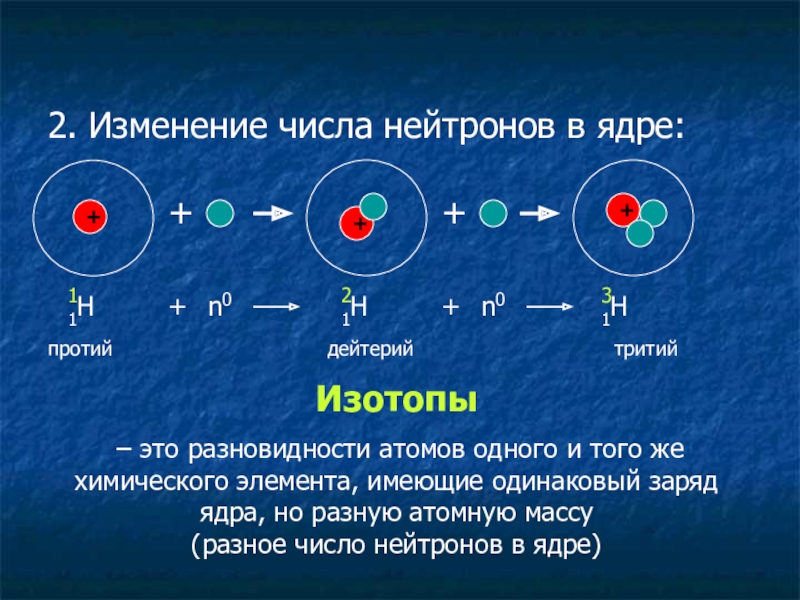
- 17. 2. Изменение числа нейтронов в ядре:+1Н++++1+n01Н21Н3+n0протийдейтерийтритийИзотопы –
- 18. 17 Сl3517 Сl3775% 25%Ar = 0.75 * 35 + 0.25 * 37 = 35.5
- 19. Домашнее задание - § 7;- Укажите состав
Слайд 21891 год
Ирландский физик Стони вел понятие
Английский физик Джозеф Томсон и
французский физик Жан Перен определили заряд, массу и скорость движения электрона.
Заряд = -1
m(ē)=1/1837 a.e
скорость=300 000 км/с
Слайд 4
1911 год
Английский ученый Эрнест Резерфорд обосновал планетарную модель
+
ядро
электронная оболочка
-
Слайд 5Строение атома
электроны
ядро
1-внутреняя сфера, в которой находится ядро
2-внешняя сфера, на которой находятся
(отрицательный заряд)
(положительный заряд)
Слайд 8
+
+
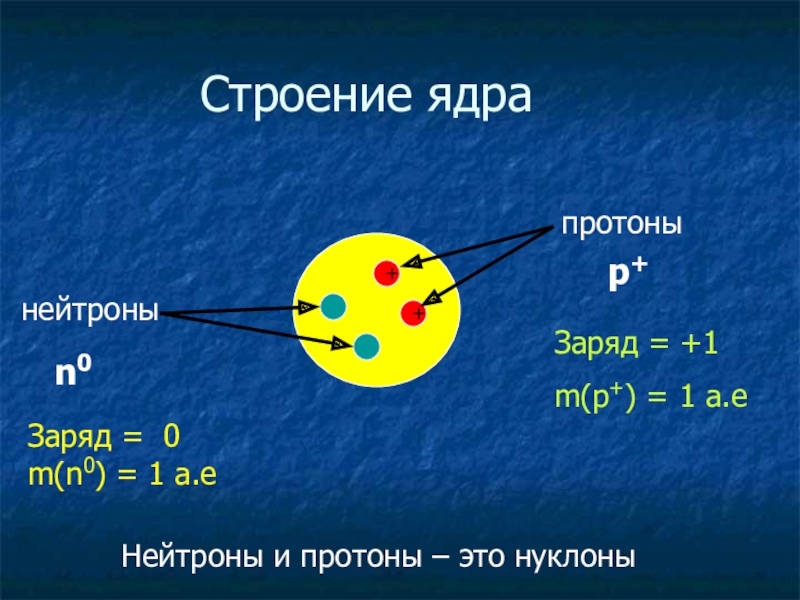
Строение ядра
протоны
нейтроны
n0
p+
Заряд = +1
m(p+) = 1 a.e
Заряд = 0
m(n0) = 1 a.e
Нейтроны и протоны – это нуклоны
Слайд 10Современная модель атома
Атом – электронейтральная частица
Ядро атома – положительно заряженное
Электроны –
Электроны вращаются вокруг
ядра с определённой скоростью
Слайд 11Число протонов = заряду атомного ядра = числу электронов =
=
Mg
12
Заряд ядра = +12
p+ = 12
Атомный номер →
ē = 12
Слайд 12Состав ядра атома
Протоны.
Масса = 1, заряд = +1
Нейтроны.
Масса = 1,
Заряд ядра определяется количеством протонов
Количество протонов соответствует порядковому номеру элемента в ПСХЭ
Слайд 13Масса атома – это масса его ядра.
Число протонов + число нейтронов
массовое число (А)
Число протонов = номеру элемента (Z)
Число нейтронов (N)=
Mg
24
12
Массовое число -
Атомный номер -
N = 24 – 12 = 12
А - Z
Слайд 14Задание
Укажите состав атома натрия
Na
11
23
p+ = 11
ē = 11
n0 = 23
Атом в ядре имеет 15 протонов.
Определите элемент.
Р
- фосфор
В атоме 53 электрона.
Определите элемент.
Заряд ядра = +11
I - иод
Слайд 15Изменения в составе ядер атомов
1. Изменение числа протонов:
+
+
+
+
+
1Н
Р+
2
He
+
Превращение одного химического элемента
ядерная реакция