- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад практической работы по химии на тему: Классы неорганических соединений (8 класс)
Содержание
- 1. Презентация практической работы по химии на тему: Классы неорганических соединений (8 класс)
- 2. Задачи:Научить определять вещества по качественным реакциям.Развивать умения
- 3. Цель: решить предложенные задачи практическим путём.Оборудование: пробирки
- 4. Опыт №2 Определить в какой пробирке каждое вещество?Цвет раствораголубойбесцветныйбесцветныйNa2SO4BaSO4белыйBaCl2BaSO4белый
- 5. Опыт №3 Получить веществоИз Mg
- 6. Опыт №4 Получить вещество.CuSO4
- 7. Опыт №5 Осуществить превращение
- 8. Решить предложенные задания.Систематизировать формулы оксидов по:
- 9. Тест 1. Выберите формулы оснований:
- 10. 4. Раствор гидроксида калия вступает в химические
- 11. 3. Закончите молекулярные уравнения возможных реакций:
- 12. Домашнее задание: № 4,5,7 стр. 112
Слайд 1Практическая работа
«Экспериментальное решение задач по теме:
«Классы неорганических соединений»».
Разработка учителя
МБОУ Спасская СОШ Рязанской области.
Слайд 2Задачи:
Научить определять вещества по качественным реакциям.
Развивать умения работать с лабораторным оборудованием
Воспитывать дисциплину и аккуратность при выполнении эксперимента, соблюдение правил техники безопасности.
Слайд 3Цель: решить предложенные задачи практическим путём.
Оборудование: пробирки в штативе, спиртовка, стакан
Реактивы: щёлочь, соляная кислота, сульфат натрия, хлорид бария.
Опыт №1
Доказать присутствие растворов:
Н2О; НСl; NaOH
Слайд 4Опыт №2
Определить в какой пробирке каждое вещество?
Цвет
раствора
голубой
бесцветный
бесцветный
Na2SO4
BaSO4
белый
BaCl2
BaSO4
белый
Слайд 5Опыт №3 Получить вещество
Из Mg Mg(OH)2
Mg
Mg + HCl = MgCl2 + H2
MgCl2 + NaOH = Mg(OH)2 + NaCl
Уравнять уравнения реакций!
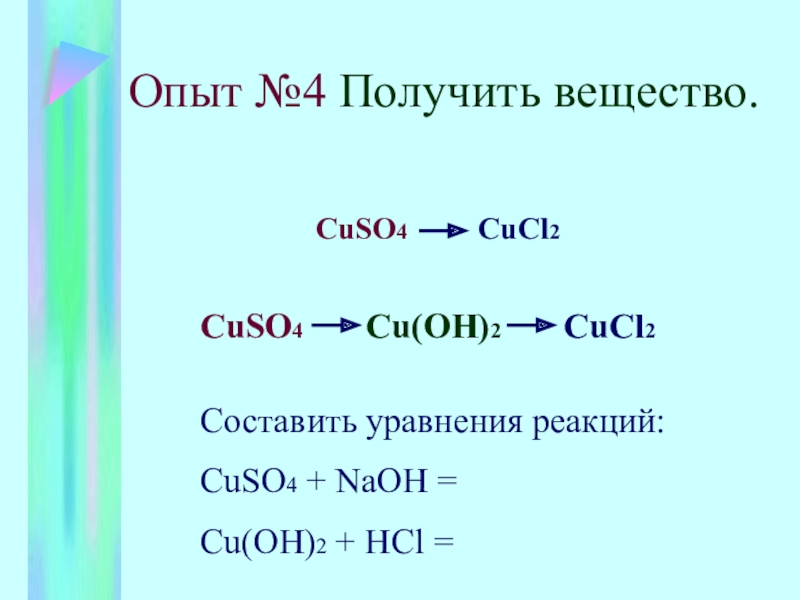
Слайд 6Опыт №4 Получить вещество.
CuSO4 CuCl2
CuSO4
Составить уравнения реакций:
CuSO4 + NaOH =
Cu(OH)2 + HCl =
Слайд 7Опыт №5
Осуществить превращение
FeCl3 Fe(OH)3
FeCl3 + … = Fe(OH)3 + …
Fe(OH)3 = Fe2O3 + …
Вывод: Кислоты и щёлочи можно определить с помощью индикатора, а соли качественными реакциями на их ионы.
(по таблице растворимости)
Слайд 8Решить предложенные задания.
Систематизировать формулы оксидов по:
а)
б) амфотерности
в) кислотности
Mn2O7, BaO, CO, MnO, Cr2O3, CrO, CrO3,
Al2O3, Cu2O, NO, NO2, SiO2, FeO, BeO.
BaO, MnO, CrO, Cu2O, FeO
Cr2O3, Al2O3, BeO
Mn2O7, CrO3, NO2, SiO2
Слайд 9Тест
1. Выберите формулы оснований:
а) SO3 б)
в) H2SO4 г) СаО
2. Если к указанным веществам прибавить воду и фенолфталеин. В каких случаях появится малиновое окрашивание?
а) BaO б) HNO3
в) CuO г) КОН
3. Какие из указанных гидроксидов не могут быть получены взаимодействием соответствующих оксидов с водой?
а) Аl(OH)3 б) Fe(OH)3
в) Са(ОН)2 г) LiOH
Слайд 104. Раствор гидроксида калия вступает в химические реакции с веществами, формулы
а) СО2 б) H2S в) Са(ОН)2
г) Cu д) NaNO3 e) Mg
5. Используя таблицу растворимости составьте формулы разных кислот, дайте им названия, определите основность.
Н, Н2, Н3 , S, NО3, РО4, СI, SО3, SiO3, BO3, SO4.
Слайд 113. Закончите молекулярные уравнения
возможных реакций:
Al2О3 + H Cl
Mg + H2SO4 = FeCl 3 + KOH =
HNO3 + Zn SO4 = Ca CO3 + HNO3 =
4 Выполните цепочку превращений:
S SO2 SO3 H2SO4 CuSO4
CuSO4
CuSO4
Проверьте свои знания