- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии Роль воды в химических реакциях
Содержание
- 1. Презентация по химии Роль воды в химических реакциях
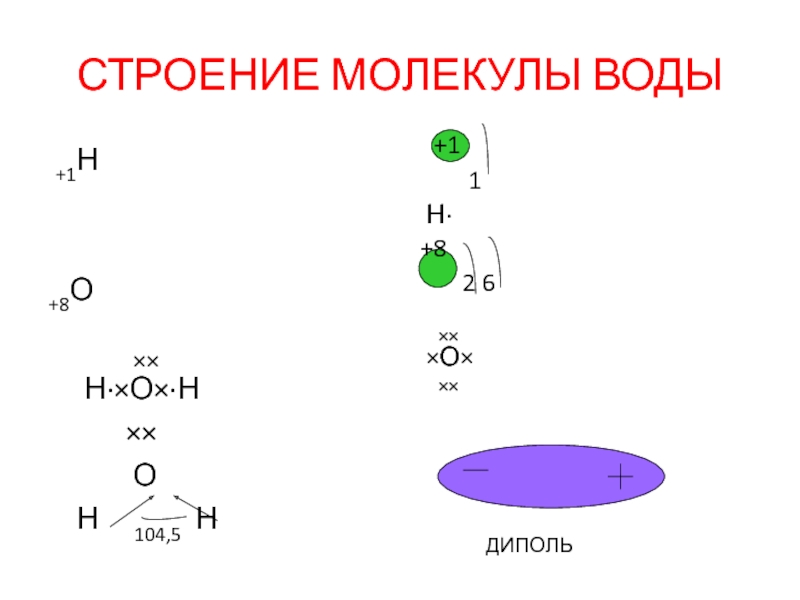
- 2. СТРОЕНИЕ МОЛЕКУЛЫ ВОДЫ +1Н
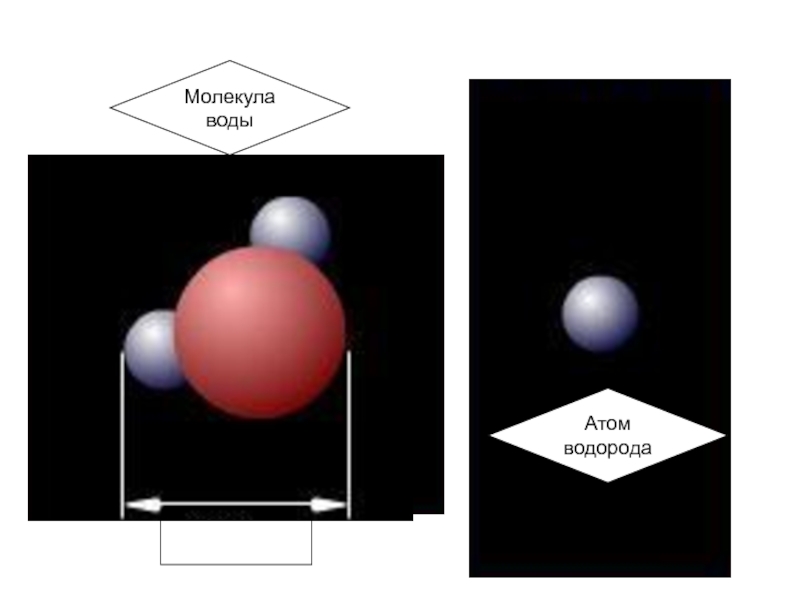
- 3. Атом водородаМолекула воды0,2 нм
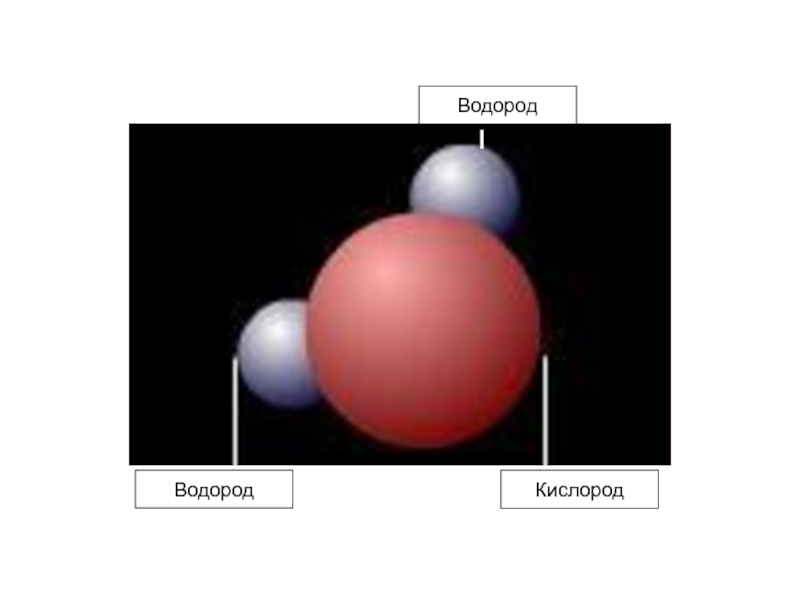
- 4. КислородВодородВодород
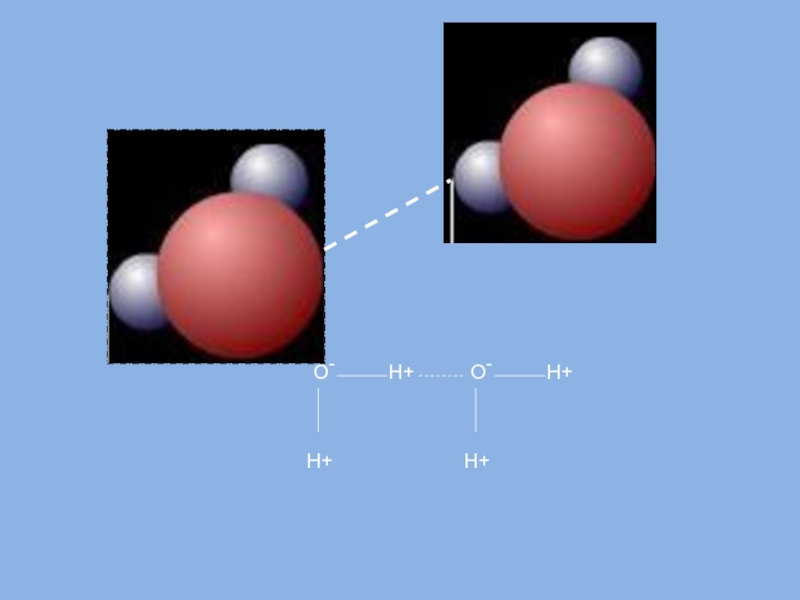
- 5. Слайд 5
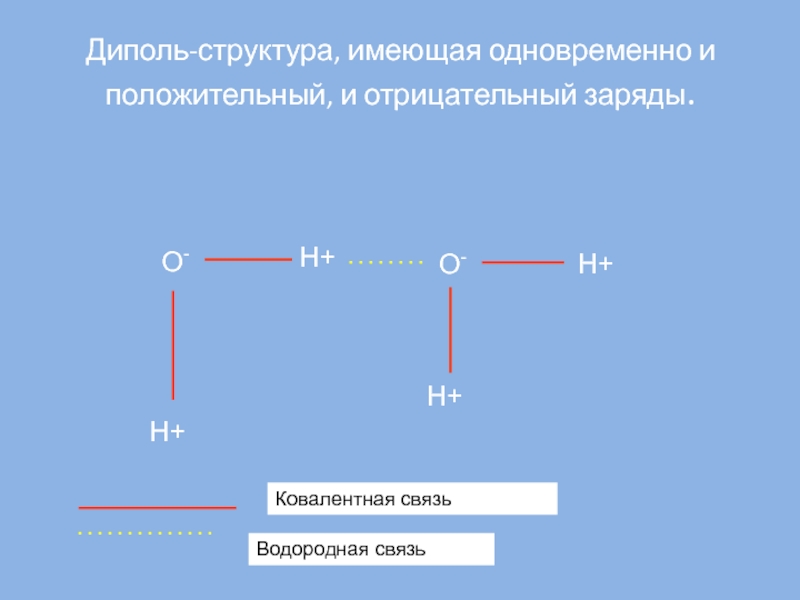
- 6. Диполь-структура, имеющая одновременно и положительный, и отрицательный заряды.Ковалентная связьВодородная связь
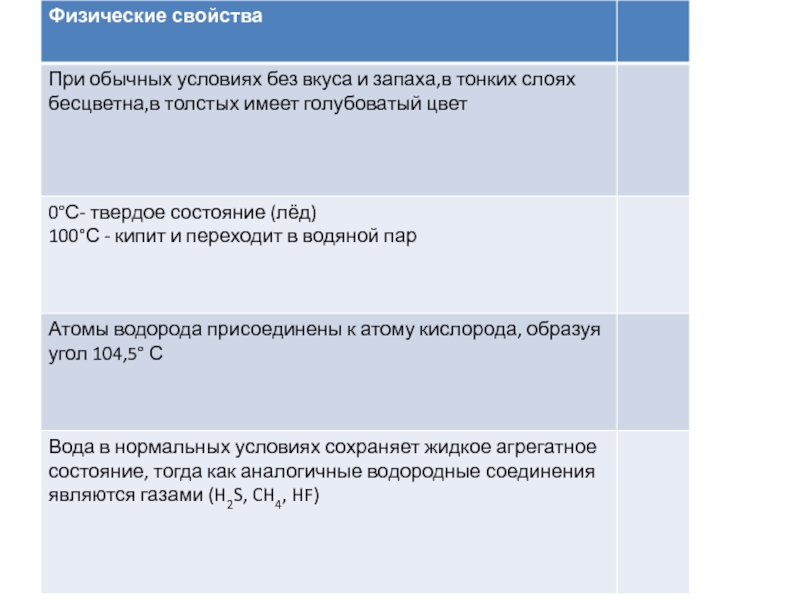
- 7. Слайд 7
- 8. Химические свойстваВода-окислитель(с щелочными и щелочно-земельными металлами)образуя щелочь
- 9. С некоторыми солями, образуя кристаллогидратыFeSO4 +7 H2O
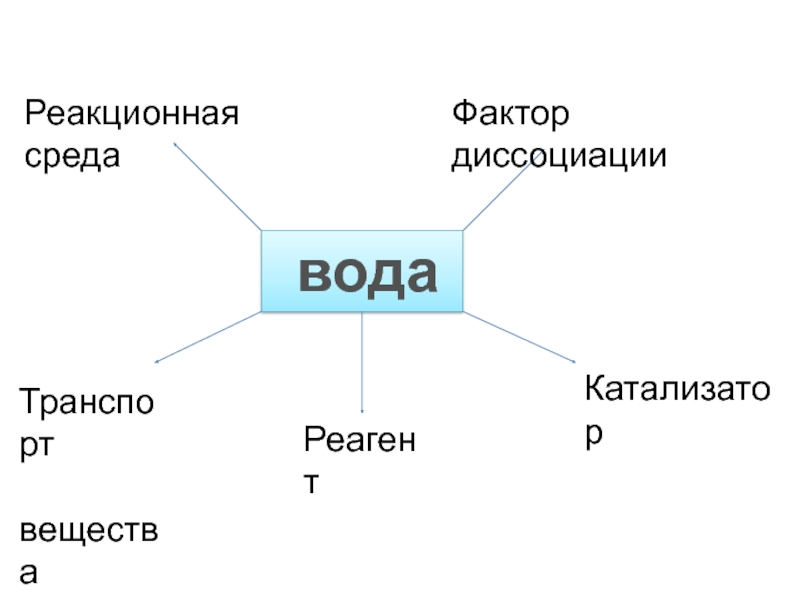
- 10. водаРеакционная средаФактор диссоциацииКатализаторРеагентТранспорт вещества
- 11. Вещества:Растворимые(в 100г воды растворяется более 1г вещества)Малорастворимые(
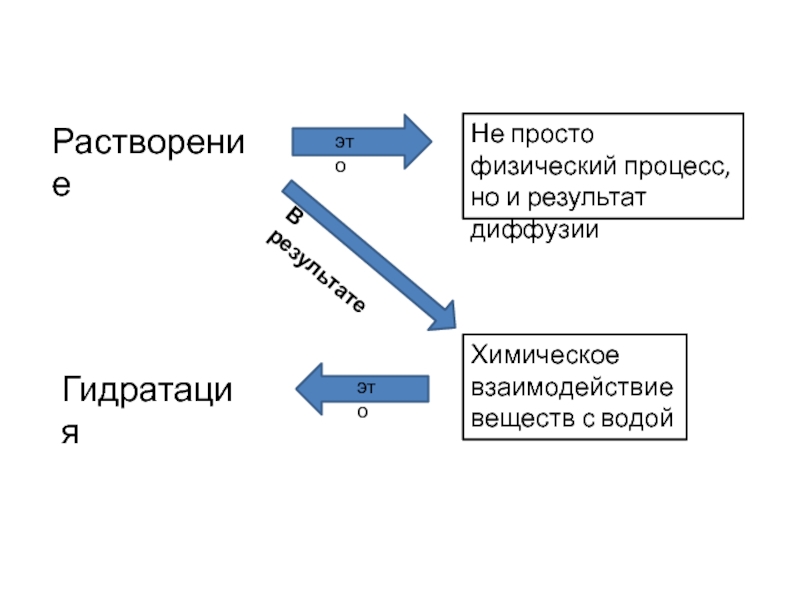
- 12. РастворениеГидратацияНе просто физический процесс, но и результат диффузииХимическое взаимодействие веществ с водойВ результатеэтоэто
- 13. Водные растворы- это гомогенные системы, состоящие из
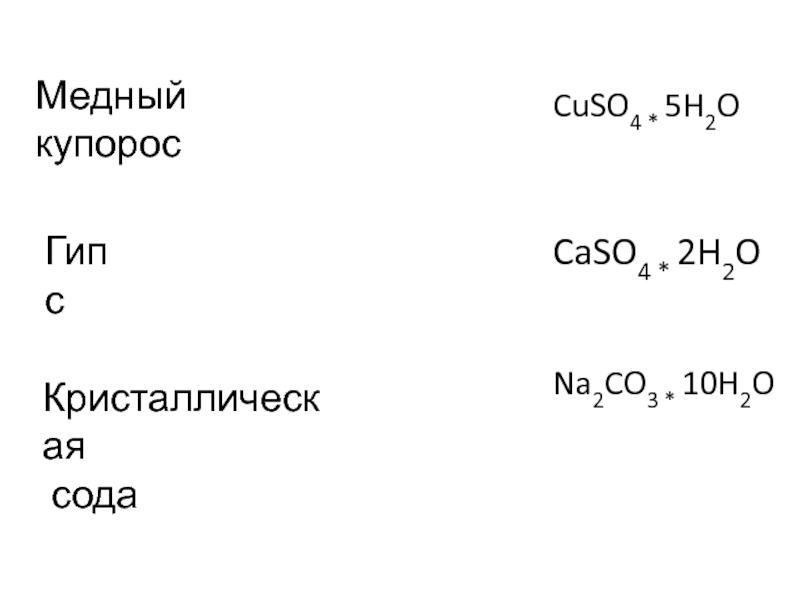
- 14. CuSO4 * 5H2OМедный купоросCaSO4 * 2H2OГипсNa2CO3 * 10H2OКристаллическая сода
- 15. Электролиты - это вещества, которые
- 16. Степень электролитической диссоциации NА
- 17. NaOH = Na+ + OH-Al2(SO4)3 = 2Al3+
- 18. Аррениус Сванте (1859–1927)Предложил (1887) всесторонне обоснованную теорию
- 19. HCl = H+ + Cl-КислотыОснованияKOH = K+
- 20. Химический состав клетки70-80%
- 21. Задание для 1 группы: Впишите недостающие слова:
- 22. Задание для 2 группы: Покажите выигрышный путь, состоящий
- 23. в) являются сильными электролитами
- 24. Задание для 3 группы:Соотнесите: 1.А) Электролиты
Слайд 6Диполь-структура, имеющая одновременно и положительный, и отрицательный заряды.
Ковалентная связь
Водородная связь
Слайд 8Химические свойства
Вода-окислитель(с щелочными и щелочно-земельными металлами)образуя щелочь и водород
2Na0
Вода-восстановитель( с сильным окислителем)
4F0 +2H2O = 4HF +O20
Вода горит во фторе голубым пламенем
Разложение воды(заметно при 2000° С)
2H2O = 2H20 +O20
Реакции соединения с оксидами активных металлов,образуя растворимые основания
2Li2O +2 H2O =4LiOH
С кислотными оксидами соответствующие кислоты
P2O5 +3 H2O =t 2 H3PO4
Слайд 9С некоторыми солями, образуя кристаллогидраты
FeSO4 +7 H2O = FeSO4 * 7
Кислотно-основные свойства
Не в значительной степени, но диссоциирует т.е. вода-очень слабый амфотерный электролит
H2O = H+ + OH-
Слайд 11Вещества:
Растворимые(в 100г воды растворяется более 1г вещества)
Малорастворимые( в 100г воды- от
Практически нерастворимые
В 100г воды растворяется менее 0,01г вещества
Слайд 12Растворение
Гидратация
Не просто физический процесс, но и результат диффузии
Химическое взаимодействие веществ с
В результате
это
это
Слайд 13Водные растворы- это гомогенные системы, состоящие из молекул воды, частиц растворенного
Гидратированные молекулы- это молекулы, окруженные оболочкой из молекул воды.
Гидратация- взаимодействие воды с молекулами растворяемого вещества.
Слайд 15Электролиты - это вещества, которые в
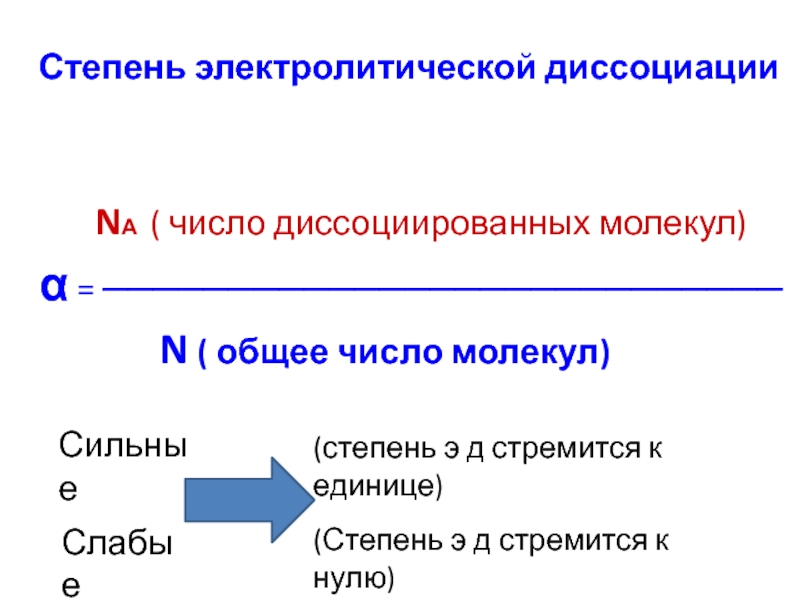
Степень электролитической диссоциации- это отношение молей вещества, распавшегося на ионы, к общему количеству растворенного вещества.
Слайд 16Степень электролитической диссоциации
NА ( число диссоциированных молекул)
α
N ( общее число молекул)
Сильные
(степень э д стремится к единице)
Слабые
(Степень э д стремится к нулю)
Слайд 17NaOH = Na+ + OH-
Al2(SO4)3 = 2Al3+ + 3SO42-
Сильные электролиты
Щелочи, все
Слабые электролиты
Многие неорганические и почти все органические кислоты
HNO2 H+ + NO2-
CH3COOH CH3COO- + H+
Слайд 18Аррениус Сванте (1859–1927)
Предложил (1887) всесторонне обоснованную теорию электролитической диссоциации, согласно которой
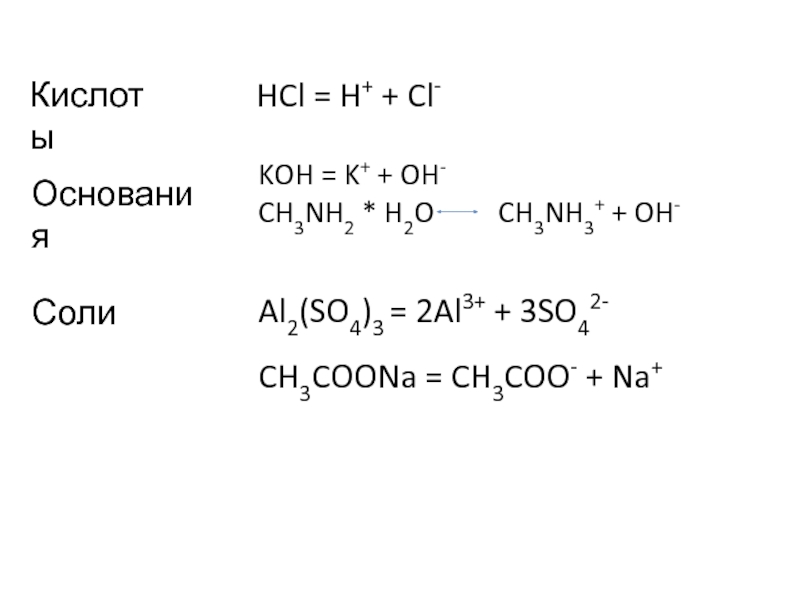
Слайд 19HCl = H+ + Cl-
Кислоты
Основания
KOH = K+ + OH-
CH3NH2 * H2O
Соли
Al2(SO4)3 = 2Al3+ + 3SO42-
CH3COONa = CH3COO- + Na+
Слайд 21Задание для 1 группы:
Впишите недостающие слова:
Все вещества по их
Процесс распада электролита на ионы называется __________________ ______________.
В растворах электролиты диссоциируют на _______________ и ______________ ионы.
По степени электролитической диссоциации электролиты делятся на _________ и _______.
2) Все соли – электролиты, CuSO4 – ___________.
Все растворимые основания – сильные электролиты,
NaOH – ___________________.
электролиты
неэлектролиты
электролитической диссоциацией
положительные
отрицательные
сильные
слабые
электролит
сильный электролит
Слайд 22Задание для 2 группы:
Покажите выигрышный путь, состоящий из названий веществ или
а) проводят электрический ток
б) не проводят электрический ток
Слайд 24Задание для 3 группы:
Соотнесите:
1.
А) Электролиты
Б) Неэлектролиты 2) Оксиды
3) Простые вещества
4) Соли
5) Основания
2.
А) Сильные электролиты 1) Азотная кислот
Б) Слабые электролиты 2) Вода
3) Гидроксид натрия
4) Соляная кислота
5) Гидроксид алюминия
3.
Электролиты: Ионы в растворе электролита:
А) NaCl
Б) KOH
В) HNO3
1) OH¯ 4) K
2) H 5) NO3¯
+
+
3) Na 6)Cl
+
–