- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему: Железо
Содержание
- 1. Презентация по химии на тему: Железо
- 2. Железо-никелевые метеориты
- 3. 4,65%распространённость железа в земной кореЖелезо составляет большую часть земного ядра.
- 4. Слайд 4
- 5. Слайд 5
- 6. Железо — это простое вещество, металл, серебристо-белого
- 7. Слайд 7
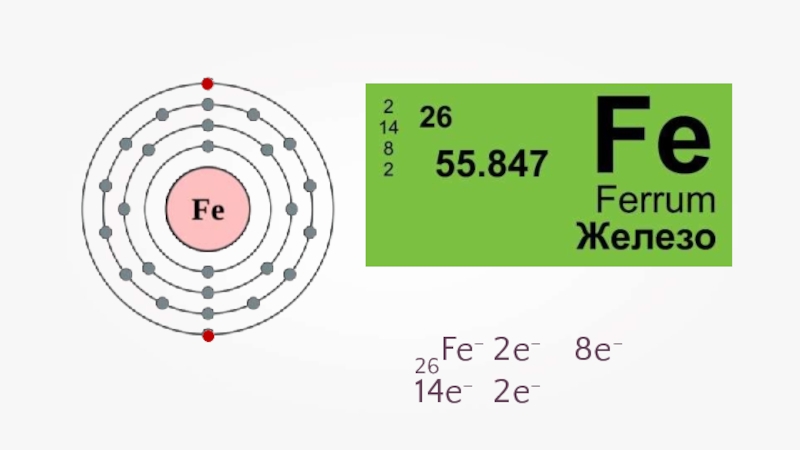
- 8. 26Fe– 2e– 8e– 14e– 2e–
- 9. Опты №13Fe + 2O2 = Fe3O4 + Q
- 10. При взаимодействии железа с галогенами (кроме йода) оно образует галогениды.2Fe + 3Cl2 = 2FeCl3
- 11. При нагревании смеси железных опилок и порошка серы образуется сульфид железа (II).Fe + S = FeS
- 12. Li, K, Ba, Ca, Na, Mg, Al,
- 13. Железо восстанавливает из водных растворов солей металлы,
- 14. При восстановлении железом еще менее активных металлов,
- 15. Свойства оксидовОксид железа(II) FeO обладает основными свойствами,
- 16. Свойства оксидовГидроксид железа(III) Fe(OH)3 проявляет слабо амфотерные
- 17. Раствор FeCl2Раствор NaOHОсадокбез допуска воздухаОпыт №2Осадокс частичным окислениемОкисление гидроксида железа4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
- 18. ЖелезоAlchemist-hp
- 19. Железо в промышленностиКрасный железнякКрасный железнякNorbert Kaiser
- 20. По запасу железных руд Россия занимает первое место в мире. Они залегают на Урале,в Курской области.
- 21. Слайд 21
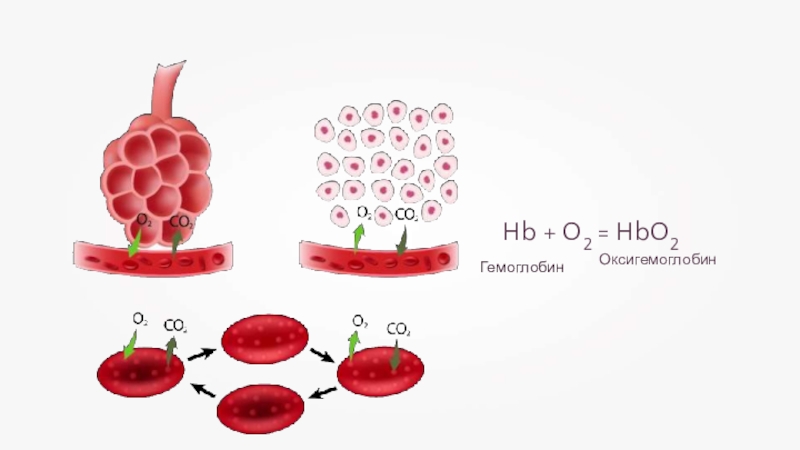
- 22. Hb + O2 = HbO2Гемоглобин Оксигемоглобин
- 23. Слайд 23
- 24. ЧугуныСталиЖелезо
- 25. Железные сплавыЧугунСталь
- 26. В чугуне содержится углерода больше, чем железо
- 27. Особенность чугуна: при затвердевании он не сжимается,
- 28. Решётка Летнего Сада
- 29. Сталь
- 30. Свойства стали в закаленном состоянии зависят от
- 31. Слайд 31
- 32. Легированная сталь
- 33. Слайд 33
- 34. Быстрорежущая сталь
- 35. Нержавеющая сталь
- 36. Нержавеющие стали широко применяют в химической, машиностроительной,
- 37. Арки станции метро «Маяковская» московского метрополитенаEugeny1988
- 38. Содержание железау взрослого человека: 2–5 г.Содержание железау взрослого человека: 300–400 мг.
- 39. Слайд 39
- 40. Hb + O2 = HbO2Гемоглобин Оксигемоглобин
- 41. Железо выполняет множество важнейших функций, основная из которых — поддержание постоянного уровня гемоглобина в крови.
- 42. Анемия
- 43. Слайд 43
- 44. Слайд 44
- 45. Слайд 45
Слайд 6Железо — это простое вещество, металл, серебристо-белого цвета; его плотность 7,87
Обладает хорошей пластичностью, легко куётся и прокатывается в тонкие листы или проволоку.
Alchemist-hp
Слайд 10При взаимодействии железа с галогенами (кроме йода) оно образует галогениды.
2Fe +
Слайд 11При нагревании смеси железных опилок и порошка серы образуется сульфид железа
Fe + S = FeS
Слайд 12Li, K, Ba, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe,
Железо растворяется в разбавленной серной и соляной кислотах, вытесняя из них водород и образуя соответствующую соль.
Fe + 2HCl = FeCl2 + H2↑
Слайд 13Железо восстанавливает из водных растворов солей металлы, расположенные правее в электрохимическом
Fe + CuSO4(р-р) = FeSO4(р-р) + Cu
+2 +2
0 0
2e–
Слайд 14При восстановлении железом еще менее активных металлов, например, серебра из соли
3AgNO3 + Fe = Fe(NO3)3 + 3Ag
+1 0 +3 0
Слайд 15Свойства оксидов
Оксид железа(II) FeO обладает основными свойствами, ему отвечает основание Fe(OH)2.
2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 6H2O
Слайд 16Свойства оксидов
Гидроксид железа(III) Fe(OH)3 проявляет слабо амфотерные свойства, он способен реагировать
Fe(OH)3 + 3КОН → K3[Fe(OH)6]
Слайд 17Раствор FeCl2
Раствор NaOH
Осадок
без допуска воздуха
Опыт №2
Осадок
с частичным окислением
Окисление гидроксида железа
4Fe(OH)2 +
Слайд 20По запасу железных руд Россия занимает первое место в мире. Они
в Курской области.
Слайд 26В чугуне содержится углерода больше, чем железо может удержать его при
в виде пластинчатых кристаллов
графита.
Слайд 27Особенность чугуна: при затвердевании он не сжимается, как большинство металлов, а
Поэтому чугун можно использовать для изготовления деталей сложной конфигурации литьем.