- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Углеводы в нашей жизни
Содержание
- 1. Презентация по химии на тему Углеводы в нашей жизни
- 2. Цель: Качественное обнаружение различных углеводов (поли-, олиго, моносахаридов) в продуктах питания
- 3. Оборудование:ПробиркиСпиртовкаСтупка с пестикомСтеклянные палочкиХимические стаканыПредметные стёкла
- 4. Реактивы:Гидроксид натрия Сульфат меди (II)Соляная кислотаРаствор люголяР-р Сегнетовой солиСпирт этиловыйРезорцинБиосенсор (АН)Нитрат серебраВодный раствор аммиака
- 5. Исследуемые лекарственные препараты:ФруктозаВалидол с глюкозойНовопасситАскорбиновая кислота с глюкозойГлюкоза
- 6. Реакция Троммера
- 7. Ход работы: В пробирку наливают 1-2
- 8. Реакция с фелинговой жидкостью
- 9. Приготовление Фелинговой жидкости:
- 10. Ход работы: К 1-2 мл раствора
- 11. Реакция серебряного зеркалаРеакция серебряного зеркала – это
- 12. Ход работы:К 1-2 мл глюкозы добавили раствор
- 13. Реакция серебряного зеркала на определение альдегидной группы в составе глюкозы
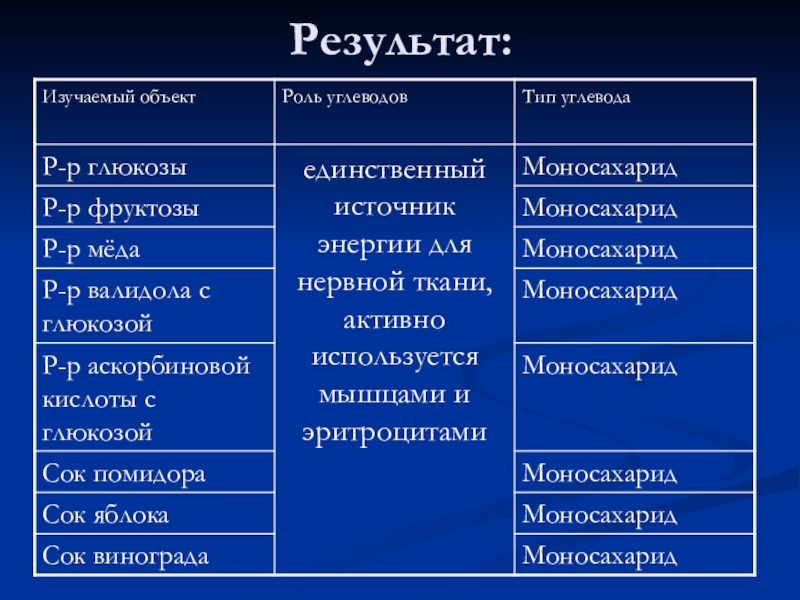
- 14. Продукты исследуемые на наличие моносахаридов:Р-р глюкозыР-р фруктозыР-р
- 15. Результат:
- 16. Реакция Селиванова на кетозы При
- 17. Ход работы: В две пробирки наливают
- 18. Результат:За это время в пробирке с фруктозой
- 19. Результат:
- 20. Реакция крахмала с раствором Люголя К
- 21. КрахмалСтроение молекул амилозы (А)
- 22. Ход работы:В пробирку наливают 2-3 мл исследуемой
- 23. Продукты исследуемые на наличие полисахарида(крахмала):Манная крупаГречневая крупаРисовая крупаПшенная крупаКукурузная крупаЙогурт «нежный»Питьевой йогурт Biomax
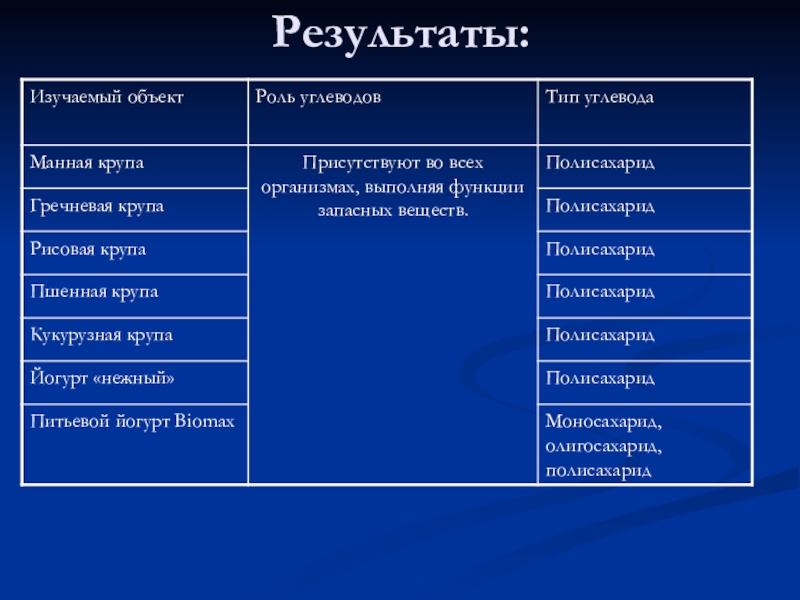
- 24. Результаты:
- 25. Определение глюкозы с помощью индикаторных полосок
- 26. Фото растворов с индикаторными полосками:
- 27. Выводы: Проделав все опыты, мы качественно
- 28. Спасибо за внимание!
Цель: Качественное обнаружение различных углеводов (поли-, олиго, моносахаридов) в продуктах питания
Слайд 2Цель:
Качественное обнаружение различных углеводов
(поли-, олиго, моносахаридов) в продуктах
питания
Слайд 3Оборудование:
Пробирки
Спиртовка
Ступка с пестиком
Стеклянные палочки
Химические стаканы
Предметные стёкла
Слайд 4Реактивы:
Гидроксид натрия
Сульфат меди (II)
Соляная кислота
Раствор люголя
Р-р Сегнетовой соли
Спирт этиловый
Резорцин
Биосенсор (АН)
Нитрат
серебра
Водный раствор аммиака
Водный раствор аммиака
Слайд 5Исследуемые лекарственные препараты:
Фруктоза
Валидол с глюкозой
Новопассит
Аскорбиновая кислота с глюкозой
Глюкоза
Слайд 6Реакция Троммера
Моносахариды и восстанавливающие олигосахариды в щелочной
среде при нагревании восстанавливают гидроксид меди (II) до оксида меди (I), окисляясь при этом до альдоновых кислот.
Слайд 7Ход работы:
В пробирку наливают 1-2 мл раствора глюкозы и
равный объем 10%-ного раствора гидроксида натрия. К смеси прибавляют при встряхивании по каплям 5%-ный раствор сульфата меди(II) до появления неисчезающей мути. Осторожно нагревают верхнюю часть содержимого пробирки. Появляется желтое окрашивание (гидроксид меди(I)), переходящее в оранжево-красное (оксид меди (I)), что указывает на положительную реакцию Троммера (моносахариды и (или) восстанавливающие олигосахариды присутствуют).
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
O O
CH2 – (CHOH)4 – C + 2Cu(OH)2 = CH2 – (CHOH)4 – C +2CuOH + H2O
H OH желтый
2CuOH = Cu2O + H2O
красный
Слайд 8
Реакция с фелинговой жидкостью
Фелингова жидкость содержит ион меди (2+)
в виде комплекного соединения с тартратами. Механизм реакции редуцирующих углеводов с фелинговой жидкостью такой же, как и реакции Троммера. Преимуществом фелинговой жидкости является то, что медь при избытке реактива не выпадает в виде оксида меди (II).
Слайд 9Приготовление Фелинговой жидкости:
Готовят два раствора:
34,6 г медного мупороса
в 500 мл раствора;
173 г сегнетовой соли и 70 г гидроксида натрия в 500 мл раствора.
Растворы хранят раздельно. Перед употреблением смешивают равные объемы первого и второго раствора.
173 г сегнетовой соли и 70 г гидроксида натрия в 500 мл раствора.
Растворы хранят раздельно. Перед употреблением смешивают равные объемы первого и второго раствора.
Слайд 10Ход работы:
К 1-2 мл раствора глюкозы приливают равный объем
фелинговой жидкости и смесь нагревают до начинающегося кипения. Образуется красный осадок оксида меди(I).
Слайд 11Реакция серебряного зеркала
Реакция серебряного зеркала – это реакция восстановления серебра из
аммиачного раствора оксида серебра. В водном растворе аммиака оксид серебра растворяется с образованием комплексного соединения – гидроксид диамминсеребра (I).
Ag2O + 4NH4OH = 2 [Ag(NH3)2]OH + H2O
При добавлении к которому альдегида происходит окислительно – восстановительная реакция с образованием металлического серебра
Ag2O + 4NH4OH = 2 [Ag(NH3)2]OH + H2O
При добавлении к которому альдегида происходит окислительно – восстановительная реакция с образованием металлического серебра
Слайд 12Ход работы:
К 1-2 мл глюкозы добавили раствор нитрата серебра (I) до
образования осадка и водный раствор аммиака до его полного растворения, нагрели. На стенках пробирки увидели отложение серебра в виде зеркала.
O
CH2 – (CHOH)4 - C + 2 [Ag(NH3)2]OH t 2Ag + CH2 – (CHOH)4 –COONH4 +3NH3+ H2O
H
O
CH2 – (CHOH)4 - C + 2 [Ag(NH3)2]OH t 2Ag + CH2 – (CHOH)4 –COONH4 +3NH3+ H2O
H
Слайд 14Продукты исследуемые на наличие моносахаридов:
Р-р глюкозы
Р-р фруктозы
Р-р сахарозы
Р-р мёда
Р-р валидола с
глюкозой
Р-р аскорбиновой кислоты с глюкозой
Сок помидора
Сок яблока
Сок винограда
Р-р аскорбиновой кислоты с глюкозой
Сок помидора
Сок яблока
Сок винограда
Слайд 16Реакция Селиванова на кетозы
При нагревании фруктозы (и
других кетогексоз) с соляной кислотой образуется оксиметилфурфурол, который с резорцином образует соединение, окрашенное в вишнево-красный цвет.
Слайд 17Ход работы:
В две пробирки наливают по 3 мл реактива
Селиванова (0,05 г резорцина растворяют в 100 мл разбавленной (1:1) соляной кислоты), в одну из них добавляют 3 капли раствора фруктозы, в другую - 3 капли раствора мёда. Обе пробирки помещают в водяную баню, нагретую до 80ºС, и держат в ней 8 минут.
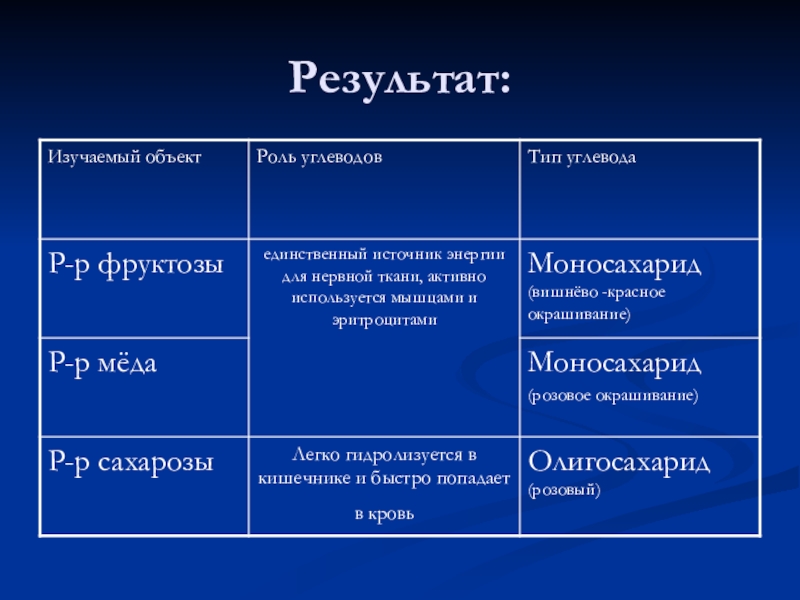
Слайд 18Результат:
За это время в пробирке с фруктозой появилось вишнёво -красное окрашивание
А
в пробирке в р-ром мёда розовое. Мёд содержит глюкозу и фруктозу в отношении (1:1)
Слайд 20Реакция крахмала с раствором Люголя
К 2-3 мл раствора крахмала прибавляют 1-2
капли раствора Люголя. Раствор окрашивается в синий цвет. Содержимое пробирки делят на три части: к первой прибавляют 1-2 мл 10%-ного раствора гидроксида натрия, ко второй — 2 мл этилового спирта; третью часть нагревают. Во всех случаях окраска исчезает, причем в третьей пробе окраска вновь появляется при охлаждении. Это связанно с тем, что в холодном растворе молекулы йода встраиваются внутрь закрученной спирали молекулы амилозы – получается синее окрашивание, при нагревании молекулы амилозы раскручивается – окрашивание исчезает.
Реакция основана на образовании нестойкого адсорбционного соединения йода с амилозой.
Реакция основана на образовании нестойкого адсорбционного соединения йода с амилозой.
Слайд 21Крахмал
Строение молекул амилозы (А) и амилопектина (Б)
Амилоза
(А) дает с йодом характерную синюю окраску
Амилопектин (Б) дает с йодом характерную красно-фиолетовую окраску
Амилопектин (Б) дает с йодом характерную красно-фиолетовую окраску
Слайд 22Ход работы:
В пробирку наливают 2-3 мл исследуемой пробы, добавляют 1-2 капли
раствора Люголя, перемешивают, появляется фиолетовое окрашивание. Которое при нагревании исчезает, а при охлаждении появляется.
Слайд 23Продукты исследуемые на наличие полисахарида(крахмала):
Манная крупа
Гречневая крупа
Рисовая крупа
Пшенная крупа
Кукурузная крупа
Йогурт «нежный»
Питьевой
йогурт
Biomax
Biomax
Слайд 25Определение глюкозы с помощью индикаторных полосок
Индикаторные полоски опускали
в раствор и наблюдали изменение цвета сенсорной зоны согласно шкале на пенале. Полоски показали, что продукты содержат глюкозу. Цвет полоски стал зелёным, что соответствует шкале больше или равно 112 ммоль/л.
Этот опыт подтверждает реакцию Троммера и с Фелинговой жидкостью, но является более диагностичным.
Этот опыт подтверждает реакцию Троммера и с Фелинговой жидкостью, но является более диагностичным.
Слайд 27Выводы:
Проделав все опыты, мы качественно обнаружили моносахариды в следующих
растворах: глюкозы, фруктозы, мёда, валидола с глюкозой, а также в натуральных соках: помидора, яблока и винограда. Олигосахариды (сахароза) в растворе сахара. Полисахариды (крахмал) в таких продуктах: манной, гречневой, рисовой, пшенной, кукурузной крупах, в йогурте «нежный» и питьевом йогурте Biomax.