- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Строение атома (8 класс)
Содержание
- 1. Презентация по химии на тему Строение атома (8 класс)
- 2. Основные сведения о строении атомов
- 3. Историческая справка Понятие атом возникло еще в
- 4. Но не только электроны входят в
- 5. Ядро имеет сложное строение оно состоит из
- 6. Так как атом электронейтрален – число протонов
- 7. Атомный (порядковый номер) == Заряд ядра атома= Число протонов в ядре= Число электронов в атоме
- 8. Определение Атом – это электронейтральная, химически неделимая
- 9. Химический элемент – это вид атомов с одинаковым зарядом ядраОпределение
- 10. Задание № 1 Определить число протонов
- 11. Домашнее задание§ 4, вопросы 1-3 упр.6-8
- 12. Какая частица самая главная в атоме?Заряд ядра
- 13. Слайд 13
- 14. K - 1. Z = 19,
- 15. Атом не существуетЗаряд ядра
- 16. ВыводЕсли менять количество нейтронов в ядре, то
- 17. Химический элемент – это совокупность атомов с одинаковым зарядом ядра
- 18. Задание № 2 Поиграйте в «крестики -
- 19. т.к. в ядре атома 8 протонов, порядковый номер элемента – 8. Правильный ответ:кислород
Слайд 3Историческая справка
Понятие атом возникло еще в античном мире для обозначения
Так считали ученые вплоть до конца XIX века, когда было доказано, что атом делим, что он состоит из более мелких (элементарных) частиц.
Ученый Стони ввел понятие «электроны», а Томсон и Перрен изучили и охарактеризовали эти частицы.
ЭЛЕКТРОН – отрицательно заряженная частица (условный заряд -1).
Масса электрона (me) в 1876 раз меньше массы атома водорода.
Скорость движения электрона равна скорости света: 300 000 км/с
Слайд 4 Но не только электроны входят в состав атомов. Работы Беккереля,
Историческая справка
По размерам ядро в 100 000 раз меньше размеров самого атома (это как футбольный мяч, лежащий в центре поля), но именно в ядре сосредоточена вся его масса.
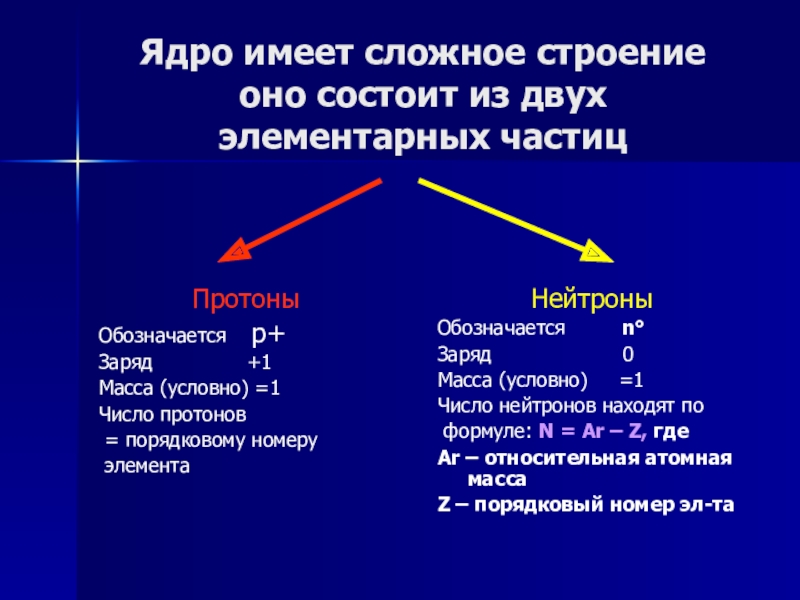
Слайд 5Ядро имеет сложное строение
оно состоит из двух элементарных частиц
Протоны
Обозначается p+
Заряд +1
Масса (условно) =1
Число протонов
= порядковому номеру
элемента
Нейтроны
Обозначается n°
Заряд 0
Масса (условно) =1
Число нейтронов находят по
формуле: N = Ar – Z, где
Ar – относительная атомная масса
Z – порядковый номер эл-та
Слайд 6Так как атом электронейтрален – число протонов и электронов в атоме
Слайд 7
Атомный (порядковый номер) =
= Заряд ядра атома
= Число протонов в ядре
=
Слайд 8Определение
Атом – это электронейтральная, химически неделимая частица, состоящая из положительно
Слайд 10Задание № 1
Определить число протонов и нейтронов для атома
P 15
30.973
фосфор
порядковый
номер
относительная
атомная масса
ответ:
протонов -
электронов -
нейтронов -
15
15
31-15=16
Слайд 12Какая частица самая главная в атоме?
Заряд ядра +1
Масса
Водород Н
Водород: Н
Заряд ядра +1
Масса атома 1
1. Попробем изменить число нейтронов в ядре
+
протий
дейтерий
+
D
Слайд 13
это две разновидности одного химического элемента – водорода. Их называют ИЗОТОПАМИ («изос» - равный, «топос» - место), т.е. им отведено одно место в периодической системе.
протий и дейтерий
Слайд 14K - 1. Z = 19, Ar = 39
Изотопы – это разновидности одного и того же химического элемента, имеющие одинаковый заряд ядра, но разную относительную атомную массу.
СI - 1. Z=17, Ar=35
2. Z=17, Ar=37
протий и дейтерий
K - 1. Z = 19, Ar = 39
2. Z = 19, Ar = 40
O - 1. Z = 8, Ar = 16
2. Z = 8, Ar = 17
3. Z = 8 Ar = 18
пример
Слайд 15Атом не существует
Заряд ядра +2
Масса
=> изотоп гелия
Водород (дейтерий)
заряд ядра +1
масса 2
2. Что произойдет с атомом,
если в ядре изменить
количество протонов?
+
+
+
+
Слайд 16Вывод
Если менять количество нейтронов в ядре, то меняется только масса атома.
Если
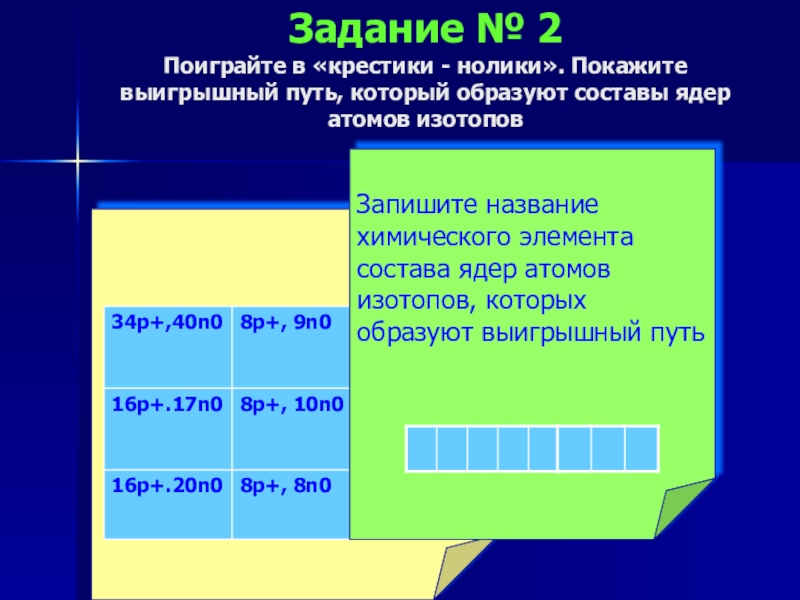
Слайд 18Задание № 2 Поиграйте в «крестики - нолики». Покажите выигрышный путь, который
Запишите название химического элемента состава ядер атомов изотопов, которых образуют выигрышный путь