- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Скорость химической реакции
Содержание
- 1. Презентация по химии на тему Скорость химической реакции
- 2. Химическая кинетикаЧто даёт знание скорости химической реакцииКлассификация
- 3. Химическая кинетика- это раздел химии, который изучает
- 4. Медленные химические процессы: коррозия, фотосинтез, биосинтез белка.Белки
- 5. Знание скорости химической реакции имеет большое практическое
- 6. Идут во всём объёме2СО(г)+ О2(г)= 2СО2(г)2HBr(г)↔H2(г) +
- 7. Средняя скорость гомогенной реакции- определяется изменением количества
- 8. Средняя скорость гетерогенной реакции- определяется изменением количества
- 9. Факторы, влияющие на скорость химической реакцииПрирода реагирующих
- 10. Природа реагирующих веществРеакционная активность веществ определяется:характером химических
- 11. КонцентрацияДля взаимодействия веществ их молекулы должны столкнуться.
- 12. Сванте Аррениус (1859-1927)Объяснение зависимости скорости реакции
- 13. Энергия активации В газе при нормальных условиях каждая
- 14. Якоб Вант-Гофф (1852-1911)Температура повышает количество столкновений
- 15. КатализаторыЙенс Якоб Берцелиусввел термин «катализ»в 1835 г.
- 16. Промоторы- вещества повышающие активность катализаторовСинтез аммиака
- 17. ДавлениеДавление сильно влияет на скорость реакций с
- 18. Площадь соприкосновенияСкорость гетерогенной реакции прямо пропорциональна площади
- 19. Задачи1. Вычислите среднюю скорость химической реакции, если
- 20. Дано:При уменьшенииобъёма смеси в 2раза концентрациякаждого веществавозрасла
- 21. Дано:c1 (А)= 1моль/лс1(В) = 3моль/лНайти: v1/v21) Запишем
- 22. 4. Как изменится скорость реакции 2Fe +
- 23. 1) Запишем выражение зависимости скорости реакции от
- 24. 6. Реакция при 50 °С протекает за
- 25. 7. Скорость реакции при охлаждении от 80°
- 26. График, отражающий зависимость скоростиреакции оксида меди (II) и соляной кислоты оттемпературы:1234ТестЗадание №11)2)3)4)
- 27. Задание №2Какой из факторов не оказываетвлияния на скорость химическойреакции в растворах:концентрация веществиспользование катализатораиспользование ингибитораобъём реакционного сосуда
- 28. На скорость химической реакции междураствором серной кислоты
- 29. Во сколько раз изменится скоростьэлементарной реакции 2А
- 30. Как повлияет на скорость элементарнойреакции А +
- 31. Быстрее при комнатной температуребудет протекать реакция между
- 32. В течение одной минуты выделится больше водорода,
- 33. При увеличении температуры от 10° до30° С
- 34. Для уменьшения скорости химическойреакции необходимо:увеличить концентрацию реагирующих веществввести в систему катализаторповысить температурупонизить температуруЗадание №9
- 35. Скорость химической реакции междумедью и азотной кислотой зависит от:массы медиобъёма кислотыконцентрации кислотыобъёма колбыЗадание №10
- 36. http://www.hemi.nsu.ru/ucheb214.htmhttp://www.chem.msu.su/rus/teaching/Kinetics-online/welcome.htmlО.С.Габриелян. Химия. 11 класс. Базовый уровень. Учебник
Слайд 2Химическая кинетика
Что даёт знание скорости химической реакции
Классификация реакций по фазовому составу
Средняя
Скорость гетерогенной реакции
Факторы, влияющие на скорость химической реакции
Природа реагирующих веществ
Концентрация
Температура
Катализатор, ингибитор, промотор
Давление
Площадь соприкосновения
Задачи
Тест
Литература
Содержание презентации
Слайд 3Химическая кинетика
- это раздел химии, который изучает скорости химических реакций, их
Быстрые химические процессы: взрывы, ионные реакции в растворах, передача нервного импульса
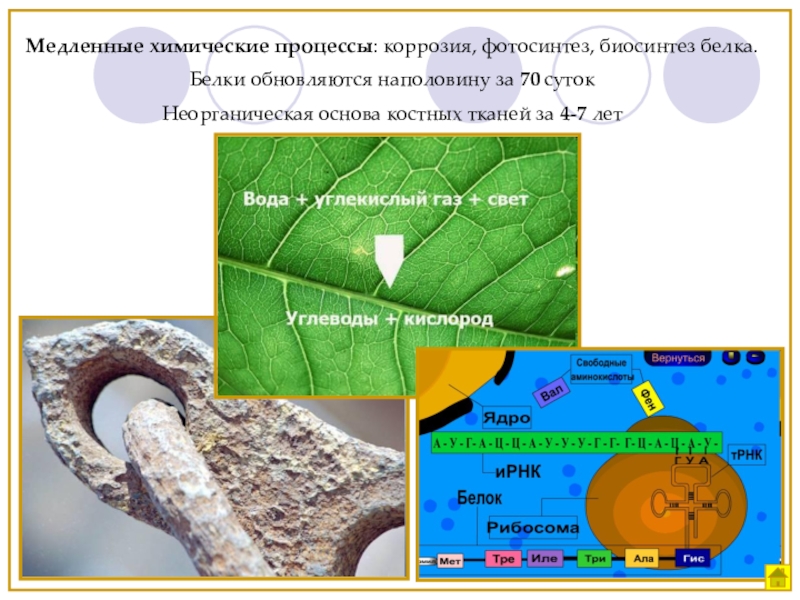
Слайд 4Медленные химические процессы: коррозия, фотосинтез, биосинтез белка.
Белки обновляются наполовину за 70
Неорганическая основа костных тканей за 4-7 лет
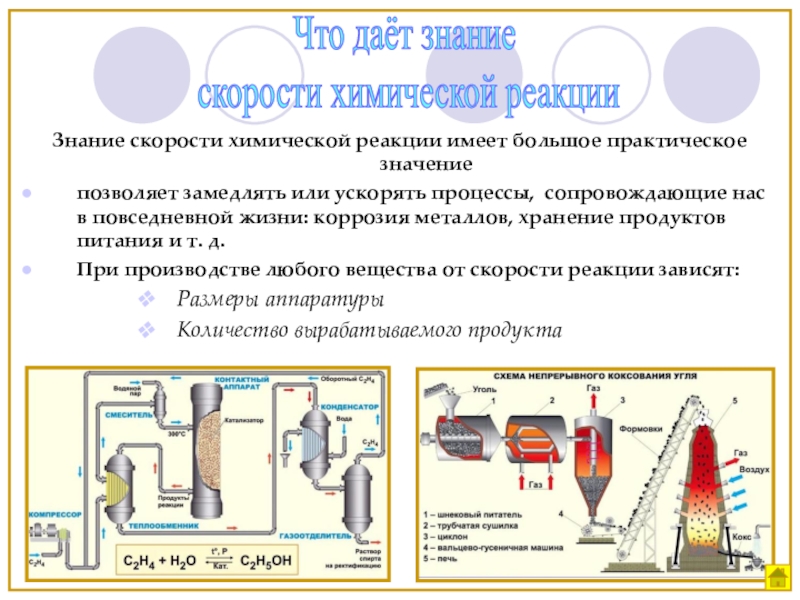
Слайд 5Знание скорости химической реакции имеет большое практическое значение
позволяет замедлять или ускорять
При производстве любого вещества от скорости реакции зависят:
Размеры аппаратуры
Количество вырабатываемого продукта
Что даёт знание
скорости химической реакции
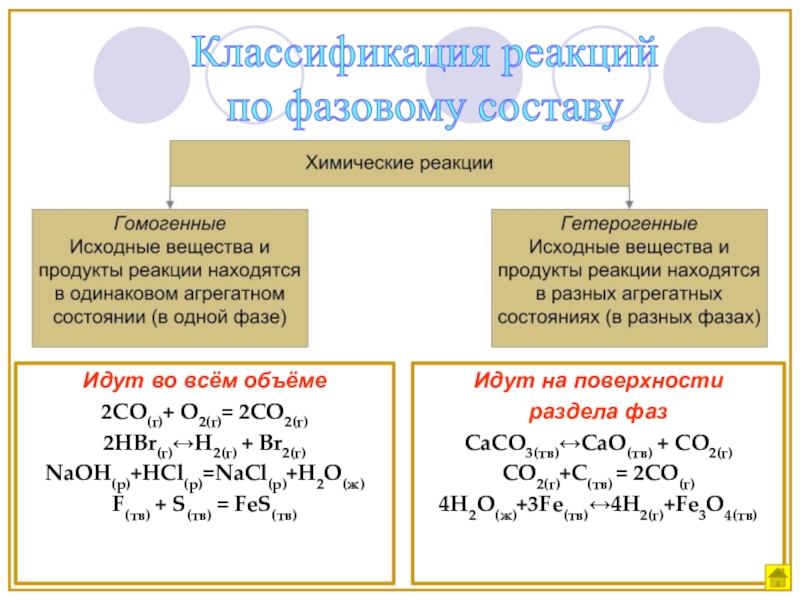
Слайд 6Идут во всём объёме
2СО(г)+ О2(г)= 2СО2(г)
2HBr(г)↔H2(г) + Br2(г)
NaOH(р)+HCl(р)=NaCl(р)+H2O(ж)
F(тв) + S(тв) =
Идут на поверхности
раздела фаз
CaCO3(тв)↔CaO(тв) + CO2(г)
CO2(г)+С(тв) = 2СО(г)
4H2O(ж)+3Fe(тв)↔4H2(г)+Fe3O4(тв)
Классификация реакций
по фазовому составу
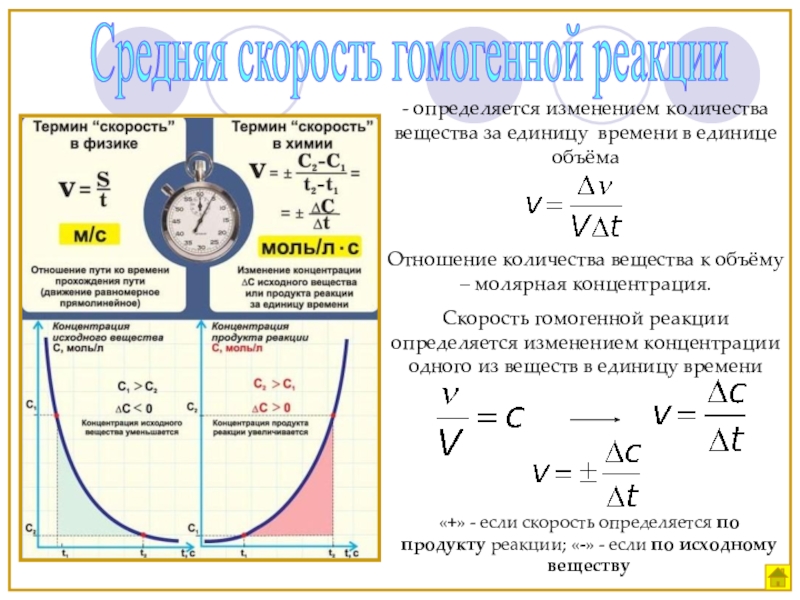
Слайд 7Средняя скорость гомогенной реакции
- определяется изменением количества вещества за единицу времени
Отношение количества вещества к объёму – молярная концентрация.
Скорость гомогенной реакции определяется изменением концентрации одного из веществ в единицу времени
«+» - если скорость определяется по продукту реакции; «-» - если по исходному веществу
Слайд 8Средняя скорость гетерогенной реакции
- определяется изменением количества вещества, вступившего в реакцию
Взаимодействие происходит только на поверхности раздела между веществами
S – площадь поверхности
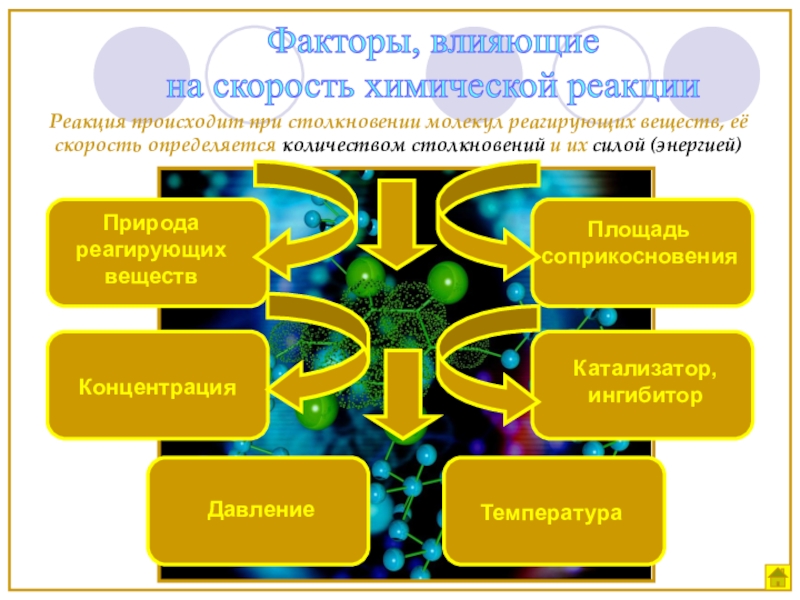
Слайд 9Факторы, влияющие
на скорость химической реакции
Природа реагирующих веществ
Концентрация
Температура
Катализатор, ингибитор
Площадь соприкосновения
Реакция происходит
Давление
Слайд 10Природа реагирующих веществ
Реакционная активность веществ определяется:
характером химических связей
скорость больше у
скорость меньше у веществ с ковалентной малополярной и неполярной связью (органические вещества)
υ(Zn + HCl = H2 + ZnCl2) > υ(Zn + CH3COOH = H2 + Zn(CH3COO)2
их строением
скорость больше у металлов, которые легче отдают электроны (с большим радиусом атома)
скорость больше у неметаллов, которые легче принимают электроны (с меньшим радиусом атома)
υ(2K + 2H2O = H2 + 2KOH) > υ(2Na + 2H2O = H2 + 2NaOH)
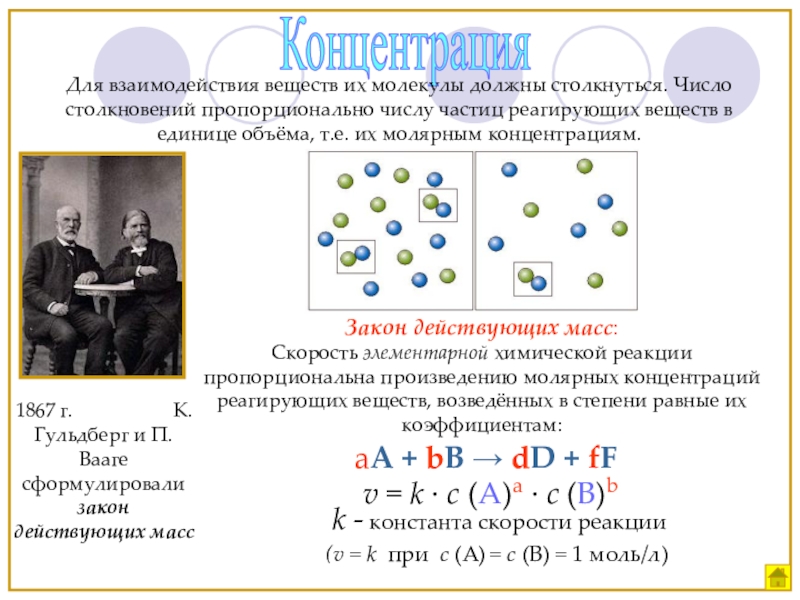
Слайд 11Концентрация
Для взаимодействия веществ их молекулы должны столкнуться. Число столкновений пропорционально числу
Закон действующих масс:
Скорость элементарной химической реакции пропорциональна произведению молярных концентраций реагирующих веществ, возведённых в степени равные их коэффициентам:
1867 г. К.Гульдберг и П.Вааге сформулировали закон действующих масс
Слайд 12Сванте Аррениус
(1859-1927)
Объяснение зависимости скорости реакции от температуры было дано
С.Аррениус рассчитал долю активных (т.е. приводящих к реакции) соударений реагирующих частиц , зависящую от температуры.
молекула - энергетически выгодное образование
химические вещества на энергетической диаграмме занимают положение в "ямках"
для превращения этих веществ в другие, им надо сообщить энергию, достаточную для того, чтобы они выбрались из "ямки", перевалили через "барьер" (энергию активации)
Температура
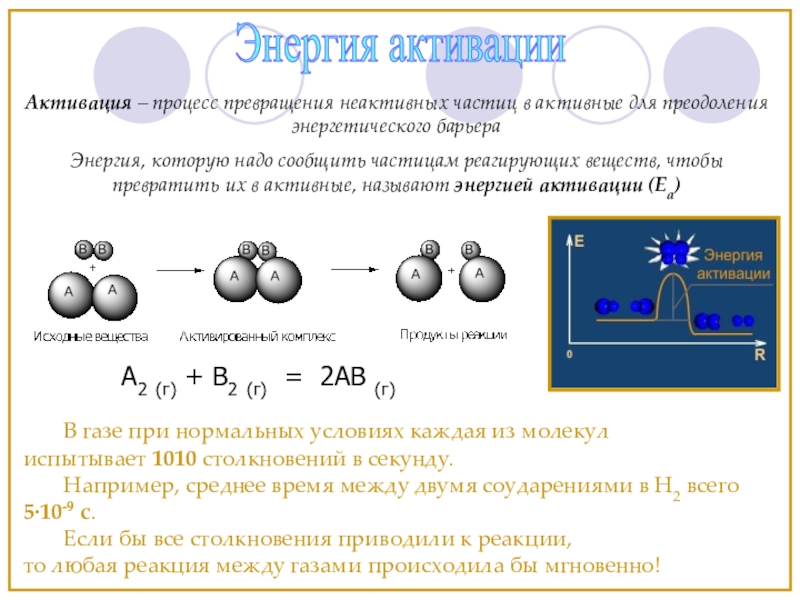
Слайд 13Энергия активации
В газе при нормальных условиях каждая из молекул
испытывает 1010
Например, среднее время между двумя соударениями в Н2 всего 5·10-9 с.
Если бы все столкновения приводили к реакции,
то любая реакция между газами происходила бы мгновенно!
A2 (г) + B2 (г) = 2AB (г)
Активация – процесс превращения неактивных частиц в активные для преодоления энергетического барьера
Энергия, которую надо сообщить частицам реагирующих веществ, чтобы превратить их в активные, называют энергией активации (Еа)
Слайд 14Якоб Вант-Гофф
(1852-1911)
Температура повышает количество столкновений молекул.
Правило Вант-Гоффа не имеет силу закона. Лабораторная техника была несовершенна, поэтому:
оказалось, что температурный коэффициент в значительном температурном интервале непостоянен
невозможно было изучать как очень быстрые реакции (протекающие за миллисекунды), так и очень медленные (для которых требуются тысячи лет)
реакции с участием больших молекул сложной формы (например, белков) не подчиняются правилу Вант-Гоффа
v = v0·∆τ/10
- температурный коэффициент Вант-Гоффа
Слайд 15Катализаторы
Йенс Якоб Берцелиус
ввел термин «катализ»
в 1835 г.
Вильгельм Оствальд
1909 г. –
«в признание работ по катализу»
вещества, изменяющие скорость химической реакции за счёт изменения энергии активации, но сами при этом не расходующиеся. Процесс в присутствии катализатора – катализ. Реакция с катализатором – каталитическая.
Положительные катализаторы – ускоряют реакцию, уменьшая Еа
Отрицательные катализаторы (ингибиторы) – замедляют реакцию, увеличивая Еа
A + K = AK (1)
AK + B = AB + K (2)
Суммарная реакция
A + B = AB
Но вместо энергетического барьера этой реакции преодолеваются более низкие барьеры реакций (1) и (2): E1 и E2
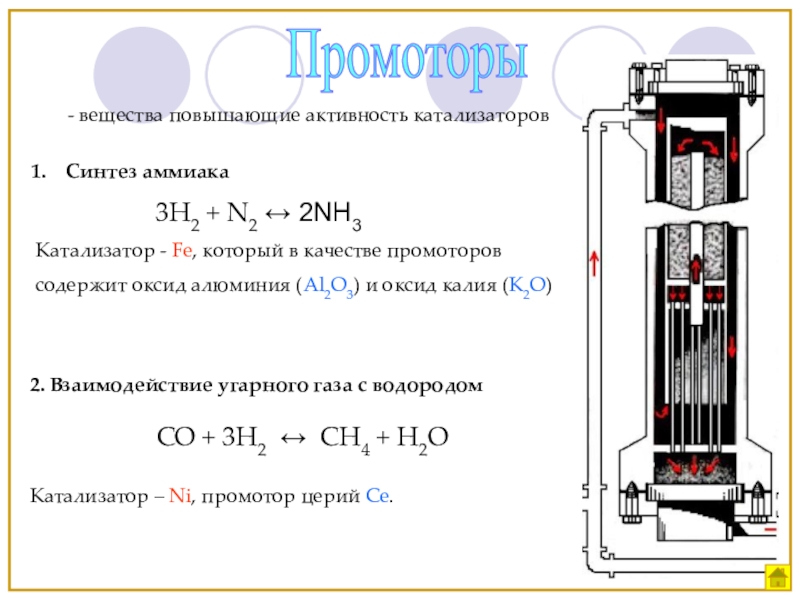
Слайд 16Промоторы
- вещества повышающие активность катализаторов
Синтез аммиака
Катализатор - Fe, который в качестве промоторов
содержит оксид алюминия (Al2O3) и оксид калия (K2O)
2. Взаимодействие угарного газа с водородом
СО + 3Н2 ↔ СН4 + Н2О
Катализатор – Ni, промотор церий Ce.
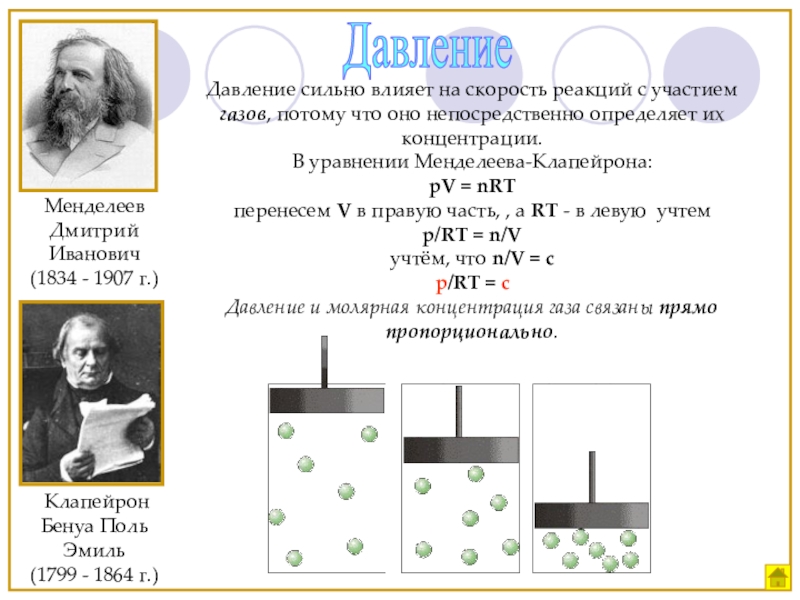
Слайд 17Давление
Давление сильно влияет на скорость реакций с участием газов, потому что
В уравнении Менделеева-Клапейрона:
pV = nRT
перенесем V в правую часть, , а RT - в левую учтем p/RT = n/V
учтём, что n/V = c
p/RT = c
Давление и молярная концентрация газа связаны прямо пропорционально.
Клапейрон Бенуа Поль Эмиль
(1799 - 1864 г.)
Менделеев Дмитрий Иванович
(1834 - 1907 г.)
Слайд 18Площадь соприкосновения
Скорость гетерогенной реакции прямо пропорциональна площади поверхности соприкосновения реагентов.
При
соприкосновения реагирующих веществ, при этом возрастает скорость реакции
Скорость гетерогенной реакции зависит от:
а) скорости подвода реагентов к границе раздела фаз;
б) скорости реакции на поверхности раздела фаз, которая зависит от площади этой поверхности;
в) скорости отвода продуктов реакции от границы раздела фаз.
Стадии (а) и (в) называются диффузионными, а стадия (б) – кинетической. Та стадия, которая протекает наиболее медленно, называется лимитирующей – именно она определяет скорость реакции в целом.
Слайд 19Задачи
1. Вычислите среднюю скорость химической реакции, если через 20 с от
Дано:
τ1 = 20c
τ2 = 40c
c1 = 0,05моль/л
с2 = 0,04моль/л
Найти: v
Расчёт ведём по исходному веществу,
значит перед формулой ставим знак «-»
υ = -∆с/∆τ
υ = -(с2-с1)/(τ2- τ1)
υ = -(0,04-0,05)/(40-20) = 0,0005 (моль/(л∙с))
Ответ: средняя скорость реакции 0,0005моль/(л∙с)
Слайд 20Дано:
При уменьшении
объёма смеси в 2
раза концентрация
каждого вещества
возрасла в 2 раза
c2 (смеси)/с1(смеси)
Найти: v2/v1
2. Как изменится скорость химической реакции 2СО + О2 = 2СО2, если уменьшить объем газовой смеси в 2 раза?
2СО + О2 = 2СО2
1) Запишем выражение закона действующих
масс для исходной смеси и после сжатия
v1 = k · c(СО)2 · c(О2)
v2 = k · c(2СО)2 · c(2О2) =
= k · 4c(СО)2 · 2c(О2) =
= 8k · c(СО)2 · c(О2)
2) Найдём отношение скоростей:
v2/v1 = (8k · c(СО)2 · c(О2))/ (k · c(СО)2 · c(О2)) = 8
Ответ: скорость реакции возрастёт в 8 раз
Слайд 21Дано:
c1 (А)= 1моль/л
с1(В) = 3моль/л
Найти: v1/v2
1) Запишем закон действующих масс для
реакции:
v = k∙с(A)∙ с(B)2
2) Найдём начальную скорость реакции:
v1 = k · c(А) · c(В)2 = k · 1 ∙ 9 = 9k
3) Найдём новые концентрации веществ:
с2(А) = 0,5 ∙ с1(А) = 0,5 ∙ 1 = 0,5(моль/л)
с2(В) = 3 – 2 ∙ с1(А) = 3 – 0,5 ∙ 1 = 2(моль/л)
4) Найдём конечную скорость реакции:
v2 = k · c2(А) · c2(В)2 = k · 0,5 ∙ 4 = 2k
5) Найдём отношение скоростей:
v1/v2 = 9k/2k = 4,5
Ответ: скорость уменьшится в 4,5 раза.
3. Во сколько раз уменьшится скорость простой реакции А + 2В = С, когда прореагирует половина вещества А, по сравнению с начальной скоростью? Начальные концентрации: 1 моль/л вещества А и 3 моль/л вещества В.
Слайд 224. Как изменится скорость реакции 2Fe + 3Cl2 = 2FeCl3, если
Дано:
Давление системы
увеличили в 5 раз
c2(Cl2)/с1(Cl2) = 5
Найти: v2/v1
2Fe + 3Cl2 = 2FeCl3
1) Запишем выражение закона действующих
масс для исходной смеси и после сжатия
(только для газов)
v1 = k · c(Cl2)3
v2 = k · c(5Cl2)3 = 125 ∙ k ∙ c(Cl2)3
2) Найдём отношение скоростей:
v2/v1 = 125 ∙ k ∙ c(Cl2)3/k · c(Cl2)3 = 125
Ответ: скорость реакции возрастёт в 125 раз
Слайд 231) Запишем выражение зависимости скорости
реакции от температуры:
υ2
2) Найдём отношение скоростей:
v2/v1 = γ∆τ/10 = 2(350-300)/10 = 25 = 32
Ответ: скорость реакции возрастёт в 32 раза
5. Во сколько раз увеличится скорость химической реакции при повышении температуры от 300° до 350 °С, если температурный коэффициент равен 2?
Дано:
τ1 = 300°С
τ2 = 350°С
γ = 2
Найти: v2/v1
Слайд 246. Реакция при 50 °С протекает за 2 мин 15 с.
Дано:
τ1 = 50°С
∆t1 = 2,25 мин
τ2 = 70°С
γ = 3
Найти: ∆t2
1) Находим, во сколько раз возрастёт скорость
реакции при повышении температуры с 50°С
до 70°С:
vτ2/vτ1 = γ∆t/10 = 3(70-50)/10 = 32 = 9 (раз)
2) Находим время, за которое закончится эта
реакция при температуре 70°С:
∆t2 = 2,25мин : 9 = 0,25мин (15с)
Ответ: реакция закончится за 15 секунд.
Слайд 257. Скорость реакции при охлаждении от 80° до 60 °С уменьшилась
Дано:
τ1 = 80°С
τ2 = 60°С
v1/v2 = 4
Найти: γ
Найдём отношение скоростей реакций:
v2/v1 = γ∆τ/10
Составим и решим уравнение:
4 = γ(80°-60°)/10
4 = γ2
γ = 2
Ответ: температурный коэффициент равен 2.
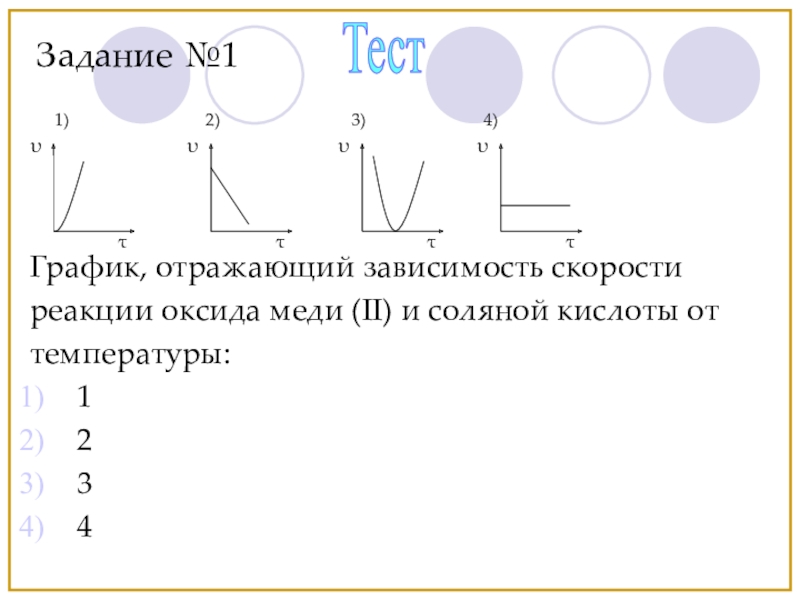
Слайд 26График, отражающий зависимость скорости
реакции оксида меди (II) и соляной кислоты от
температуры:
1
2
3
4
Тест
Задание
1)
2)
3)
4)
Слайд 27Задание №2
Какой из факторов не оказывает
влияния на скорость химической
реакции в растворах:
концентрация
использование катализатора
использование ингибитора
объём реакционного сосуда
Слайд 28На скорость химической реакции между
раствором серной кислоты и железом не
оказывает влияния:
концентрация
измельчение железа
температура реакционной смеси
увеличение давления
Задание №3
Слайд 29Во сколько раз изменится скорость
элементарной реакции 2А + В = А2В,
концентрацию вещества В уменьшить в 2
раза:
увеличится в 4 раза
уменьшится в 2 раза
уменьшится в 4 раза
увеличится в 2 раза
Задание №4
Слайд 30Как повлияет на скорость элементарной
реакции А + В = АВ увеличение
концентрации
скорость увеличится в 3 раза
скорость уменьшится в 9 раз
скорость уменьшится в 3 раза
скорость не изменится
Задание №5
Слайд 31Быстрее при комнатной температуре
будет протекать реакция между 10%
раствором соляной кислоты и:
цинком
большим куском цинка
цинком, покрытым медью
цинком в порошке
Задание №6
Слайд 32В течение одной минуты выделится
больше водорода, если для реакции
использовать:
Zn(гранулы)
Zn(порошок) и HCl(10% раствор)
Zn(гранулы) и HCl(10% раствор)
Zn(порошок) и CH3COOH(10% раствор)
Задание №7
Слайд 33При увеличении температуры от 10° до
30° С скорость реакции, температурный
коэффициент которой
возрастёт в 3 раза
возрастёт в 9 раз
уменьшится в 3 раза
уменьшится в 9 раз
Задание №8
Слайд 34Для уменьшения скорости химической
реакции необходимо:
увеличить концентрацию реагирующих веществ
ввести в систему катализатор
повысить
понизить температуру
Задание №9
Слайд 35Скорость химической реакции между
медью и азотной кислотой зависит от:
массы меди
объёма кислоты
концентрации
объёма колбы
Задание №10
Слайд 36http://www.hemi.nsu.ru/ucheb214.htm
http://www.chem.msu.su/rus/teaching/Kinetics-online/welcome.html
О.С.Габриелян. Химия. 11 класс. Базовый уровень. Учебник для общеобразовательных учебных заведений,
И.И.Новошинский, Н.С.Новошинская. Химия. 10 класс. Учебник для общеобразовательных учреждений, М., «ОНИКС 21 век»; «Мир и Образование», 2004
О.С.Габриелян, Г.Г.Лысова, А.Г.Введенская. Настольная книга учителя химии. 11 класс. М., Дрофа. 2004
К.К.Курмашева. Химия в таблицах и схемах. М., «Лист Нью». 2003
Н.Б.Ковалевская. Химия в таблицах и схемах. М., «Издат-школа 2000». 1998
П.А.Оржековский, Н.Н.Богданова, Е.Ю.Васюкова.Химия. Сборник заданий. М.»Эксмо», 2011
Фотографии: http://www.google.ru/
Литература: