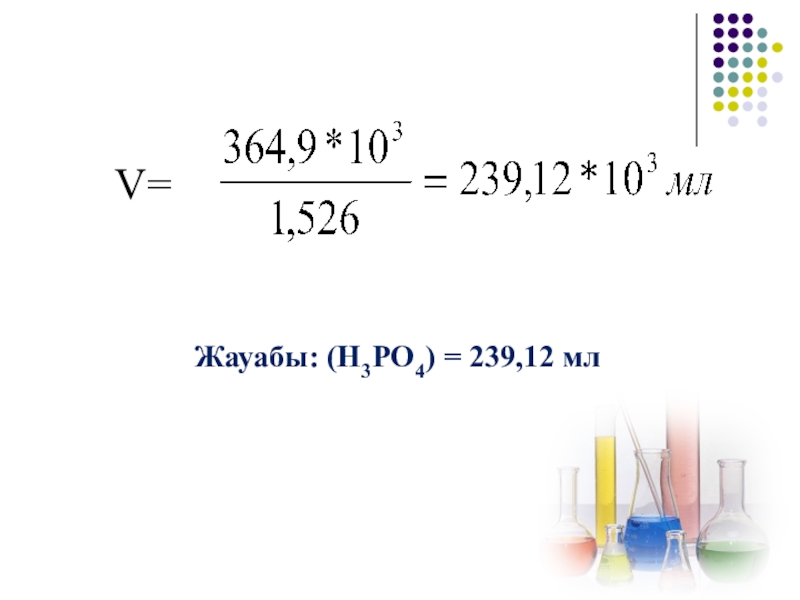- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему Химиялық теңдеулер (8 класс)
Содержание
- 1. Презентация по химии на тему Химиялық теңдеулер (8 класс)
- 2. білімділік: оқушыларға сандық есептер шығару әдісін түсіндіріп,
- 3. Химиялық теңдеулер дегеніміз – химиялық реакцияны формулалар
- 4. Химиялық теңдеулер бойынша есептеулер 1.Эквиваленттік мөлшерде
- 5. Химиялық реакция теңдеуін қолдана отырып сандық есептерді
- 6. Химиялық теңдеулер бойынша жүргізілетін есептеулердің мүмкін болатын
- 7. Алгоритм 2. Реакцияға қатысушы заттардың біреуінің массасы
- 8. Слайд 8
- 9. Берілгені:n(H2) = 1,5 моль n(Al)
- 10. Слайд 10
- 11. Реакция өнімі шығымының үлесі
- 12. Көптеген химиялық реакциялар соңына дейін жүрмейді.Органикалық заттар
- 13. «Өнім шығымы» түсінігіне байланысты есептің үш типі
- 14. Бірінші типтегі есептерді шығару алгоритмі(реакция өнімінің
- 15. 4 Мысал Массасы 32,4г мырыш
- 16. Берілгені: m(ZnO) = 32,4 г mпр(Zn)
- 17. Берілгені: m(ZnO) = 32,4 г mпр(Zn)
- 18. Слайд 18
- 19. Есептің шартын мұқият оқып шығыңдар.«Берілгені» және «Табу
- 20. 5. Мысал Егер теориямен салыстырғанда реакцияның
- 21. Слайд 21
- 22. 4. Реакцияның өнімінің теориялық массасын есептеңдер.Шешуі:2Al(OH)3 =
- 23. 5) Кері формуланы қолдана отырып, реакция өнімінің
- 24. Слайд 24
- 25. 1. Есептің шартын мұқият оқып шығыңдар. 6.Мысал
- 26. 3. Реакция теңдеуін құрыңдар (коэффициенттерін қоюды ұмытпаңдар).Берілгені:m
- 27. 4. Кері формуланы қолдана отырып, (m пр
- 28. Слайд 28
- 29. Құрамында белгілі бір қоспасы бар, бастапқы заттардың
- 30. m зат mРеакция теңдеуі бойынша бөлінген газдың
- 31. Әрекеттесуші заттардың біреуі артық мөлшерде алынғанда түзілген
- 32. Слайд 32
- 33. 2.Олай болса, калий гидроксиді аз мөлшерде берілген
- 34. Тіркес теңдеулер бойынша есептерКөптеген химиялық процестер бірнеше
- 35. Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3
- 36. Слайд 36
- 37. Слайд 37
- 38. V= Жауабы: (Н3РО4) = 239,12 мл
- 39. 10. Мысал
- 40. Слайд 40
- 41. Үй тапсырмасы: 1 есеп Массалық үлесі
- 42. Қолданылған әдебиеттер 2.М.Б.Усманова, К.Н.Сақариянова. Химия
- 43. Өзін өзі бағалау парағы:
Слайд 2білімділік: оқушыларға сандық есептер шығару әдісін түсіндіріп, есептің негізгі типін шешуге
дамытушылық: оқытылатын ұғымдарды салыстыру, жалпылау, қорытындылауды үйрету, алған білімдерін өз бетінше пайдалана білуге дағдыландыру.
тәрбиелілік: пәнге деген ынтасын арттыру, өз бетімен жұмыс жасауды үйрету.
Сабақтың мақсаты
Слайд 3Химиялық теңдеулер дегеніміз – химиялық реакцияны формулалар мен коэффициенттердің көмегімен өрнектеп
молекулалар санын;
заттың моль санын;
газдар үшін газдың көлемін.
Химиялық теңдеулер бойынша есеп шығару зат массасының сақталу заңына негізделген; теңдеулер бойынша бірнеше түрлі есептер шығаруға болады ол есептермен бүгінгі сабақтың барысында танысамыз.
Слайд 4Химиялық теңдеулер
бойынша есептеулер
1.Эквиваленттік мөлшерде реакцияға түсетін заттардың біреуінің мөлшері (массасы,
2.Реакция өнімдерінің теорияға қарағандағы шығымдарын есептеу.
3. Құрамында белгілі бір қоспасы бар, бастапқы заттардың массалары (көлемдері бойынша реакция өнімдерінің массаларын (көлемдерін) есептеу.
4.Бірнеше тізбектес реакциялардың теңдеулері бойынша жүргізілетін есептеулер.
5.Орын басу реакцияларының теңдеулері бойынша есептеулер.
Слайд 5Химиялық реакция теңдеуін қолдана отырып сандық есептерді шығару алгоритмі.
1.Зейін қойып оқып,
2. Химиялық реакция теңдеуін құрыңдар.
3.Есептің шартына байланысты сәйкес келетін өлшем бірліктерін формуланың жоғарғы жағына көрсетіңдер.
4. Заттар формулаларының төменгі жағына реакция теңдеуі бойынша табылған сәйкес мәндерді көрсетіңдер.
5. Пропорционалды сәйкестікті құрып және оны шешіңдер.
6. Есептің жауабын жазыңдар.
Слайд 6Химиялық теңдеулер бойынша жүргізілетін есептеулердің мүмкін болатын варианттарын жалпы түрде қарастырып
Мұндай есептерді шешудің ең оңай жолы мынадай: алдымен қалайда болса, есептің шартында берілген заттың зат мөлшерін тауып алу керек, сонан соң, реакция теңдеуі бойынша қажетті зат мөлшерін табу керек. Оcыдан есептің шартында сұралып отырған шамаларға (масса, көлем, және т.б.) көшу өте оңай:
m = n * M
V = n * Vm
N= n * NA
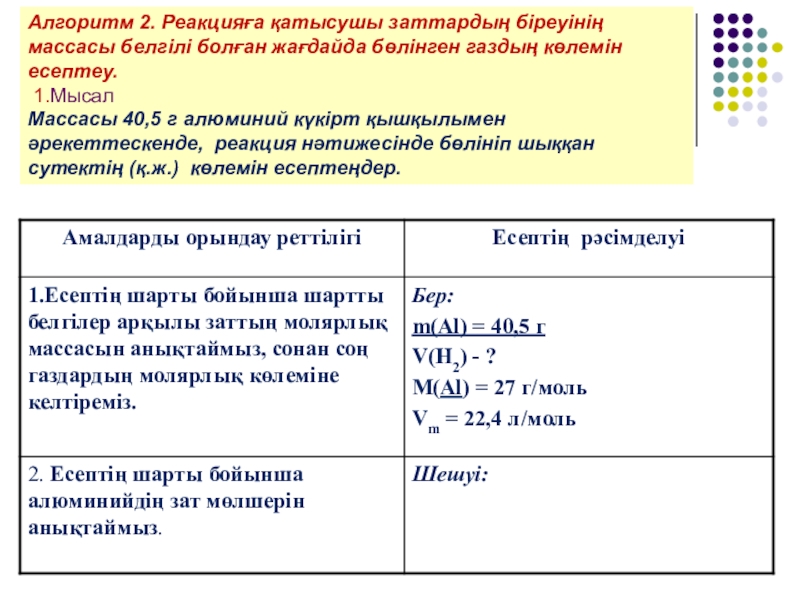
Слайд 7Алгоритм 2. Реакцияға қатысушы заттардың біреуінің массасы белгілі болған жағдайда бөлінген
Массасы 40,5 г алюминий күкірт қышқылымен әрекеттескенде, реакция нәтижесінде бөлініп шыққан сутектің (қ.ж.) көлемін есептеңдер.
Слайд 9Берілгені:
n(H2) = 1,5 моль
n(Al) – ?
Шешуі:
x моль
2Al + 6HCl = 2AlCl3 + 3H2↑
2 моль 3 моль
Пропорция құрамыз:
x = 1 (моль)
Жауабы: n(Al) = 1 моль
2 Мысал
Тұз қышқылының алюминиймен реакциясы кезінде 1,5 моль сутек газы бөлініп шықты. Реакцияға қажетті алюминийдің мөлшерін есептеңдер.
Слайд 11
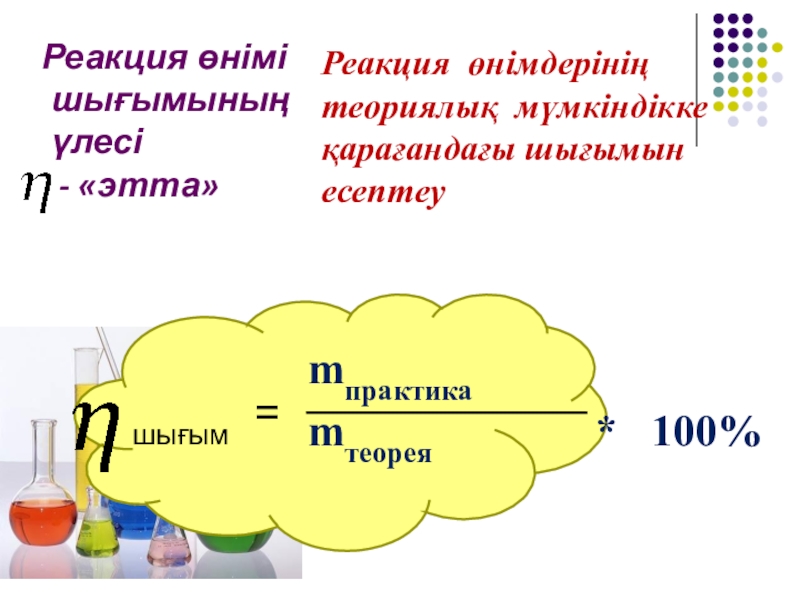
Реакция өнімі шығымының үлесі
- «этта»
Реакция өнімдерінің
теориялық мүмкіндікке
қарағандағы
есептеу
шығым =
mпрактика
mтеорея
* 100%
Слайд 12Көптеген химиялық реакциялар соңына дейін жүрмейді.
Органикалық заттар қатысында жүретін реакцияларда көбінесе
Гетерогенді реакциялар кезінде заттардың бір бөлігі реакцияға қатыспай қалады.
Химиялық реакциялардың жүруіне құрал – жабдықтарда әсерін тигізеді.
Қосылыстарды дұрыс жабылған герметикалық ыдыстарда жинамау, газтәрізді заттар мөлшерінің азаюына әкеледі.
Неліктен?
…
Шындығында жүретін химиялық
реакцияларда өнімнің массасы
барлық уақытта есептеудегі массаға
қарағанда үнемі аз болады?
Слайд 13«Өнім шығымы» түсінігіне байланысты есептің үш типі
1.Реакцияға қатысатын бастапқы
2. Бастапқы заттың массасы мен реакция өнімінің
шығымы берілген жағдай. Өнімнің массасын анықтау.
3.Өнімнің массасы мен реакция өнімінің шығымы берілген жағдай. Бастапқы заттың массасын анықтау.
Слайд 14
Бірінші типтегі есептерді шығару алгоритмі
(реакция өнімінің шығымын есептеу)
1.Есептің шартын
2. Жазып қойыңдар: «Берілгені» және «Табу керек».
3.Реакция теңдеуін құрыңдар (коэффициент қоюды ұмытпаңдар).
4.Реакция теңдеуі бойынша өнімнің теориялық массасын есептеңдер.
5.Есептің берілген шартына байланысты практикалық массасының теориялық массаға қатынасы бойынша өнімнің массалық үлесін есептеу.
Слайд 15
4 Мысал Массасы 32,4г мырыш оксиді мен алюминийдің әрекеттесуі
1.Есептің шартын мұқият оқып шығыңдар.
2.«Берілгені» және «Табу керек» деп жазыңдар.
Слайд 16Берілгені:
m(ZnO) = 32,4 г
mпр(Zn) = 24 г
Табу керек:
шығым(Zn) -
Шешуі:
3. Коэффициенттерді қойып, реакция теңдеуін құрыңдар.
3ZnO + 2Al = 3Zn + Al2O3
Слайд 17Берілгені:
m(ZnO) = 32,4 г
mпр(Zn) = 24 г
Табу керек:
шығым(Zn) -
Шешуі:
4.Реакция өнімінің теориялық массасын есепте.
32,4 г
3ZnO + 2Al = 3Zn + Al2O3
?
3 моль
3 моль
(ZnO) =
(Zn) =
m теор(Zn) = .M = 0,4 моль .65г/моль = 26 г
моль
Слайд 19 Есептің шартын мұқият оқып шығыңдар.
«Берілгені» және «Табу керек» деп жазыңдар.
Реакция теңдеуін
Химиялық реакцияның теңдеуі бойынша теориялық массаны есептеңдер.
Кері формуланы қолдана отырып реакция өнімінің практикалық массасын есептеңдер.
Екінші типтегі есептерді шығару алгоритмі
(реакция өнімінің шығымын есептеу)
(«реакция өнімінің массасы» (практикалық)
анықтау)
Слайд 20 5. Мысал Егер теориямен салыстырғанда реакцияның шығымы 92% болса,
Берілгені: Табу керек:
m (Al(OH)3)= 23,4 г
шығ (Al2O3) = 92%
Табу керек:
m пр (Al2O3) - ?
1. Есептің шартын мұқият оқып шығыңдар.
2. «Берілгені» және «Табу керек» деп жазыңдар.
Слайд 224. Реакцияның өнімінің теориялық массасын есептеңдер.
Шешуі:
2Al(OH)3 = Al2O3 +3H2O
23,4 г
х
2
1 моль
Теңдеу бойынша:
n(Al2O3) = ½ n(Al(OH)3= ½ =
m (Al(OH)3)
M (Al(OH)3)
23,4 г
78 г /моль
= 0,15 моль
mтеор. (Al2O3) = n M = 0,15 моль 102 г/моль = 15,3 г
Слайд 235) Кері формуланы қолдана отырып, реакция өнімінің практикалық массасын есептеңдер (теориялық
?
Шешуі:
2Al(OH)3 = Al2O3 +3H2O
23,4 г
х?
2 моль
1 моль
Теңдеу бойынша:
n(Al2O3) = ½ n(Al(OH)3= ½ =
m (Al(OH)3)
M (Al(OH)3)
23,4 г
78 г /моль
= 0,15 моль
mтеор. (Al2O3) = n M = 0,15 моль * 102 г/моль = 15,3 г
m пр.(Al2O3) = 15,3 г * 0,92 = 14 г
Жауабы: 14 грамм
Слайд 251. Есептің шартын мұқият оқып шығыңдар.
6.Мысал Темірдің (ІІІ) оксидіне көміртегінің
2. «Берілгені» және «Табу керек» деп жазу қажет.
Берілгені:
m пр (Fe) = 11,2 г
шығ (Fe) = 80%
Табу керек:
m (Fe2O3) - ?
Шешуі:
Слайд 263. Реакция теңдеуін құрыңдар (коэффициенттерін қоюды ұмытпаңдар).
Берілгені:
m пр (Fe) = 11,2
шығ (Fe) = 80%
Табу керек:
m (Fe2O3) - ?
Шешуі:
Fe2O3 + 3CO = 2Fe + 3CO2
Слайд 274. Кері формуланы қолдана отырып, (m пр / шығ) реакция
Берілгені:
m пр (Fe) = 11,2 г
шығ (Fe) = 80%
Табу керек:
m (Fe2O3) - ?
Шешуі:
Fe2O3 + 3CO = 2Fe + 3CO2
mтеор = = =14 г
mпр (Fe)
шығ(Fe)
11,2 г
0, 8
Слайд 29
Құрамында белгілі бір қоспасы бар, бастапқы заттардың массалары (көлемдері бойынша реакция
7. Мысал
Құрамында 10% жанбайтын қоспасы бар 20 г көмір жанғанда неше литр
(қ.ж.) көмірқышқыл газы бөлінеді?
Бер:
W(қоспа) = 10%
m (C) = 20 г
шешуі
С+ О2 = CO2
Массалық үлесі бойынша реакцияға түсетін таза заттың массасын есептеу:
100% - 10 % = 90% (С)
*100%
Слайд 30m зат
m
Реакция теңдеуі бойынша бөлінген газдың көлемін есептейміз:
V = 1,5
Жауабы:V(CO2) = 33,6 л
Слайд 31Әрекеттесуші заттардың біреуі артық мөлшерде
алынғанда түзілген заттың массасын есептеу.
8.Мысал
Массасы 15г
Бер: AlCl3 + 3KOH = Al(OH)3 + 3KCl
m (AlCl3) = 30 г
m(KOH) = 15 г
Табу керек: m(AlOH)3 - ?
Слайд 332.Олай болса, калий гидроксиді аз мөлшерде берілген 0,88 ˂ 0,22, ол
Слайд 34Тіркес теңдеулер бойынша есептер
Көптеген химиялық процестер бірнеше сатыда жүреді. Өндірістік тақырыптарға
9.Мысал
Құрамында 37% фосфор ангидриді бар 0,5 т фосфориттен тығыздығы 1,526 г/мл, массалық үлесі 70% болатын қанша фосфор қышқылын алуға болады?
w (P2O5) = 37%
m (Ca3(PO4)2 = 0,5 т
p(H3PO4) = 1,526 г/мл
w (Н3PO4) = 70%
т/к: V(H3PO4) =?
Слайд 35Ca3(PO4)2 + 3SiO2 + 5C = 3CaSiO3 + 2P + 5CO 4P
Осы тізбектен бастапқы шикізаттан соңғы өнімге дейінгі есептеулерді жүргіземіз:
Ca3(PO4)2 → P2O5
Слайд 41Үй тапсырмасы:
1 есеп
Массалық үлесі 66% -дық тығыздығы 1,403 г/мл
1000 л азот қышқылын алу үшін қанша ауа керек. (
= 78%).
2 есеп
Екі валентті металл оксидінің эквиваленттік массасы 39,77 г болса, көлемі 5,6 л (қ.ж.) сутегімен әрекеттесетін массасын есептеңдер.
3 есеп
Массасы 20 г көмір жанғанда 33,6 л (қ.ж.) газ түзілетін болса, көмірдің тазалығы қандай?
Слайд 42Қолданылған әдебиеттер
2.М.Б.Усманова, К.Н.Сақариянова. Химия Сандық есептер шығару әдістемесі.
3.
4.Қ. Бекишев. Химия есептері.- Алматы: РБК, 1998
5. Шамова М.О., “Учимся решать расчетные задачи по химии”, М.: “Школа – Пресс” 1999.
1.Ерыгин Д.П., Шишкин Е.А. Методика решения задач по химии М. Просвещение, 1989;