- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему d-металлы (11 класс)
Содержание
- 1. Презентация по химии на тему d-металлы (11 класс)
- 2. В периодической системе d-элементы или переходные металлы
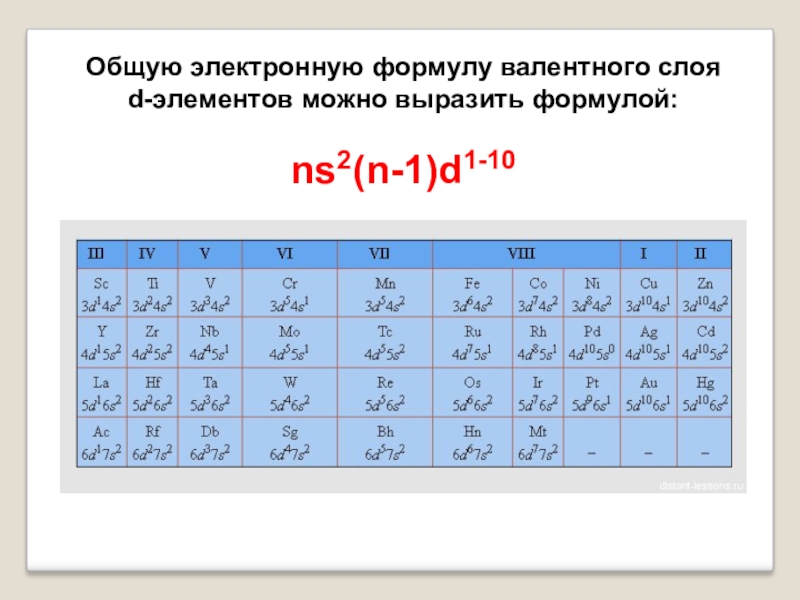
- 3. Общую электронную формулу валентного слоя d-элементов можно выразить формулой: ns2(n-1)d1-10
- 4. В периоде слева направо происходит некоторое уменьшение
- 5. У элементов IIIВ группы атомные радиусы возрастают,
- 6. В химических реакциях электроны d-орбиталей участвуют после
- 7. Таким образом, особенностями электронного строения
- 8. Физические свойства d-металловФизические свойства переходных металлов зависят
- 9. Химические свойства d-металловВсе d-элементы являются восстановителями. Восстановительная
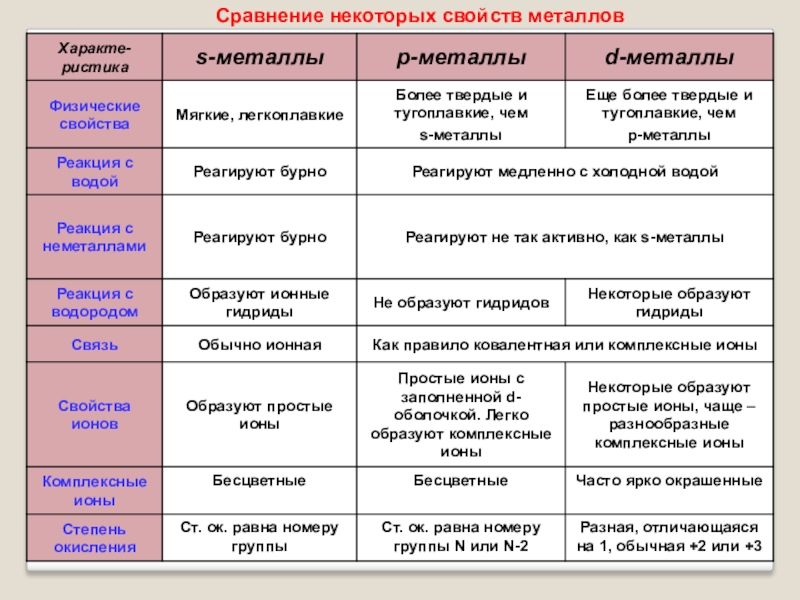
- 10. Сравнение некоторых свойств металлов
- 11. Строение и свойства соединений d-элементов зависят от степени окисления металла
- 12. Оксиды и гидроксиды d-элементовПереходные металлы реагируют с
- 13. «Вулкан»
- 14. «Огненная метель»
- 15. Гидроксиды переходных металлов получают добавлением щелочей к
- 16. Свойства соединений d-элементовС ростом степени окисления атома металла кислотные свойства соответствующих соединений усиливаются:Свойства соединений d-элементов
- 17. В пределах одной подгруппы для гидроксидов и
- 18. В периоде кислотные свойства гидроксидов в высшей
В периодической системе d-элементы или переходные металлы расположены в побочных подгруппах (или В подгруппах) всех восьми групп. Это элементы, которые при образовании соединений имеют незаполненную d-орбиталь. Под определение не подпадают скандий (3d0 в соединениях)
Слайд 2 В периодической системе d-элементы или переходные металлы расположены в побочных подгруппах
(или В подгруппах) всех восьми групп.
Это элементы, которые при образовании соединений имеют незаполненную d-орбиталь.
Под определение не подпадают скандий (3d0 в соединениях) и цинк (3d10 в соединениях); медь же входит в группу указанных соединений, если имеет в них конфигурацию 3d9.
Принято, однако, относить эти металлы к d-металлам на основании химического сходства их соединений.
Это элементы, которые при образовании соединений имеют незаполненную d-орбиталь.
Под определение не подпадают скандий (3d0 в соединениях) и цинк (3d10 в соединениях); медь же входит в группу указанных соединений, если имеет в них конфигурацию 3d9.
Принято, однако, относить эти металлы к d-металлам на основании химического сходства их соединений.
Слайд 4В периоде слева направо происходит некоторое уменьшение атомного радиуса элементов. Это
обусловлено эффектом «d-сжатия», вызванного постепенным увеличением заряда ядер и усилением кулоновского притяжения электронов к ядру.
В подгруппах сверху вниз (кроме IIIB группы) атомный радиус несколько уменьшается или остается практически неизменным за счет сокращения размеров внутренних f-орбиталей («лантаноидное сжатие»). При этом химическая активность металлов уменьшается, что отличает их от металлов главных подгрупп.
В подгруппах сверху вниз (кроме IIIB группы) атомный радиус несколько уменьшается или остается практически неизменным за счет сокращения размеров внутренних f-орбиталей («лантаноидное сжатие»). При этом химическая активность металлов уменьшается, что отличает их от металлов главных подгрупп.
Слайд 5У элементов IIIВ группы атомные радиусы возрастают, химическая активность увеличивается, благодаря
чему они проявляют большее сходство с элементами главных подгрупп, чем побочных. По реакционной способности элементы подгруппы скандия уступают лишь щелочным и щелочноземельным металлам.
В периодах слева направо металлические свойства уменьшаются.
Минимальные восстановительные свойства проявляют тяжелые металлы VIIIB и IB – групп. За свою инертность они названы благородными.
В периодах слева направо металлические свойства уменьшаются.
Минимальные восстановительные свойства проявляют тяжелые металлы VIIIB и IB – групп. За свою инертность они названы благородными.
Слайд 6В химических реакциях электроны d-орбиталей участвуют после того, как оказываются использованными
s-электроны внешнего энергетического уровня.
В образовании связей могут участвовать все или только часть d-электронов предпоследнего энергетического уровня, поэтому образуются соединения с различной валентностью или степенью окисления (кроме d-элементов II и III групп).
Например, характерными для элементов VIIIВ группы являются следующие степени окисления (в скобках – наиболее устойчивые):
Fe Co Ni семейство железа
+2,(+3),+6 +2,(+3) +2,(+3)
Ru Rh Pd легкие платиновые металлы
+3,(+4),+6,+8 (+3),+4 (+2),(+4)
Оs Ir Pt тяжелые платиновые металлы
+4,(+6),+8 +3,(+4) +2,(+4),+6
В образовании связей могут участвовать все или только часть d-электронов предпоследнего энергетического уровня, поэтому образуются соединения с различной валентностью или степенью окисления (кроме d-элементов II и III групп).
Например, характерными для элементов VIIIВ группы являются следующие степени окисления (в скобках – наиболее устойчивые):
Fe Co Ni семейство железа
+2,(+3),+6 +2,(+3) +2,(+3)
Ru Rh Pd легкие платиновые металлы
+3,(+4),+6,+8 (+3),+4 (+2),(+4)
Оs Ir Pt тяжелые платиновые металлы
+4,(+6),+8 +3,(+4) +2,(+4),+6
Слайд 7
Таким образом,
особенностями электронного строения d-элементов обусловлены
и их свойства:
а) большое разнообразие проявляемых валентностей и степеней окисления;
б) способность образовывать различные комплексные соединения;
в) каталитическая активность.
а) большое разнообразие проявляемых валентностей и степеней окисления;
б) способность образовывать различные комплексные соединения;
в) каталитическая активность.
Слайд 8Физические свойства d-металлов
Физические свойства переходных металлов зависят от электронного строения, от
числа неспаренных d-электронов, которые могут участвовать в образовании связей.
Металлы, у которых по 3–4 неспаренных d-электрона (VВ и VIВ группы), имеют максимальную температуру плавления и кипения.
Переходные металлы, имеющие на внешнем s-подуровне один электрон, как правило, имеют более высокую электрическую проводимость (Cr, Мo и особенно Cu, Ag, Au).
Элементы III-В группы, имеющие всего один d-электрон, по своим свойствам близки к соседним щелочноземельным металлом,
а металлы II-В группы с полностью заполненным d-подуровнем близки по свойствам к соседним р-элементам.
Металлы, у которых по 3–4 неспаренных d-электрона (VВ и VIВ группы), имеют максимальную температуру плавления и кипения.
Переходные металлы, имеющие на внешнем s-подуровне один электрон, как правило, имеют более высокую электрическую проводимость (Cr, Мo и особенно Cu, Ag, Au).
Элементы III-В группы, имеющие всего один d-электрон, по своим свойствам близки к соседним щелочноземельным металлом,
а металлы II-В группы с полностью заполненным d-подуровнем близки по свойствам к соседним р-элементам.
Слайд 9Химические свойства d-металлов
Все d-элементы являются восстановителями. Восстановительная способность в растворах в
пределах периода уменьшается.
Наиболее сильными восстановителями являются металлы IIIВ группы.
У большинства d-элементов образуются защитные оксидные пленки, вызывающие их пассивацию и предохраняющие их от коррозии. Наиболее склонны к пассивации металлы IVВ–VIВ групп.
Элементы IIIВ и IIВ групп (кроме ртути) легко взаимодействуют с разбавленными кислотами, а лантан взаимодействует и с водой.
Не взаимодействуют с разбавленными кислотами металлы IВ группы, ртуть и платиновые металлы (Ru, Rh, Pd, Os, Ir, Pt).
Наиболее сильными восстановителями являются металлы IIIВ группы.
У большинства d-элементов образуются защитные оксидные пленки, вызывающие их пассивацию и предохраняющие их от коррозии. Наиболее склонны к пассивации металлы IVВ–VIВ групп.
Элементы IIIВ и IIВ групп (кроме ртути) легко взаимодействуют с разбавленными кислотами, а лантан взаимодействует и с водой.
Не взаимодействуют с разбавленными кислотами металлы IВ группы, ртуть и платиновые металлы (Ru, Rh, Pd, Os, Ir, Pt).
Слайд 12Оксиды и гидроксиды d-элементов
Переходные металлы реагируют с кислородом, образуя оксиды (искл.
Ag, Au). Почти все они нерастворимы в воде, черного или иного цвета. Обладают заметной ковалентностью связей.
Оксид железа (II) FeO,
магнитный железняк (магнетит) Fe3O4
и красный железняк (гематит) Fe2O3 (в чашке).
Оксид хрома Сr2O3
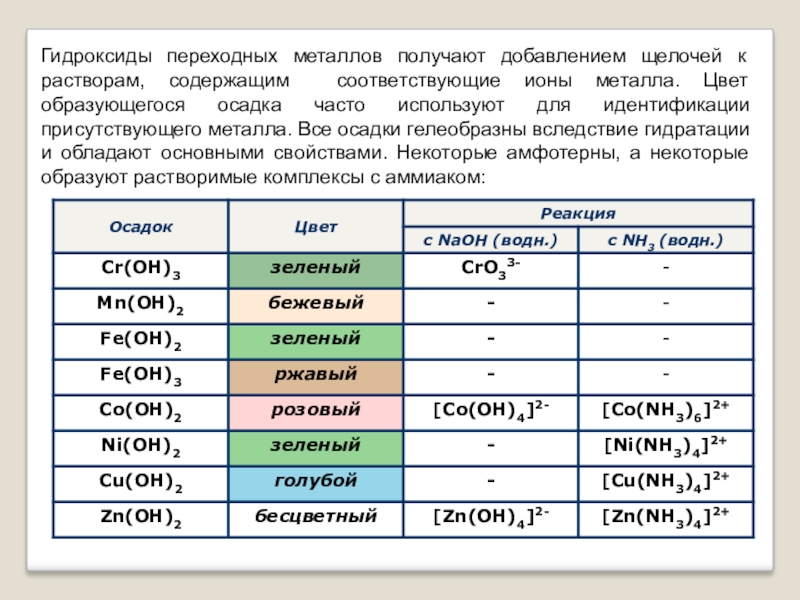
Слайд 15Гидроксиды переходных металлов получают добавлением щелочей к растворам, содержащим соответствующие ионы
металла. Цвет образующегося осадка часто используют для идентификации присутствующего металла. Все осадки гелеобразны вследствие гидратации и обладают основными свойствами. Некоторые амфотерны, а некоторые образуют растворимые комплексы с аммиаком:
Слайд 16
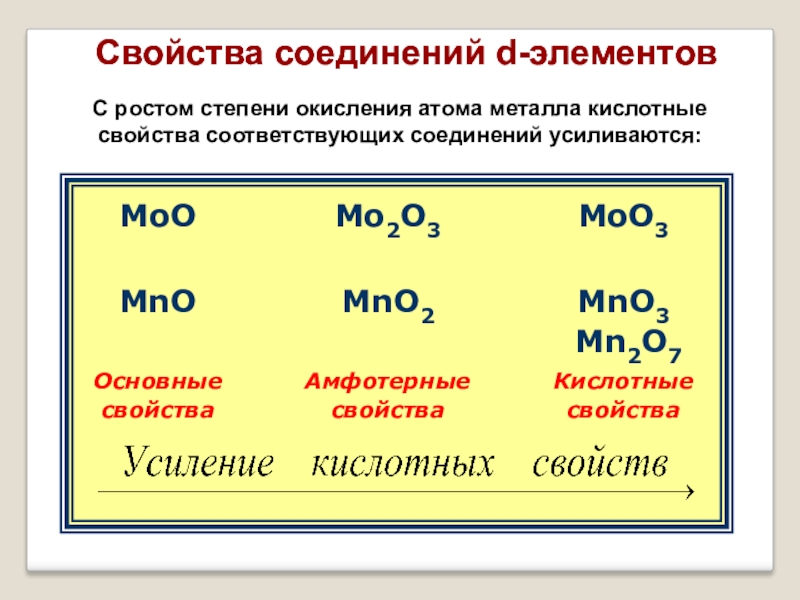
Свойства соединений d-элементов
С ростом степени окисления атома металла кислотные свойства соответствующих
соединений усиливаются:
Свойства соединений d-элементов
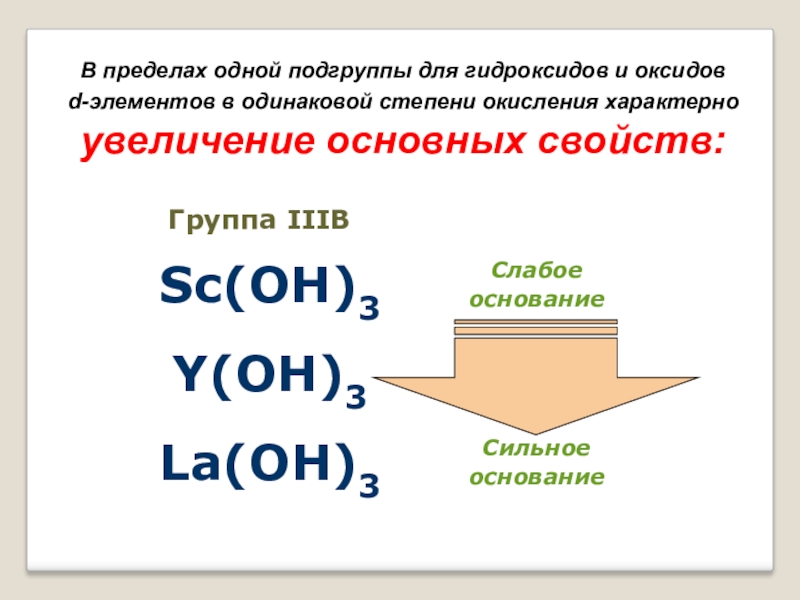
Слайд 17В пределах одной подгруппы для гидроксидов и оксидов
d-элементов в одинаковой
степени окисления характерно
увеличение основных свойств:
увеличение основных свойств:
Слайд 18
В периоде кислотные свойства гидроксидов в высшей степени окисления металла усиливаются:
Ti(OH)4
– HVO3 – H2CrO4 – HMnO4 – H2FeO4