- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
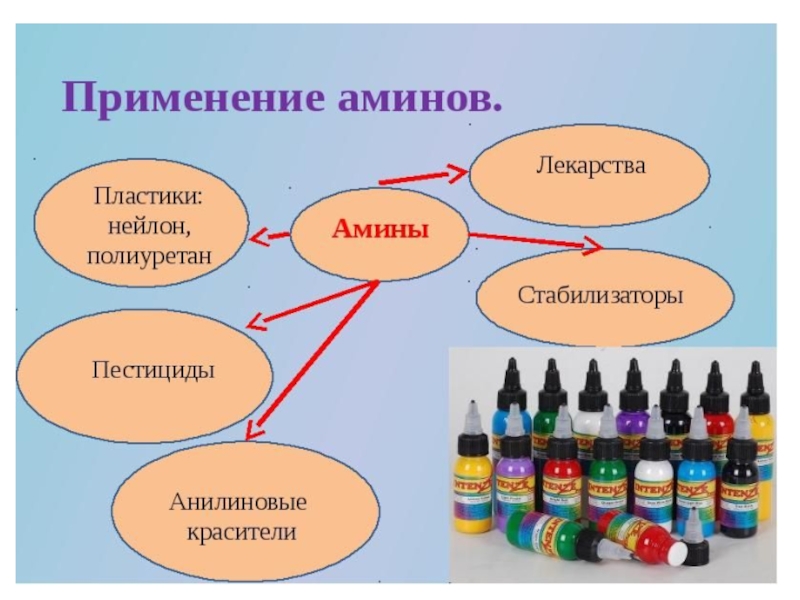
Презентация, доклад по химии на тему Амины
Содержание
- 1. Презентация по химии на тему Амины
- 2. Аминами называются соединения, которые могут быть произведены от аммиака замещением в нем атомов водорода на углеводородные радикалы.
- 3. Номенклатура аминов основывается на названии углеводородных
- 4. Классификация аминов1) По числу углеводородных радикалов, связанных с атомом азота амины делят на:
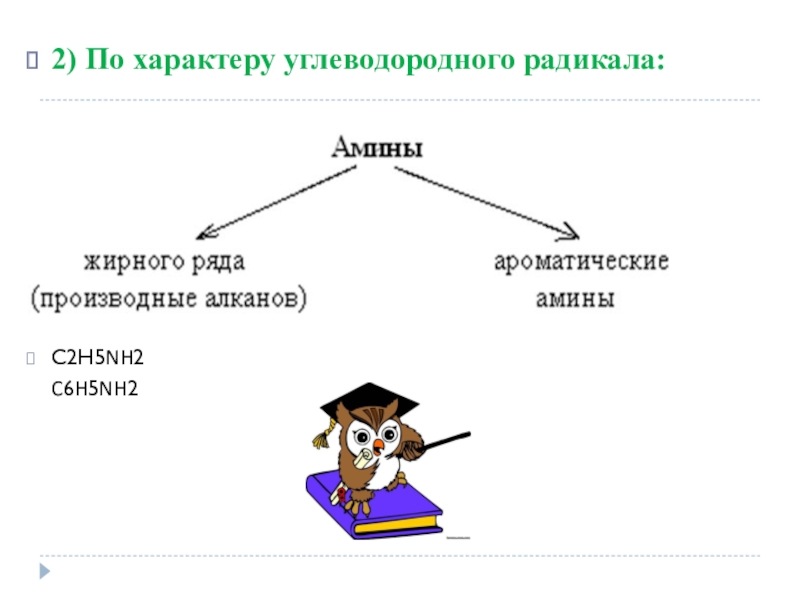
- 5. 2) По характеру углеводородного радикала:С2Н5NH2
- 6. Изомерия аминов
- 7. Строение аминовАтом азота в молекуле аминов находится
- 8. Получение аминов Из-за запаха низшие амины долгое время
- 9. В 1842 г Н. Н. Зинин получил анилин -восстановлением нитробензола в промышленности
- 10. 1) Восстановление нитросоединений: R-NO2 + 6[H] t,kat-Ni → R-NH2 + 2H2O2) Алкилирование аммиака
- 11. 3) Лабораторный - действие щелочей на соли алкиламмония(получение
- 12. Слайд 12
- 13. Химические свойства аминовОсновные свойства:Алифатические амины – более сильные
- 14. Ряд увеличения основных свойств аминов:Водные растворы аминов
- 15. 2) Взаимодействие с кислотами (донорно-акцепторный механизм):2CH3-NH2 + H2SO4 → [CH3-NH3]2SO4
- 16. Особые свойства анилинаДля анилина характерны реакции, как
- 17. б) Свойства аминогруппы: С6Н5NН2 + HCl → [С6Н5NН3 ]+Сl- хлорид фениламмония
- 18. Слайд 18
- 19. Выполните задания:Задание 1.Назовите амины, формулы которых:1- уровеньа)
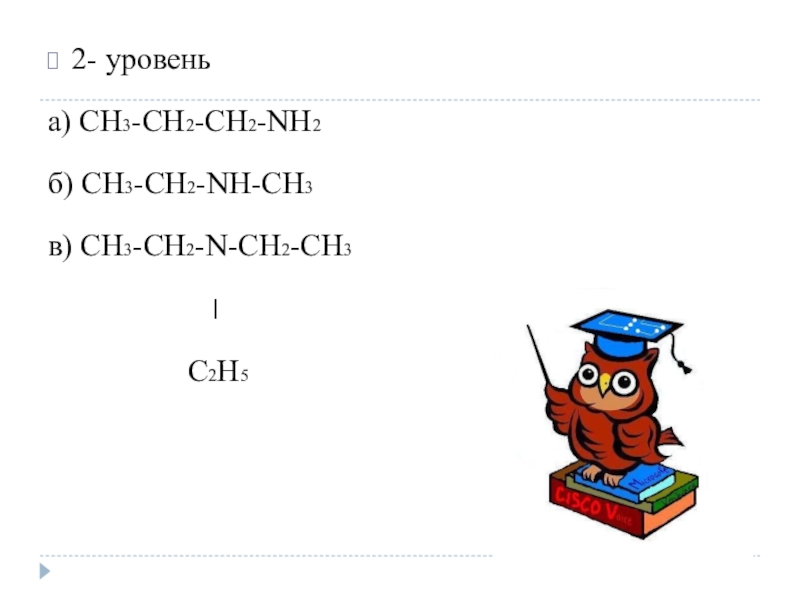
- 20. 2- уровеньа) CH3-CH2-CH2-NH2б) CH3-CH2-NH-CH3в) CH3-CH2-N-CH2-CH3
- 21. Задание 2.Расположите в ряд по возрастанию основные
- 22. Эталоны ответов:Задание1.1 уровень:а) этиламинб) пропиламин -2в) метилпропиламин2 уровень:а) пропиламин – 1б) метилэтиламинв) триэтиламин
- 23. Задание 2.Дифениламин – фениламин – аммиак –
Аминами называются соединения, которые могут быть произведены от аммиака замещением в нем атомов водорода на углеводородные радикалы.
Слайд 2Аминами называются соединения, которые могут быть произведены от аммиака замещением в нем
атомов водорода на углеводородные радикалы.
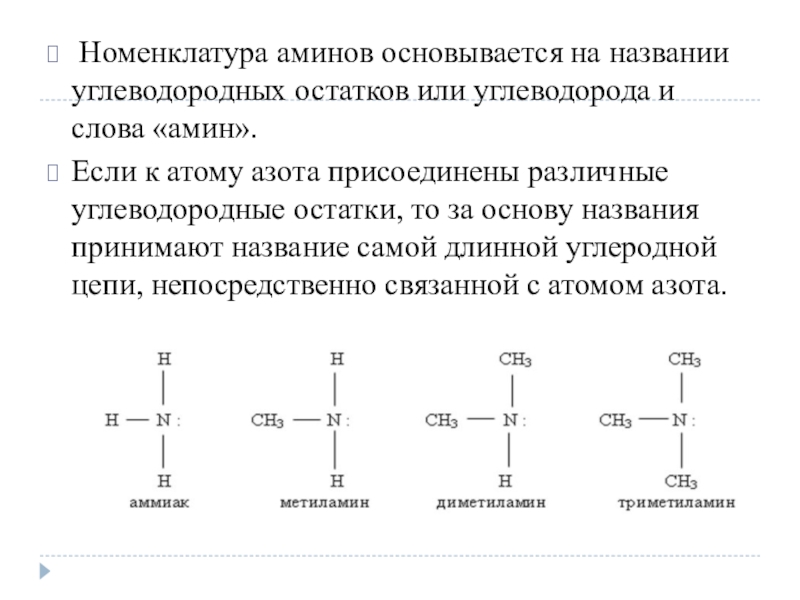
Слайд 3 Номенклатура аминов основывается на названии углеводородных остатков или углеводорода и
слова «амин».
Если к атому азота присоединены различные углеводородные остатки, то за основу названия принимают название самой длинной углеродной цепи, непосредственно связанной с атомом азота.
Если к атому азота присоединены различные углеводородные остатки, то за основу названия принимают название самой длинной углеродной цепи, непосредственно связанной с атомом азота.
Слайд 4Классификация аминов
1) По числу углеводородных радикалов, связанных с атомом азота амины
делят на:
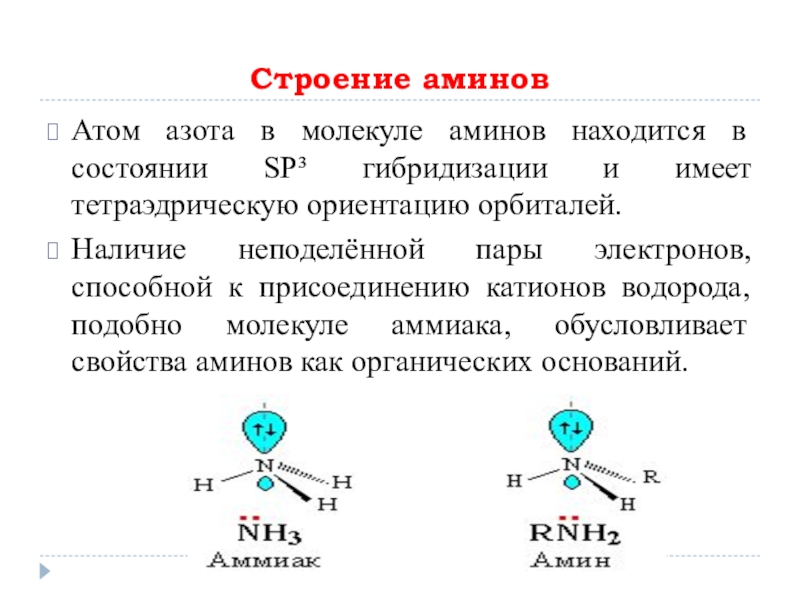
Слайд 7Строение аминов
Атом азота в молекуле аминов находится в состоянии SP³ гибридизации
и имеет тетраэдрическую ориентацию орбиталей.
Наличие неподелённой пары электронов, способной к присоединению катионов водорода, подобно молекуле аммиака, обусловливает свойства аминов как органических оснований.
Наличие неподелённой пары электронов, способной к присоединению катионов водорода, подобно молекуле аммиака, обусловливает свойства аминов как органических оснований.
Слайд 8Получение аминов
Из-за запаха низшие амины долгое
время принимали за аммиак, пока
в 1849 году французский химик
Шарль Вюрц не выяснил,
что в отличие от аммиака,
они горят на воздухе
с образованием
углекислого газа.
Он же синтезировал
метиламин и этиламин.
Шарль Вюрц не выяснил,
что в отличие от аммиака,
они горят на воздухе
с образованием
углекислого газа.
Он же синтезировал
метиламин и этиламин.
Слайд 101) Восстановление нитросоединений:
R-NO2 + 6[H] t,kat-Ni → R-NH2 + 2H2O
2) Алкилирование аммиака осуществляют нагреванием галогеноалканов с
аммиаком под давлением ( промышленный способ).
CH3Cl + 2NH3 t, ↑p → CH3-NH2 + NH4Cl
CH3Cl + 2NH3 t, ↑p → CH3-NH2 + NH4Cl
Слайд 11 3) Лабораторный - действие щелочей на соли алкиламмония
(получение первичных, вторичных, третичных аминов):
[R-NH3]Г
+ NaOH t → R-NH2 + NaГ + H2O
4).Пропусканием паров спирта и аммиака при 300оС над катализатором.
С2Н5ОН + NН3 → С2Н5-NН2 +Н2О
4).Пропусканием паров спирта и аммиака при 300оС над катализатором.
С2Н5ОН + NН3 → С2Н5-NН2 +Н2О
Слайд 13Химические свойства аминов
Основные свойства:
Алифатические амины – более сильные основания, чем аммиак, т.к.
алкильные радикалы увеличивают электронную плотность на атоме азота за счет
+I-эффекта.
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.
+I-эффекта.
Ароматические амины являются более слабыми основаниями, чем аммиак, поскольку неподеленная электронная пара атома азота смещается в сторону бензольного кольца, вступая в сопряжение с его π-электронами.
Слайд 14Ряд увеличения основных свойств аминов:
Водные растворы аминов имеют щелочную реакцию (амины реагируют
с водой по донорно-акцепторному механизму):
R-NH2 + H2O → [R-NH3]+ + OH-
Анилин с водой не реагирует и не изменяет окраску индикатора!!!
R-NH2 + H2O → [R-NH3]+ + OH-
Анилин с водой не реагирует и не изменяет окраску индикатора!!!
Слайд 152) Взаимодействие с кислотами (донорно-акцепторный механизм):
2CH3-NH2 + H2SO4 → [CH3-NH3]2SO4
(соль – сульфат метиламмония)
3) Реакция горения (полного окисления) аминов на примере метиламина:
4СH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2
3) Реакция горения (полного окисления) аминов на примере метиламина:
4СH3NH2 + 9O2 → 4CO2 + 10H2O + 2N2
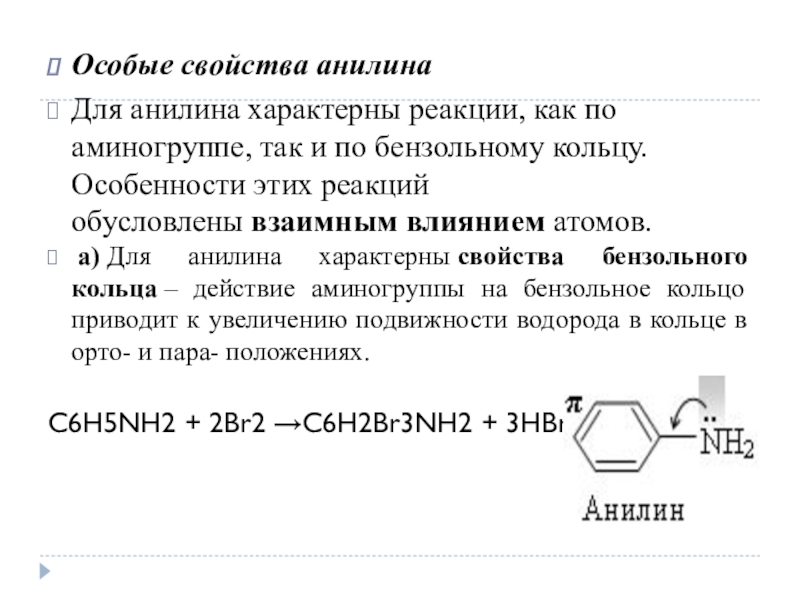
Слайд 16Особые свойства анилина
Для анилина характерны реакции, как по аминогруппе, так и
по бензольному кольцу. Особенности этих реакций обусловлены взаимным влиянием атомов.
а) Для анилина характерны свойства бензольного кольца – действие аминогруппы на бензольное кольцо приводит к увеличению подвижности водорода в кольце в орто- и пара- положениях.
C6H5NH2 + 2Br2 →C6H2Br3NH2 + 3HBr
а) Для анилина характерны свойства бензольного кольца – действие аминогруппы на бензольное кольцо приводит к увеличению подвижности водорода в кольце в орто- и пара- положениях.
C6H5NH2 + 2Br2 →C6H2Br3NH2 + 3HBr
Слайд 19Выполните задания:
Задание 1.
Назовите амины, формулы которых:
1- уровень
а) CH3-CH2-NH2
б) CH3-CH-CH3
׀
NH2
в) CH3-NH-CH2-CH2-CH3
NH2
в) CH3-NH-CH2-CH2-CH3
Слайд 21Задание 2.
Расположите в ряд по возрастанию основные свойства веществ: а) диметиламин,
б) дифениламин, в) фениламин, г) аммиак, д) метиламин.
Ответ поясните.
Ответ поясните.
Слайд 22Эталоны ответов:
Задание1.
1 уровень:
а) этиламин
б) пропиламин -2
в) метилпропиламин
2 уровень:
а) пропиламин – 1
б)
метилэтиламин
в) триэтиламин
в) триэтиламин
Слайд 23Задание 2.
Дифениламин – фениламин – аммиак – метиламин – диметиламин
Алкильные радикалы
обладают положительным индуктивным эффектом. Они увеличивают электронную плотность на азоте, основность амина возрастает. Метиламин более сильное основание, чем аммиак, а диметиламин – чем метиламин. В анилине неподелённая электронная пара азота вовлечена в ароматическое сопряжение бензольного кольца. Поэтому основность у анилина меньше, чем у аммиака.






![Презентация по химии на тему Амины 1) Восстановление нитросоединений: R-NO2 + 6[H] t,kat-Ni → R-NH2 + 2H2O2) Алкилирование аммиака осуществляют нагреванием галогеноалканов с 1) Восстановление нитросоединений: R-NO2 + 6[H] t,kat-Ni → R-NH2 + 2H2O2) Алкилирование аммиака осуществляют нагреванием галогеноалканов с аммиаком под давлением ( промышленный способ).CH3Cl](/img/thumbs/1ceb090b82fd8ae8ee99f471c00b5af6-800x.jpg)
![Презентация по химии на тему Амины 3) Лабораторный - действие щелочей на соли алкиламмония(получение первичных, вторичных, третичных аминов):[R-NH3]Г 3) Лабораторный - действие щелочей на соли алкиламмония(получение первичных, вторичных, третичных аминов):[R-NH3]Г + NaOH t → R-NH2 + NaГ + H2O 4).Пропусканием](/img/thumbs/0ec90fcf9955e28436161bef4fbc6096-800x.jpg)



![Презентация по химии на тему Амины 2) Взаимодействие с кислотами (донорно-акцепторный механизм):2CH3-NH2 + H2SO4 → [CH3-NH3]2SO4 2) Взаимодействие с кислотами (донорно-акцепторный механизм):2CH3-NH2 + H2SO4 → [CH3-NH3]2SO4](/img/tmb/5/437253/edd552fd0f6786355ae7b6c66eda7417-800x.jpg)
![Презентация по химии на тему Амины б) Свойства аминогруппы: С6Н5NН2 + HCl → [С6Н5NН3 ]+Сl- хлорид фениламмония б) Свойства аминогруппы: С6Н5NН2 + HCl → [С6Н5NН3 ]+Сl- хлорид фениламмония](/img/tmb/5/437253/945080594556a90818582e98746a4087-800x.jpg)