Химическая связь
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии на тему
Содержание
- 1. Презентация по химии на тему
- 2. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 3. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 4. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 5. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 6. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 7. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 8. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 9. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 10. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 11. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 12. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 13. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 14. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 15. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 16. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 17. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 18. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 19. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 20. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 21. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 22. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 23. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 24. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 25. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 26. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 27. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 28. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 29. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 30. Аминокислоты Синтетические Получают кислотным гидролизом белков
- 31. Определите тип химической связи в веществах,
- 32. Какая из химических связей наиболее полярна? Почему?
- 33. В каких
Слайд 1Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Слайд 2Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
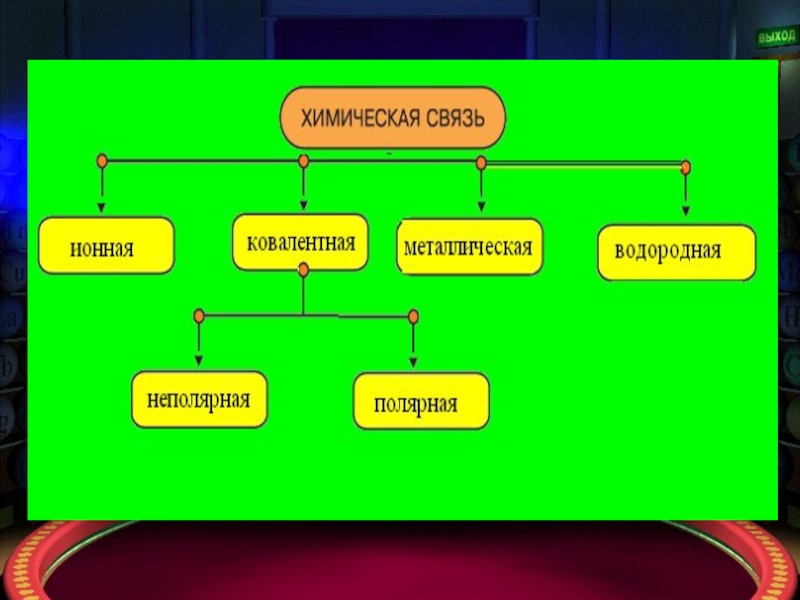
Химическая связь – взаимодействие между атомами, приводящее к образованию устойчивой многоатомной системы – молекулы, иона, кристалла.
Слайд 3Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Причина образования химической связи – стремление системы к min энергии: при образовании химической связи энергия выделяется, образующаяся система обладает меньшей энергией, чем изолированные атомы, которыми она образована.
Слайд 4Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Кроме того, большинство атомов стремится к завершению внешнего энергетического уровня путем образования химических связей.
Слайд 5Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Слайд 6Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Ионная связь – это связь, возникающая за счет электростатического притяжения разноименно заряженных ионов.
Ионная связь образуется только между атомами таких элементов, которые значительно отличаются по своей электроотрицательности (разность >1,7).
Слайд 7Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
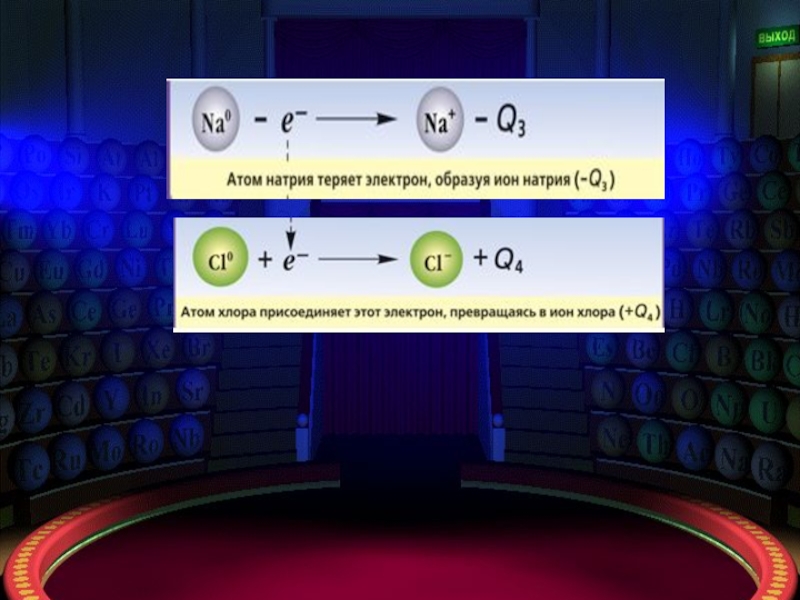
Металлы способны отдавать электроны, превращаясь в положительно заряженные ионы – катионы.
Ме0 – nē → Меn+
Неметаллы способны принимать электроны, превращаясь в положительно заряженные ионы – анионы.
неМе0 + nē → неМеn-
Слайд 8Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Слайд 9Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Слайд 10Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
.. ..
Na. + .Cl: → Na+ + :Cl: -
.. ..
Слайд 11Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
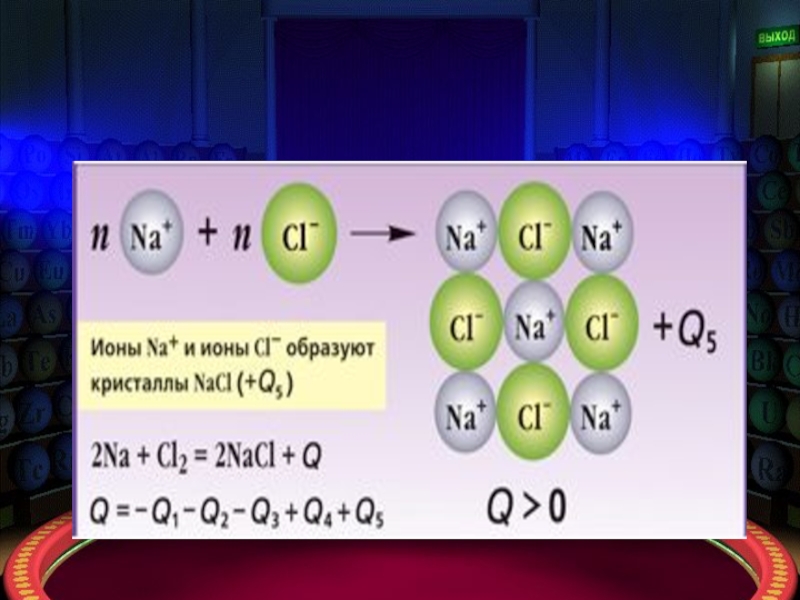
Вещества с ионной связью при обычных условиях находятся в твердом агрегатном состоянии и образуют кристаллы с ионной решеткой: в её узлах находятся ионы.
Слайд 12Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Физические свойства:
твердые, но хрупкие;
нелетучие;
тугоплавкие;
многие растворимы;
в растворах и расплавах
проводят электрический ток.
Слайд 13Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Ионная связь характеризуется:
ненаправленностью – ион может притягиваться к
другому иону по любому направлению.
ненасыщаемостью – взаимодействие иона с
другим ионом не компенсирует его силовое поле,
и он не теряет способности притягивать ионы по
другим направлениям.
Слайд 14Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Ковалентная связь – это связь между атомами, возникающая за счет образования общих электронных пар.
Различают два механизма образования ковалентной связи:
Слайд 15Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Обменный - когда каждый атом отдаёт неспаренный электрон для образования общей электронной пары.
Слайд 16Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
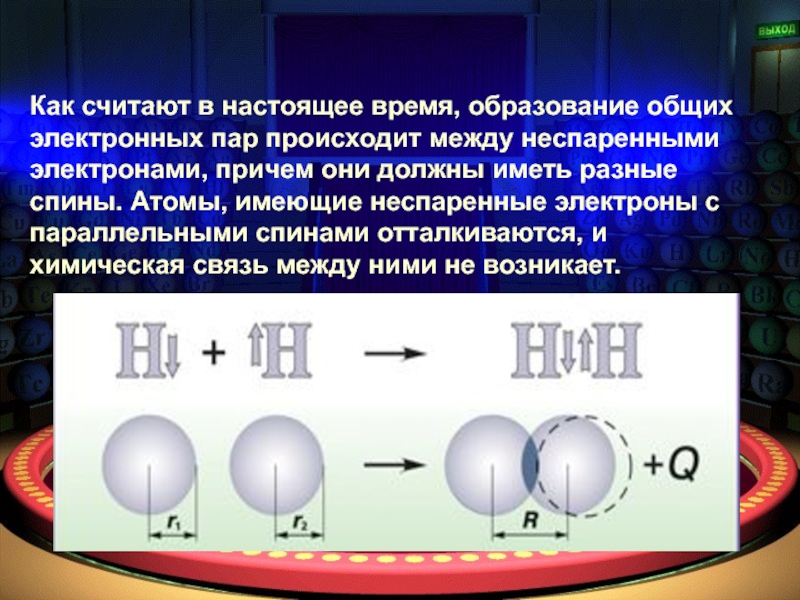
Как считают в настоящее время, образование общих электронных пар происходит между неспаренными электронами, причем они должны иметь разные спины. Атомы, имеющие неспаренные электроны с параллельными спинами отталкиваются, и химическая связь между ними не возникает.
Слайд 17Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
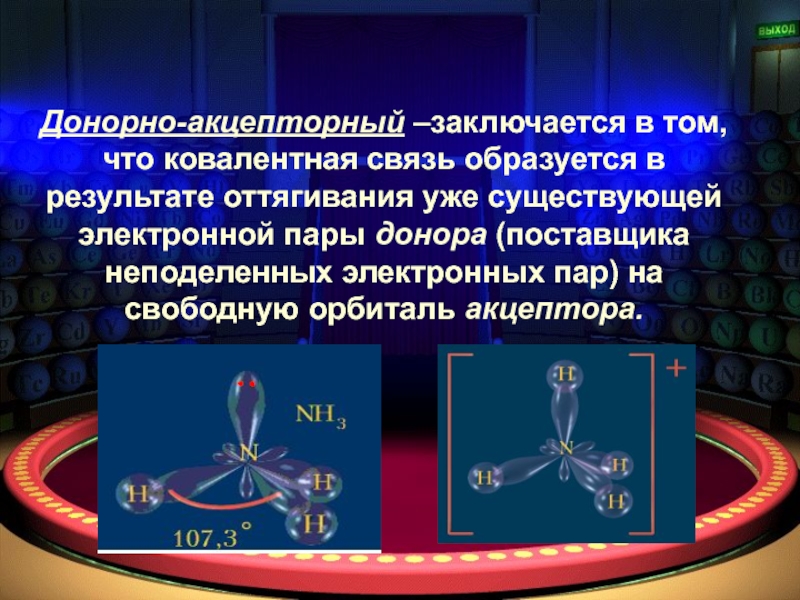
Донорно-акцепторный –заключается в том, что ковалентная связь образуется в результате оттягивания уже существующей электронной пары донора (поставщика неподеленных электронных пар) на свободную орбиталь акцептора.
Слайд 18Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Различают неполярную и полярную ковалентную связь.
При ковалентной неполярной связи электронное облако распределяется в пространстве на одинаковом расстоянии от ядер атомов. Такая связь возникает между молекулами, состоящими из одинаковых атомов ( например, молекулы водорода, кислорода).
Н-Н О=О Cl-Cl
При ковалентной полярной связи электронное облако смещено к атому с большей электроотрицательностью (разница <1,7).
Например: Н→Cl
Слайд 19Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Химическая связь, образованная в результате перекрывания электронных облаков вдоль условной линии, соединяющей центры атомов, называется σ-связью.
Связь, образованная при перекрывании электронных облаков, расположенных перпендикулярно условной линии, соединяющей центры атомов, называется π-связью.
В молекуле может присутствовать одновременно как σ, так и π-связь.
Слайд 20Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Характеристика
ковалентной
связи
Слайд 21Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Длина связи – это расстояние между центрами ядер атома в молекуле или кристалле.
Например:
Длина С- С связи в молекуле этана равна 0,154 нм
Длина С=С связи в молекуле этена равна 0,134 нм
Длина С ≡ С связи в молекуле этина равна 0,120 нм
Энергия связи – это мера прочности связи. Ее величина определяется выделенной или поглощенной энергией при разрушении или образовании связи.
Например, образование связей в 1 моль водорода сопровождается выделением 432, 1 кДж теплоты. Значит энергия связи Н-Н составляет 432,1 кДж/моль.
Слайд 22Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Число общих электронных пар равно числу связей между двумя атомами, или кратности связи.
Например: Н : Н Н – Н простая (одинарная) связь;
О :: О О = О двойная связь;
N :::N N ≡ N тройная связь.
Полярность связи – неравномерное распределение электронной плотности в молекуле.
Например: Н : Н Н – Н ков. неполярная связь.
Н :Сl Н →Сl ков. полярная связь.
Насыщаемость – способность атомов присоединять определенное число других атомов.
Слайд 23Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
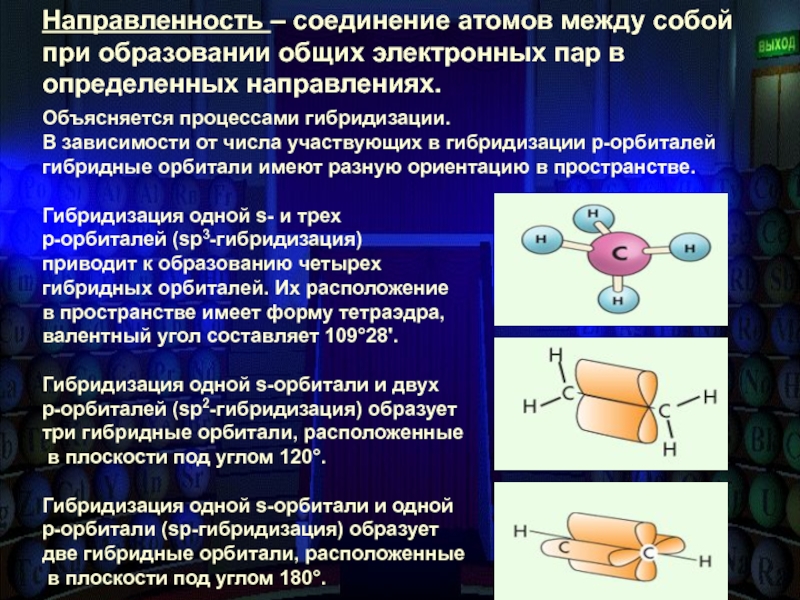
Направленность – соединение атомов между собой при образовании общих электронных пар в определенных направлениях.
Объясняется процессами гибридизации.
В зависимости от числа участвующих в гибридизации р-орбиталей гибридные орбитали имеют разную ориентацию в пространстве.
Гибридизация одной s- и трех
р-орбиталей (sр3-гибридизация)
приводит к образованию четырех
гибридных орбиталей. Их расположение
в пространстве имеет форму тетраэдра,
валентный угол составляет 109°28'.
Гибридизация одной s-орбитали и двух
р-орбиталей (sp2-гибридизация) образует
три гибридные орбитали, расположенные
в плоскости под углом 120°.
Гибридизация одной s-орбитали и одной
р-орбитали (sp-гибридизация) образует
две гибридные орбитали, расположенные
в плоскости под углом 180°.
Слайд 24Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Поляризуемость – способность неполярных связей становиться полярными под действием внешнего электрического поля.
Например: неполярная молекула Br2 становится полярной под действием электронной плотности двойной связи алкена.
СН2 Электроны ближайшего
║ Brδ+ → Brδ- к двойной связи атома
СН2 брома отталкиваются от
электронной плотности
двойной связи.
Слайд 25Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Физические свойства – зависят от типа кристаллической решетки.
Вещества с ковалентной связью могут иметь два типа кристаллической решетки.
1. Атомная кристаллическая решетка – в узлах её
атомы, между которыми ковалентные связи.
Физические свойства:
твердые;
нелетучие;
тугоплавкие;
нерастворимые в воде.
Примеры веществ: Al2O3, Fe2O3, B, карборунд SiC,
кварц SiO2.
Слайд 26Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
2. Молекулярная кристаллическая решетка – в узлах
её молекулы, между которыми слабые силы
межмолекулярного взаимодействия.
Физические свойства:
летучесть;
хрупкость в кристаллическом виде;
низкие температуры плавления и кипения;
растворимые в воде и способность проводить эл.
ток зависят от полярности связи.
Примеры веществ: газы – О2, Сl2, N2, СО2
жидкости – вода, спирты,
кислоты, Br2
твердые – нафталин, глюкоза, I2
Слайд 27Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Металлическая связь.
Образуется в металлах и сплавах.
Атомы металлов имеют неболь-
шое число валентных электронов.
Они слабо связаны с ядром и
могут легко отрываться от него.
В результате в узлах кристал-
лической решетки появляются по-
ложительно заряженные ионы, а
между ними свободно перемещаются электроны – образуется так называемый “электронный газ”. Вид связи между положительными ионами, осуществляемой за счет притяжения электронов, свободно перемещающихся по кристаллу, называется металлической.
Слайд 28Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Металлическая связь характеризуется:
ненаправленностью;
ненасыщаемостью;
меньшей прочностью по сравнению с
ковалентной и ионной.
Слайд 29Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
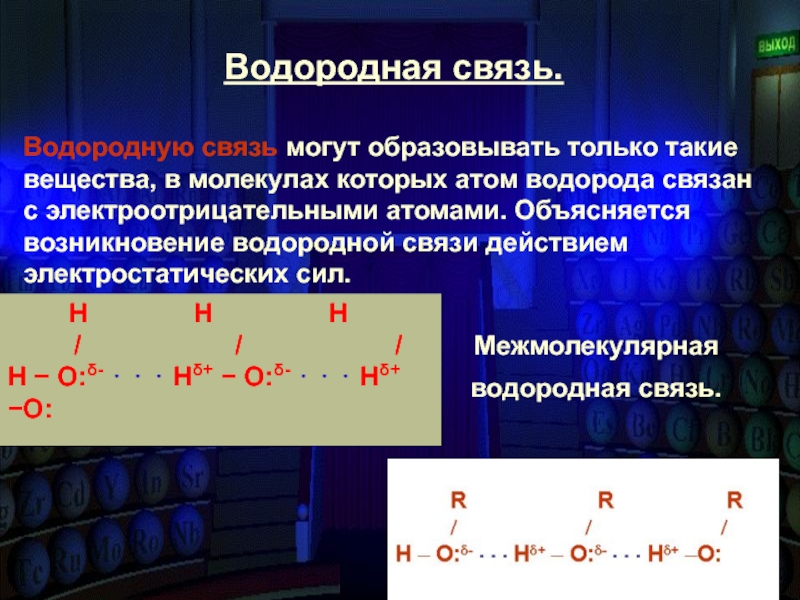
Водородная связь.
Водородную связь могут образовывать только такие вещества, в молекулах которых атом водорода связан с электроотрицательными атомами. Объясняется возникновение водородной связи действием электростатических сил.
Межмолекулярная
водородная связь.
Н Н Н
/ / /
H − O:δ- ⋅ ⋅ ⋅ Hδ+ − O:δ- ⋅ ⋅ ⋅ Hδ+ −O:
Слайд 30Аминокислоты
Синтетические
Получают кислотным гидролизом белков либо из карбоновых кислот,
Водородная связь может быть
и внутримолекулярной,
особенно часто она
проявляется в органических
веществах.
В частности у белков
вторичная структура
поддерживается
водородными связями.
Энергия водородной связи невелика и на
порядок меньше энергии ковалентной
связи, что не мешает ей оказывать
Значительное влияние на физические и
химические свойства многих веществ.
Слайд 31
Определите тип химической связи в веществах, покажите схему её образования:
Na3N CO2 CaCl2
Слайд 33 В каких из веществ присутствует донорно-акцепторный механизм образования связи?