- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии кислород
Содержание
- 1. Презентация по химии кислород
- 2. В состоянии свободном Газом он бывает, С
- 3. Джозеф Пристли Открыл кислород 1 августа 1774Пристли
- 4. В конце ХVIII в. английский ученый Джозеф
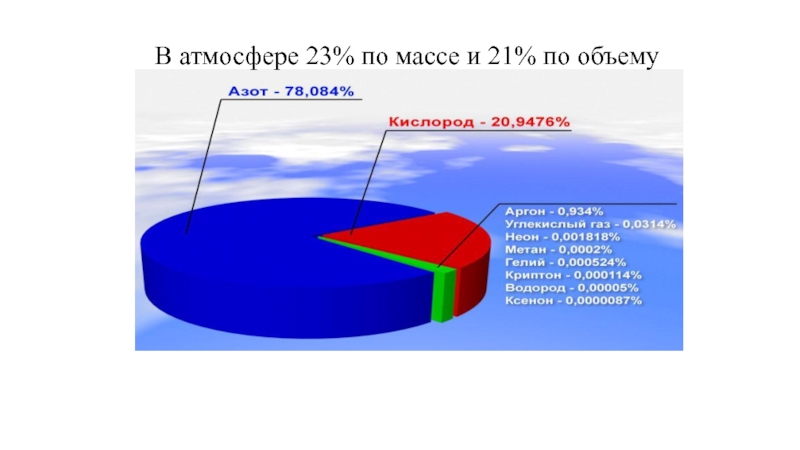
- 5. В атмосфере 23% по массе и 21% по объему
- 6. Кислород входит в составБиологически важныхмолекул, образующихживую материюКислород как элементБелкиАминокислоты и белкиуглеводыЖиры
- 7. Способы получения кислорода Разложение перманганата калия при
- 8. В лаборатории кислород получают при нагревании веществ, которые
- 9. Рефлексиясегодня я узнал...было трудно…я понял, что…я научился…я смог…было интересно узнать, что…меня удивило…мне захотелось…
В состоянии свободном Газом он бывает, С водородом и азотом Воздух составляет. Дышат птицы им и звери, и растения. Его много в атмосфере, В этом нет сомнения.
Слайд 2В состоянии свободном Газом он бывает, С водородом и азотом Воздух составляет. Дышат птицы им
и звери,
и растения.
Его много в атмосфере,
В этом нет сомнения.
Слайд 3Джозеф Пристли
Открыл кислород
1 августа 1774
Пристли направлял на
оксид ртути
солнечные
лучи с помощью
мощной линзы
лучи с помощью
мощной линзы
История открытия
2HgO=2Hg+O2
Слайд 4В конце ХVIII в. английский ученый Джозеф Пристли занимался нагреванием разных
веществ, собирая солнечные лучи при помощи увеличительного стекла. Когда он накалил оксид ртути (II) в приборе, изображенном на рисунке, выделилось много газа. Сначала Джозеф Пристли подумал, что это воздух. Но когда он опустил в сосуд с собранным газом горящую свечу, то увидел нечто необычное. «Меня поразило, — писал Джозеф Пристли, — больше, чем я мог выразить, что свеча в этом газе горела замечательно блестящим пламенем».
Джозеф Пристли поместил одну мышь в сосуд с обыкновенным воздухом, а другую в такой же сосуд с полученным им газом. Первая мышь быстро задохнулась, а вторая в это время еще чувствовала себя хорошо и оживленно двигалась. Джозеф Пристли и сам пробовал дышать полученным газом и нашел, что им дышится особенно легко и приятно.
Открытый Джозефом IIристли газ и был кислород.
Джозеф Пристли поместил одну мышь в сосуд с обыкновенным воздухом, а другую в такой же сосуд с полученным им газом. Первая мышь быстро задохнулась, а вторая в это время еще чувствовала себя хорошо и оживленно двигалась. Джозеф Пристли и сам пробовал дышать полученным газом и нашел, что им дышится особенно легко и приятно.
Открытый Джозефом IIристли газ и был кислород.
Слайд 6 Кислород входит в состав
Биологически важных
молекул, образующих
живую материю
Кислород как элемент
Белки
Аминокислоты и
белки
углеводы
Жиры
Слайд 7Способы получения кислорода
Разложение перманганата калия при нагревании:
2KMnO4 –t200
K2MnO4 + MnO2 + O2
Нагрев KMnO4 Проверка собравшегося
кислорода
Нагрев KMnO4 Проверка собравшегося
кислорода
Слайд 8В лаборатории кислород получают при нагревании веществ, которые легко разлагаются с выделением
кислорода.
1) Разложение перманганата калия
2КМnО4 → К2МnО4 + МnО2 + О2
2) разложение воды электрическим током
2Н2О → 2Н2 + О2
3) Разложение бертолетовой соли
КСlО3 → 2КСl + 3О2 (при нагревании или при действии катализатора)
4) Разложение пероксида водорода
2Н2О2 → 2Н2О + О2
1) Разложение перманганата калия
2КМnО4 → К2МnО4 + МnО2 + О2
2) разложение воды электрическим током
2Н2О → 2Н2 + О2
3) Разложение бертолетовой соли
КСlО3 → 2КСl + 3О2 (при нагревании или при действии катализатора)
4) Разложение пероксида водорода
2Н2О2 → 2Н2О + О2
Слайд 9Рефлексия
сегодня я узнал...
было трудно…
я понял, что…
я научился…
я смог…
было интересно узнать, что…
меня
удивило…
мне захотелось…
мне захотелось…