- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии 9 класс ОВР
Содержание
- 1. Презентация по химии 9 класс ОВР
- 2. ОГЭ Задание №4. Валентность и степень окисления
- 3. 3. Определите все степени окисления атома азота
- 4. Ответы:1 +4 ; -2 ; +6 ;
- 5. Определите, что происходит со степенью окисления серы
- 6. Окислительно- восстановительные реакции
- 7. ОГЭ. Задание 14. Окислительно-восстановительные реакции:Сера является окислителем
- 8. 3. В какой реакции окислителем и восстановителем
- 9. ОВРмежмолекулярные внутримолекулярные
- 10. ОГЭ. Задание 20. Окислительно-восстановительные реакцииИспользуя метод электронного
- 11. Cl2 + KOH = KCl
- 12. Алгоритм составления уравнений окислительно-восстановительных реакций
- 13. Домашняя работа:П.1 стр.7 пис.вопросы №1, 4, 7Для
- 14. Рефлексия Вопросы к ученикуПостарайся точно вспомнить то,
ОГЭ Задание №4. Валентность и степень окисления химических элементов.Определите все степени окисления у атома серы в соединениях: Низшие степени окисления азота и серы соответственно равны:
Слайд 2ОГЭ Задание №4. Валентность и степень окисления химических элементов.
Определите все степени
окисления у атома серы в соединениях:
Низшие степени окисления азота и серы соответственно равны:
Низшие степени окисления азота и серы соответственно равны:
Слайд 33. Определите все степени окисления атома азота в соединениях:
4. Атом серы
имеет отрицательную степень окисления в соединении:
5. Максимальную степень окисления хлора проявляется в соединении:
5. Максимальную степень окисления хлора проявляется в соединении:
Слайд 5Определите, что происходит со степенью окисления серы при следующих переходах:
H 2S
SO2 SO3
SO2 H2SO3 Na2SO3
SO2 H2SO3 Na2SO3
Слайд 6Окислительно- восстановительные
реакции (ОВР) –
реакции,
идущие с изменением степени окисления атомов, входящих в состав реагирующих веществ
Слайд 7ОГЭ. Задание 14.
Окислительно-восстановительные реакции:
Сера является окислителем в реакции:
H2S +I2 =S
+ 2HI
3S + 2Al = Al 2 S3
2SO2 + O2 =2SO3
SO2 является восстановителем в реакции:
SO2 + 2H2S = 3S + H2O
SO2 + 2KOH = K2SO3 + H2O
SO2 + Br2 +2H2O = H2SO4 + 2HBr
3S + 2Al = Al 2 S3
2SO2 + O2 =2SO3
SO2 является восстановителем в реакции:
SO2 + 2H2S = 3S + H2O
SO2 + 2KOH = K2SO3 + H2O
SO2 + Br2 +2H2O = H2SO4 + 2HBr
Слайд 83. В какой реакции окислителем и восстановителем служит один и тот
же элемент?
1) 2H2S + SO2 = 3S + 2H2O
2)Br2 + 2HI = I2 + 2HBr
3) 2ZnS + 3O2 = 2ZnO + 2SO2
4. В реакции C + H2O = CO + H2
изменение степени окисления окислителя соответствует схеме:
1) +2 +4
2) +1 0
3) -2 +4
1) 2H2S + SO2 = 3S + 2H2O
2)Br2 + 2HI = I2 + 2HBr
3) 2ZnS + 3O2 = 2ZnO + 2SO2
4. В реакции C + H2O = CO + H2
изменение степени окисления окислителя соответствует схеме:
1) +2 +4
2) +1 0
3) -2 +4
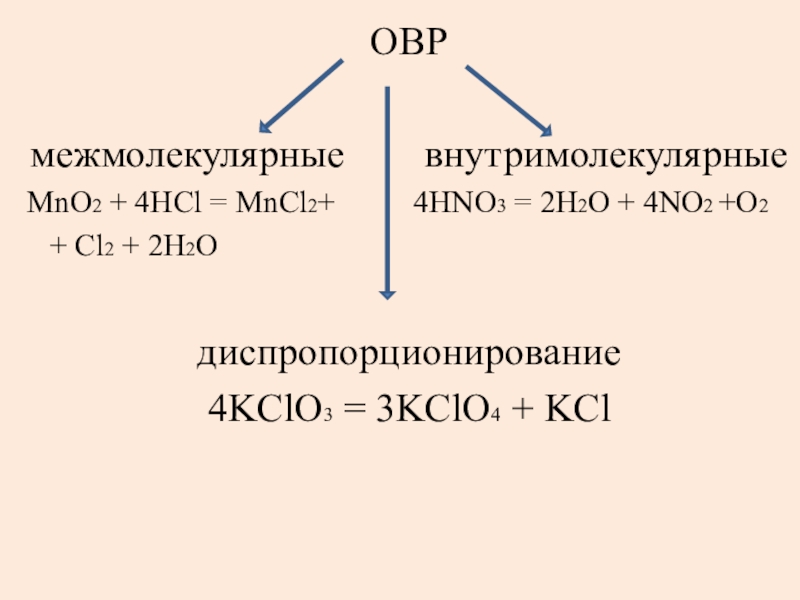
Слайд 9ОВР
межмолекулярные внутримолекулярные
MnO2 +
4HCl = MnCl2+ 4HNO3 = 2H2O + 4NO2 +O2
+ Cl2 + 2H2O
диспропорционирование
4KClO3 = 3KClO4 + KCl
+ Cl2 + 2H2O
диспропорционирование
4KClO3 = 3KClO4 + KCl
Слайд 10ОГЭ. Задание 20. Окислительно-восстановительные реакции
Используя метод электронного баланса, расставьте коэффициенты в
уравнении реакции, схема которого:
Cl2 + KOH = KCl + KCLO3 + H2O
Определите окислитель и восстановитель.
Cl2 + KOH = KCl + KCLO3 + H2O
Определите окислитель и восстановитель.
Слайд 11 Cl2 + KOH = KCl + KCLO3 + H2O
Алгоритм составление уравнений окислительно-восстановительных реакций (методом электронного баланса):
1)
2)
3)
4) …
1)
2)
3)
4) …
Слайд 12 Алгоритм составления уравнений окислительно-восстановительных реакций (методом электронного баланса)
1. Записать
схему реакции.
2. Определить степень окисления атомов до и после реакции.
3. Выписать знаки химических элементов, которые меняют степень окисления.
4. Составить электронные уравнения (сбалансировать заряды, показать процесс отдачи и присоединения электронов).
5. Определить коэффициенты при окислителе и восстановителе.
6. Составить окончательное уравнение.
2. Определить степень окисления атомов до и после реакции.
3. Выписать знаки химических элементов, которые меняют степень окисления.
4. Составить электронные уравнения (сбалансировать заряды, показать процесс отдачи и присоединения электронов).
5. Определить коэффициенты при окислителе и восстановителе.
6. Составить окончательное уравнение.
Слайд 13Домашняя работа:
П.1 стр.7 пис.вопросы №1, 4, 7
Для повышенного уровня
сайт «Решу
ОГЭ» задания № 4,14 и 20
(по пять примеров)
(по пять примеров)
Слайд 14Рефлексия
Вопросы к ученику
Постарайся точно вспомнить то, что слышал на уроке
и ответь на поставленные вопросы:
1Какова была тема урока?
2Какая цель стояла перед тобой на уроке?
3Как работали на уроке твои одноклассники?
4Как работал ты на уроке?
5Сегодня я узнал…
6Я удивился…
7Теперь я умею…
8Я хотел бы…
1Какова была тема урока?
2Какая цель стояла перед тобой на уроке?
3Как работали на уроке твои одноклассники?
4Как работал ты на уроке?
5Сегодня я узнал…
6Я удивился…
7Теперь я умею…
8Я хотел бы…