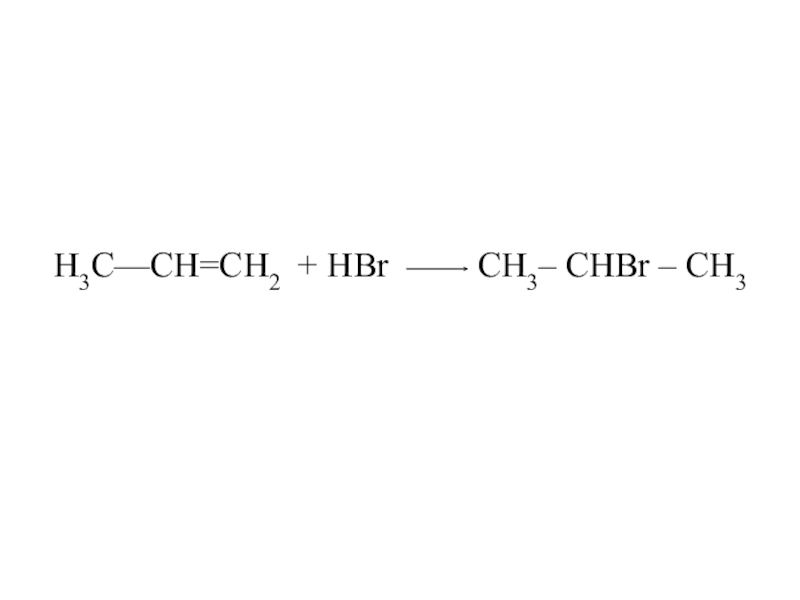- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад к уроку Непредельные углеводороды
Содержание
- 1. Презентация к уроку Непредельные углеводороды
- 2. Алкены, или олефины, этиленовые — непредельные углеводороды,
- 3. Алкены образуют гомологический ряд с общей формулой CnH2n
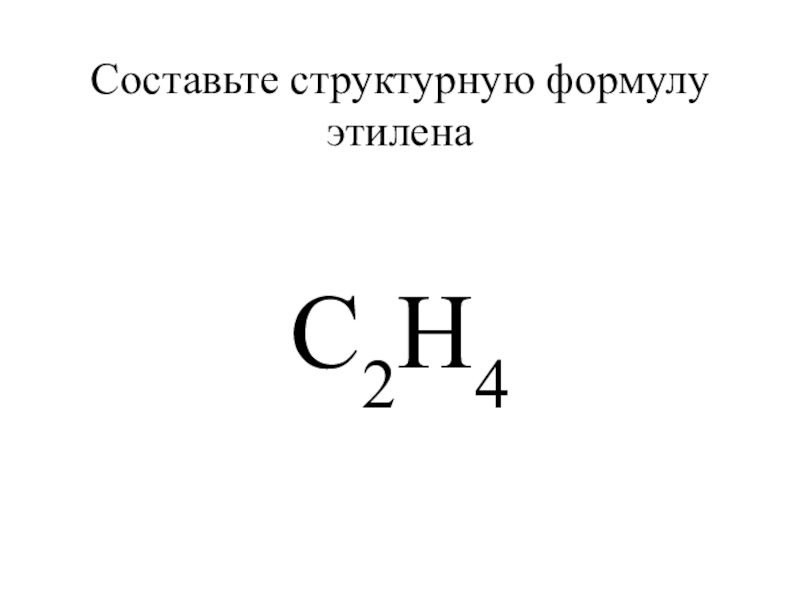
- 4. Составьте структурную формулу этиленаС2Н4
- 5. H
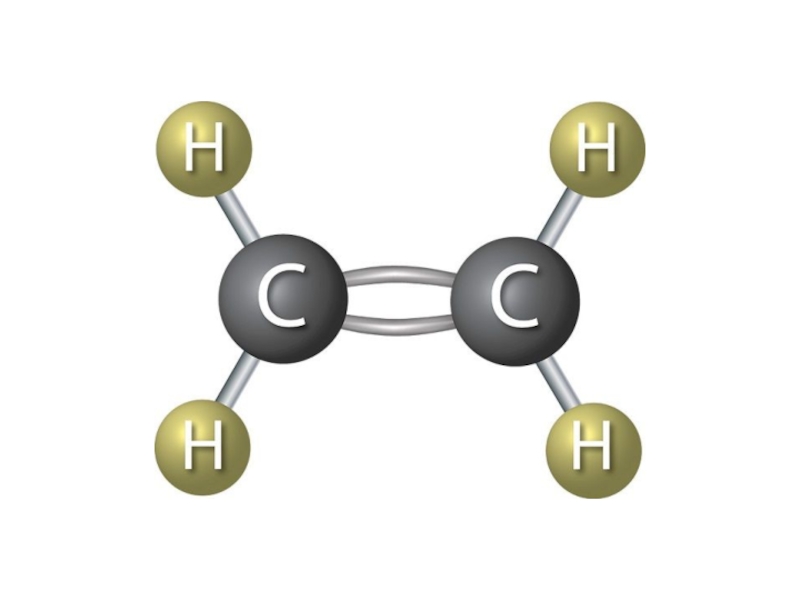
- 6. Собрать шаростержневую модель молекулы этилена
- 7. Слайд 7
- 8. Изомерия углеродного скелета положение двойной связи
- 9. Изомерия углеродного скелета CH3-CH=CH-CH2-CH3 CH3–C=CH-CH3 CH
- 10. Положение двойной связиCH 2= CH – CH2
- 11. Номенклатура
- 12. Собрать шаростержневую модель молекулы бутена – 1 и его изомера. Дать ему название.
- 13. Получение алкенов1. крекинг или пиролиз нефти2. крекинг
- 14. 4. из спиртов
- 15. 5.Дегидрированием алканов
- 16. Физические свойства С2H4 до C4H8
- 17. Химические свойства Присоединение водорода (гидрирование) Н2С=СН2 + H2 → Н3С—СН3
- 18. Химические свойства Присоединение галогенов (галогенирование) Н2С=СН2 + Cl2 → Cl−H2C—CH2−Cl
- 19. Химические свойства Присоединение галогеноводородов H2С=СН2 + НВr → Н3С—CH2Вr
- 20. Как пойдёт присоединение бромоводорода к гомологам этилена
- 21. H3C—CH=CH2 + НВr CH3– CHBr – CH3
- 22. Химические свойства Присоединение воды (реакция гидратации)H3C—CH=CH2 +
- 23. Химические свойства Горение Н2С=СН2 + 3O2 → 2СO2 + 2Н2O
- 24. Химические свойства Действие на этилен водного раствора
- 25. Химические свойства Реакция полимеризацииСH2=CH2 + CH2=CH2 + CH2=CH2 + … CH2-CH2-CH2-CH2-CH2-CH2-…
- 26. Выводы по урокуАлкены – непредельные углеводороды, в
- 27. Выводы по урокуДля алкенов характерны: изомерия углеродной
- 28. Выводы по урокуАлкены обладают большой химической активностью.
- 29. Домашнее задание: § 33, упражнения № 3,5
Алкены, или олефины, этиленовые — непредельные углеводороды, в молекулах которых между углеродными атомами имеется одна двойная связь.
Слайд 2Алкены, или олефины, этиленовые — непредельные углеводороды, в молекулах которых между
углеродными атомами имеется одна двойная связь.
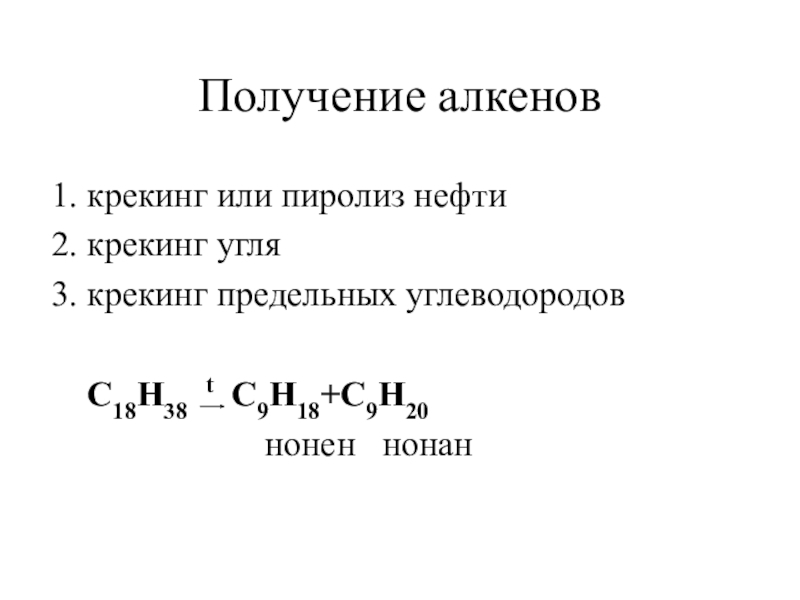
Слайд 13Получение алкенов
1. крекинг или пиролиз нефти
2. крекинг угля
3. крекинг предельных углеводородов
C18H38 t C9H18+C9H20
нонен нонан
нонен нонан
Слайд 16Физические свойства
С2H4 до C4H8 - газы
C5 H10
до C18H36 - жидкости
C19H38 и т.д. – твердые вещества.
С ростом числа атомов углерода возрастает tкип, tпл и плотность. Все алкены плохо растворяются в воде
C19H38 и т.д. – твердые вещества.
С ростом числа атомов углерода возрастает tкип, tпл и плотность. Все алкены плохо растворяются в воде
Слайд 20Как пойдёт присоединение бромоводорода к гомологам этилена несимметричного строения, например к
пропилену?
Правило Морковникова:
Атом водорода присоединяется к наиболее гидрированному атому углерода
Слайд 22Химические свойства
Присоединение воды (реакция гидратации)
H3C—CH=CH2 + H—OH → H3C—CH—CH3
|
OH
OH
Слайд 24Химические свойства
Действие на этилен водного раствора КМnO4
3H2C=CH2 + 2KMnO4
+ 4H2O → 3HOCH2—CH2OH + 2MnO2 + KOH
Слайд 25Химические свойства
Реакция полимеризации
СH2=CH2 + CH2=CH2 + CH2=CH2 + …
CH2-CH2-CH2-CH2-CH2-CH2-…
Слайд 26Выводы по уроку
Алкены – непредельные углеводороды, в молекулах которых имеется одна
двойная связь. Общая формула – СnH2n. В названии алкенов используется суффикс –ен.
Слайд 27Выводы по уроку
Для алкенов характерны: изомерия углеродной цепи, изомерия положения двойной
связи, пространственная (геометрическая) и изомерия между классами.
Слайд 28Выводы по уроку
Алкены обладают большой химической активностью. За счёт наличия кратной
связи алкены вступают в реакции присоединения, окисления, полимеризации.