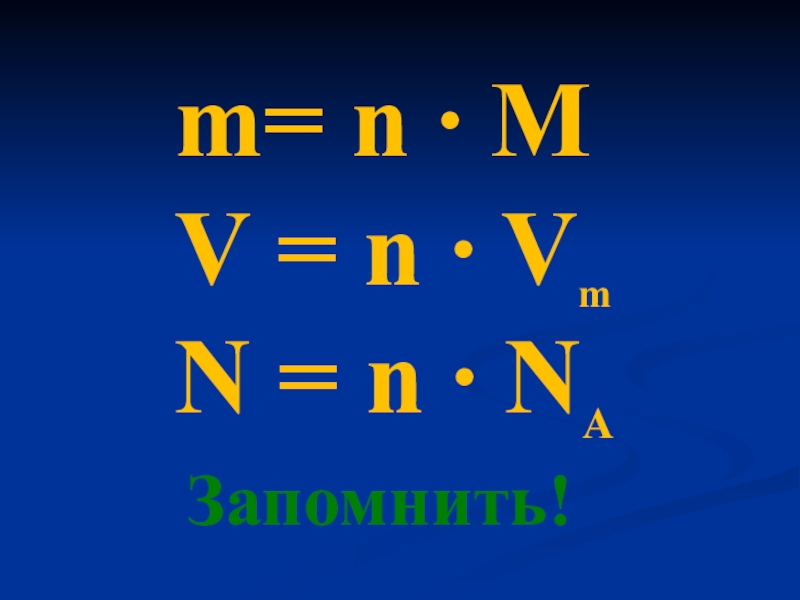- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Открытый урок по химии
Содержание
- 1. Открытый урок по химии
- 2. 1/«Я буду проявлять инициативу» 2/«Я готов( а) к сотрудничеству»3/«Я буду самостоятельно принимать решения»
- 3. Тип урока: закрепление материала.Вид урока:
- 4. m= n ∙ MV = n∙ Vm N = n ∙ NA
- 5. Обозначение: ν (ню), или nЕдиница измерения: мольКоличество вещества
- 6. [ Mr = M ]Mr(H2O)= 18M(H2O)= 18
- 7. 1 моль любого газа (н.у.) занимает объем 22,4 лVM = 22,4л/моль
- 8. Число частиц в одном моль веществаназывается числом Авогадро (NА)NА = 6,02 ∙1023 1/моль
- 9. Задача. Найти массу 3 моль атомов серыn(S)
- 10. Направление №1: m= n ∙ M Рассчитайте массу кислорода (O2) количеством вещества 0,25 моль.
- 11. Направление №2. V = n ∙ Vm Рассчитайте объем (н.у.) азота N2 количеством вещества 0,5 моль.
- 12. 1 моль вещества – 6,02∙1023частицСколько частиц содержат
- 13. Направление №3: N = n ∙ NA.Рассчитайте число молекул 5 моль углекислого газа CO2.
- 14. 1.В периодической системе найдите элемент, образующий вещество,
- 15. ?Можно ли найти число частиц в
- 16. Сколько ложек сахарного песка вы кладете в
- 17. Что тяжелее: 1
- 18. Рефлексия
- 19. m= n ∙ MV = n ∙ VmN = n ∙ NAЗапомнить!
- 20. Цель достигнута?
- 21. Спасибо за внимание!
1/«Я буду проявлять инициативу» 2/«Я готов( а) к сотрудничеству»3/«Я буду самостоятельно принимать решения»
Слайд 1
Улыбнись Новому Дню!
Максимова Маргарита Викторовнна
МБОУ «Новобуяновская
СОШ» Янтиковского района Чувашской Республики,
учитель
химии,
1 квалификационная категория.
1 квалификационная категория.
Слайд 21/«Я буду проявлять инициативу»
2/«Я готов( а) к сотрудничеству»
3/«Я буду самостоятельно
принимать решения»
Слайд 3
Тип урока:
закрепление материала.
Вид урока:
урок-путешествие.
Цель: закрепить умения решать задачи с использованием изученных формул и понятий.
Цель: закрепить умения решать задачи с использованием изученных формул и понятий.
Количественные отношения в химии.
Количество вещества.
Моль.
Молярная масса.
Слайд 6[ Mr = M ]
Mr(H2O)= 18
M(H2O)= 18 г/моль
Молярная масса (М) –
это суммарная масса всех частиц, входящих в 1 моль вещества.
Слайд 9Задача.
Найти массу 3 моль атомов серы
n(S) = 3моль
M(S) = 32
г/моль
Найти m(S)
Найти m(S)
Решение
m = n ∙ M
m = 3 ∙ 32 = 96 (г)
Ответ: m(S) = 96 г
Слайд 121 моль вещества – 6,02∙1023частиц
Сколько частиц содержат
3 моль вещества?
Сколько частиц
содержат
0,5 моль вещества?
0,5 моль вещества?
3 ∙ 6,02∙1023 = 18,06∙1023
0,5 ∙ 6,02∙1023 = 3,01∙1023
Слайд 141.В периодической системе найдите элемент, образующий вещество, которое поддерживает горение.
(6 группа, 2 период)
2.Переведите взгляд вниз и влево, на элемент, который образует металл, содержащееся в градусниках.
(2 группа 6 период).
3. Переведите взгляд вправо и вверх, на элемент с относительной атомной массой 35, 5 (7 группа, 3 период).
4. Переведите взгляд вниз и влево, на элемент, который образует драгоценный металл желтого цвета.
(1 группа, 6 период).
2.Переведите взгляд вниз и влево, на элемент, который образует металл, содержащееся в градусниках.
(2 группа 6 период).
3. Переведите взгляд вправо и вверх, на элемент с относительной атомной массой 35, 5 (7 группа, 3 период).
4. Переведите взгляд вниз и влево, на элемент, который образует драгоценный металл желтого цвета.
(1 группа, 6 период).
Гимнастика
Гимнастика для глаз
Слайд 16Сколько ложек сахарного песка
вы кладете в чашку чая?
Рассчитайте:
какое количество
сахарозы
вы выпиваете с чаем;
2) сколько молекул сахарозы (C12H22O11)
содержится в этом количестве, если
в 1 чайной ложке
примерно 5 г сахарозы.
вы выпиваете с чаем;
2) сколько молекул сахарозы (C12H22O11)
содержится в этом количестве, если
в 1 чайной ложке
примерно 5 г сахарозы.
Слайд 17 Что тяжелее:
1 моль атомов кислорода
или 1 моль атомов фосфора?
Почему?
M(O) = 16 г/моль
M(P) = 31 г/моль



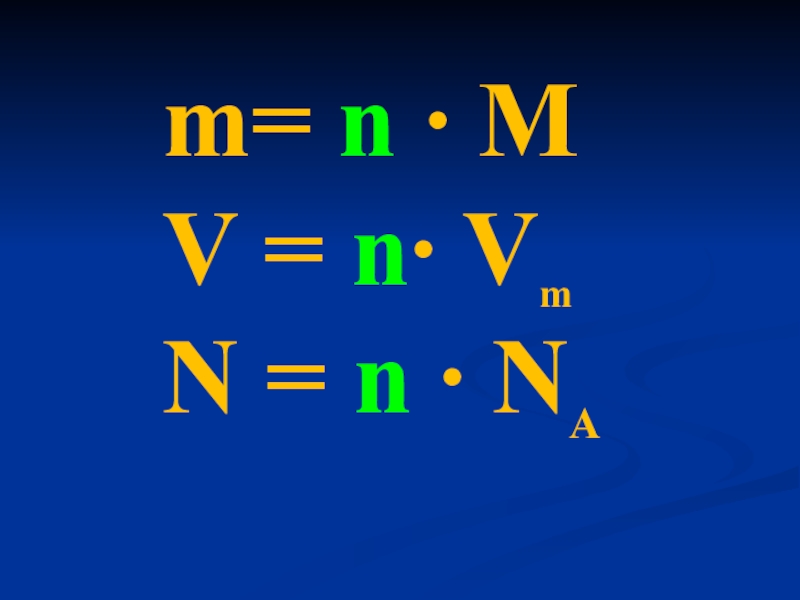

![Открытый урок по химии [ Mr = M ]Mr(H2O)= 18M(H2O)= 18 г/мольМолярная масса (М) – [ Mr = M ]Mr(H2O)= 18M(H2O)= 18 г/мольМолярная масса (М) – это суммарная масса всех частиц, входящих](/img/tmb/3/288771/a74b2b58c0154585ed882d667164208f-800x.jpg)