- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Оксиды
Содержание
- 1. Оксиды
- 2. 1. Сформировать представления об оксидах, их
- 3. В нашу лабораторию пришел заказ:
- 4. 1. Оксиды- это простые или сложные вещества?2.
- 5. Внимание, внимание! Пришло
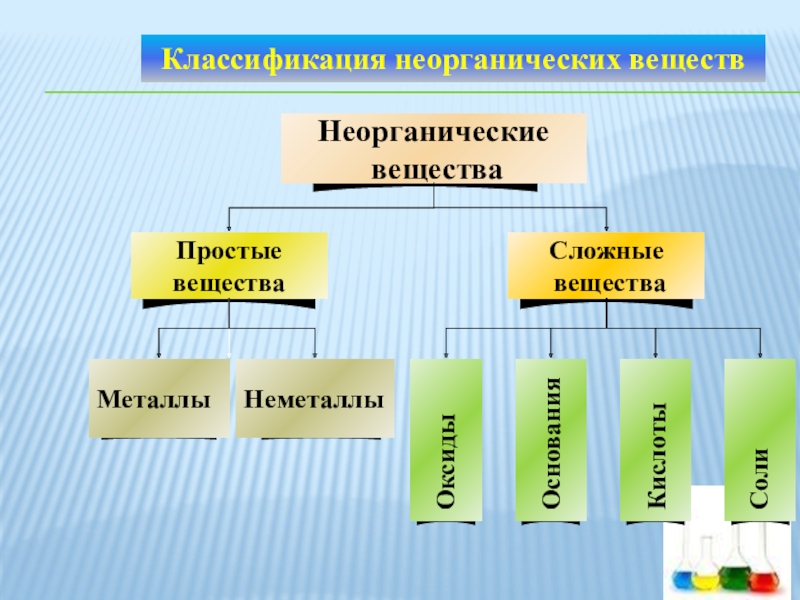
- 6. Оксиды - этосложные вещества,состоящие из двух элементов,
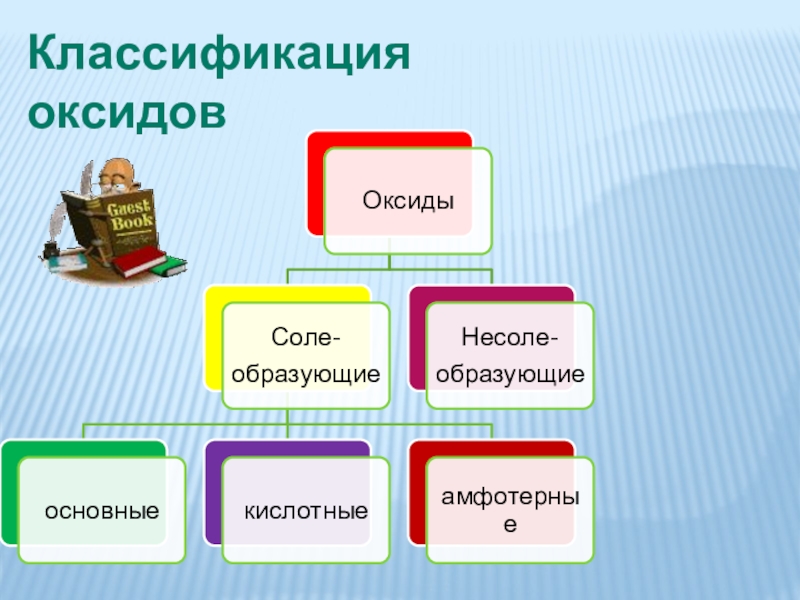
- 7. Классификация оксидов
- 8. НесолеобразующиеоксидыЭто оксиды, которые не взаимодействуют ни с
- 9. Основные оксидыЭто оксиды, которым в качестве гидроксидов
- 10. Кислотные оксидыЭто оксиды, которым в качестве гидроксидов
- 11. Амфотерные Оксиды. Это оксиды, которым соответствуют гидроксиды,
- 12. В нашу лабораторию пришло ещё одно письмо:
- 13. Молодцы, ребята! Вы сегодня хорошо поработали! И
Слайд 2 1. Сформировать представления об оксидах, их составе и классификации.
2.
3. Выяснить основные свойства оксидов.
4. Закрепить умения определять валентность элементов в соединении, составлять формулы бинарных соединений, давать названия веществам.
5. Приобрести и закрепить новые умения по изучению веществ, составлению уравнений химических реакций.
Задачи урока :
Слайд 3 В нашу лабораторию пришел заказ: «Изучить и дать конкретные
По накладной мы получили восемь склянок и этикетки с названиями, вложенные в эти пробирки. Выньте таблички, прочитайте название, перепишите формулы в тетрадь.
Сравните, что общего и чем отличаются формулы этих
веществ друг от друга. Попробуйте распределить их на две
группы. Какой признак вы взяли за основной?
Опишите агрегатное состояние при обычных условиях каждого оксида.
CuO
P2O5
Fe2O3
СаО
SiO2
Н2О
AL2O3
CO2
Слайд 41. Оксиды- это простые или сложные вещества?
2. Сколько элементов входит в
3. На какие две основные группы можно раз-
делить оксиды?
4. Какова валентность кислорода в соединении?
Как вы думаете, почему оксиды неметаллов называются кислотными, а оксиды металлов – основными?
Если вам, друзья-лаборанты, трудно ответить на этот вопрос, вам поможет разобраться в этом найденное письмо.
Сделайте выводы :
Слайд 5 Внимание, внимание! Пришло задание! Друзья - научные
Не забудьте соблюдать правила техники безопасности!
Ход работы:
Возьмите пробирки с водой. Поместите в них небольшие порции веществ.
2.Размешайтестеклянными палочками. Что наблюдаете?
3. Во все пробирки добавьте по 2-3 капли лакмуса. Свойства каких сред – кислотных или основных – они проявляют?
Слайд 6Оксиды - это
сложные вещества,
состоящие из двух
элементов, один из
которых кислород.
Например:
Al2O3, CO.
Слайд 8Несолеобразующие
оксиды
Это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями
CO, NO, N2O, SiO.
Солеобразующие
оксиды
Это оксиды, которые взаимодействуют с кислотами или со щелочами с образованием солей и воды: N2O5, CO2, CaO, Na2O.
Слайд 9Основные оксиды
Это оксиды, которым в качестве гидроксидов
соответствуют основания.
Например: CuO →
Основные оксиды образуют только металлы со степенью
окисления +1, +2.
Например: Na2O, K2O, CaO, MgO, CuO, CrO.
Исключение BeO, ZnO, SnO, PbO.
Слайд 10Кислотные оксиды
Это оксиды, которым в качестве гидроксидов соответствуют кислоты.
Например:
Кислотные оксиды образуют все неметаллы в любой степени окисления, исключая несолеобразующие оксиды, и металлы со степенью окисления +5 и выше.
Например: CO2, N2O5, SiO2,
Mn2O7, CrO3.
Слайд 11Амфотерные
Оксиды.
Это оксиды, которым соответствуют гидроксиды, проявляющие свойства как оснований,
Например:
BeO → Be(OH)2 → H2BeO2
ZnO → Zn(OH)2 → H2ZnO2
Амфотерные оксиды образуют только металлы со степенью окисления +3, +4.
Например: Cr2O3, Fe2O3, Al2O3.
Оксиды BeO, ZnO , SnO, PbO также являются амфотерными.
Слайд 12В нашу лабораторию пришло ещё одно письмо:
Здравствуйте, здравствуйте!
Не
С уважением Иванов.
4AI + 3O2 = 2AI2O3( оксид алюминия)
Слайд 13Молодцы, ребята! Вы сегодня хорошо поработали! И на последок, для закрепления материала
Два элемента в них всего-
Кислород важней всего!
***
Мы - весёленький народ
Элемент и кислород,
В формулах оксидов
Главные два вида.
***
Узнай меня! Я газ. Я прост.
Я рыжий, словно лисий хвост.
***
Чтоб появиться я сумел,
Прокаливают белый мел,
Меня дает огонь в печи
И пламя маленькой свечи
И стоит только сделать вдох,
Чтоб я на свет явиться смог.
Единственное вещество в природе, которое в земных условиях существует во всех трех агрегатных состояниях: жидком, твердом и газообразном.
***