- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Обобщающий урок по теме Металлы
Содержание
- 1. Обобщающий урок по теме Металлы
- 2. Общие физические свойства металловПластичность – способность изменять
- 3. Общие химические свойства металлов Сильные восстановителиС простыми
- 4. Коррозия металлов
- 5. А) кислотными оксидами; Б) основаниями;В) кислотами.
- 6. А. CaOБ. Fe3O4В.NaHCO3Г. NaClД.Al 2O3Е. CaCO3
- 7. Ответы:Ответы:
- 8. Зачем нужны металлы?
- 9. Не сразу в дом пришел металл, Не
- 10. железо
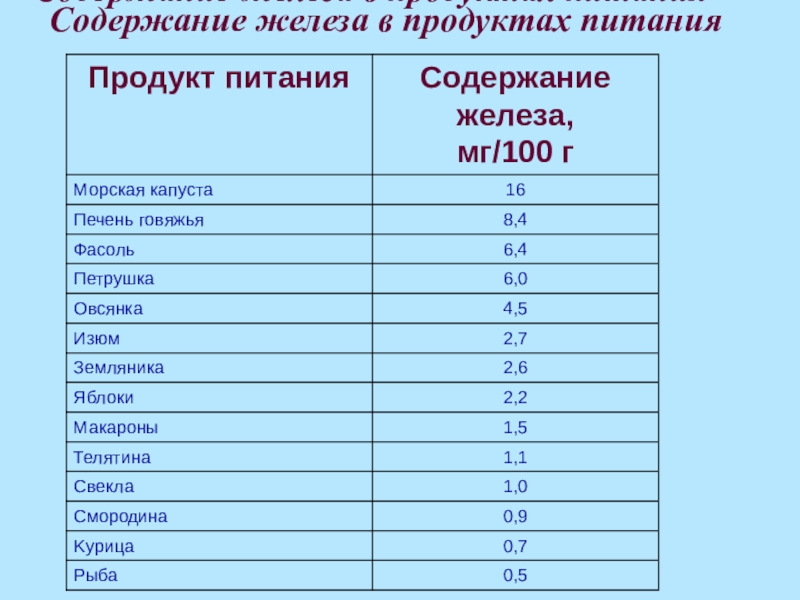
- 11. Содержание железа в продуктах питанияСодержание железа в продуктах питания
- 12. медь
- 13. ртуть
- 14. серебро
- 15. золото
Слайд 2Общие физические свойства металлов
Пластичность – способность изменять свою форму при ударе,
Электропроводность – при нагревании уменьшается (колебание ионов Физические свойства объясняются особым строением кристаллической решетки (свободные электроны – «электронный газ») затрудняется движение электронов)
Теплопроводность – закономерность та же. За счет движения свободных электронов быстрое выравнивание температуры в массе металла
Металлический блеск – хорошо отражают световые лучи.
Плотность – самый легкий литий, самый тяжелый - осмий
Температура плавления, °С – цезий (28,6), галлий (30) – плавятся на ладони руки, вольфрам (3410)
Твердость – самый твердый – хром (режет стекло), самые мягкие – калий, рубидий, цезий (легко режутся ножом).
Слайд 3Общие химические свойства металлов
Сильные восстановители
С простыми веществами
С кислородом (оксиды, пероксиды,)
С галогенами
С азотом (нитриды)
С фосфором (фосфиды)
С водородом (гидриды)
Со сложными веществами
С кислотами:
МЕ + кислота = соль + водород
(не брать конц. азотную и серную кислоты, металлы после водорода в ряду напряжений металлов)
2. С водой
а) активные металлы – гидроксиды и водород
б) металлы средней активности – оксиды и водород (при нагревании)
в) неактивные металлы – не реагируют
3. С солями – более активный металл вытесняет менее активный из его соли