УИОП городского округа Красногорск
Беличенко Анастасии, Гринько Дарьи, Самбатовой Натальи
Руководитель работы:
Семидетова Елизавета Юрьевна.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Нерастворимые основания. Получение. Окраска.
Содержание
- 1. Нерастворимые основания. Получение. Окраска.
- 2. ЦельПродемонстрировать внешний вид нерастворимых оснований.
- 3. ЗадачиПодобрать необходимые реактивы: растворы солей металлов, щелочь;Провести
- 4. Получение Co(OH)₂CoSO₄+2NaOH→Co(OH)₂↓+Na₂SО₄Осадок серо-синего цвета
- 5. Получение Fe(OH)₂FeSO₄+2NaOH→Fe(OH)₂↓+Na₂SO₄Осадок грязно-зеленого цвета
- 6. Получение Fe(OH)₃FeCl₃+3NaOH→Fe(OH)₃↓+3NaClОсадок ярко-бурого цветаизбыток
- 7. Получение Cu(OH)₂CuSO₄+2NaOH→Cu(OH)₂↓+Na₂SO₄Осадок синего цвета
- 8. Получение Zn(OH)₂ZnCl₂+2NaOH→Zn(OH)₂↓+2NaClизбытокОсадок белого цвета
- 9. Получение Mn(OH)₂MnSO₄+2NaOH→Mn(OH)₂↓+Na₂SO₄Осадок кремово-белого цвета (ванильный)
- 10. Получение Pb(OH)₂Pb(NO₃)₂+2NaOH→Pb(OH)₂↓+2NaNO₃Осадок белого цветаизбыток
- 11. Получение Ni(OH)₂NiSO₄+2NaOH→Ni(OH)₂↓+Na₂SO₄Осадок зеленого (мятного) цвета
- 12. Получение Сr(OH)₃CrCl₃ +3NaOH→Сr(OH)₃↓+3NaClОсадок серо-зеленого цвета (болотный)избыток
- 13. Получение Al(OH)₃AlCl₃ +3NaOH→Al(OH)₃↓+3NaCl Осадок белого цветаизбыток
- 14. Получение Mg(OH)₂MgCl₂+2NaOH→Mg(OH)₂↓+2NaClОсадок белого цвета
- 15. Слайд 15
- 16. Источники информацииН.Л.Глинка Общая химия. М.; «Химия»,1965.Р.А.Лидин и
ЦельПродемонстрировать внешний вид нерастворимых оснований.
Слайд 3Задачи
Подобрать необходимые реактивы: растворы солей металлов, щелочь;
Провести опыты по осаждению нерастворимых
оснований;
Найти в литературе описание нерастворимых оснований;
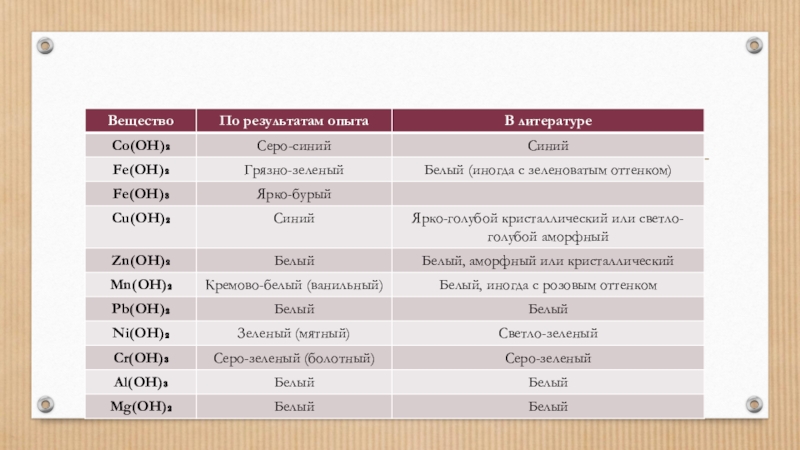
Сравнить нерастворимые основания, полученные опытным путем, с их описанием в латературе.
Найти в литературе описание нерастворимых оснований;
Сравнить нерастворимые основания, полученные опытным путем, с их описанием в латературе.
Слайд 16Источники информации
Н.Л.Глинка Общая химия. М.; «Химия»,1965.
Р.А.Лидин и др. Химические свойства неорганических
веществ.М.;Химия,1996.
П.И. Воскресенский Техника лабораторных работ. «Химия», Ленинградское отделение. 1970.
П.И. Воскресенский Техника лабораторных работ. «Химия», Ленинградское отделение. 1970.