- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Ионы и их образование
Содержание
- 1. Ионы и их образование
- 2. Учащиеся должны:-понимать, что для заполнения своей внешней
- 3. Атомы благородных газов имеют завершенный
- 4. Атомы других элементов пытаются приобрести конфигурацию ближайшего
- 5. Ионы- заряженные частицы, которые образуются в результате
- 6. Слайд 6
- 7. Ионы (по знаку заряда)Катионы - положительно заряженные частицыАнионы - отрицательно заряженные частицы
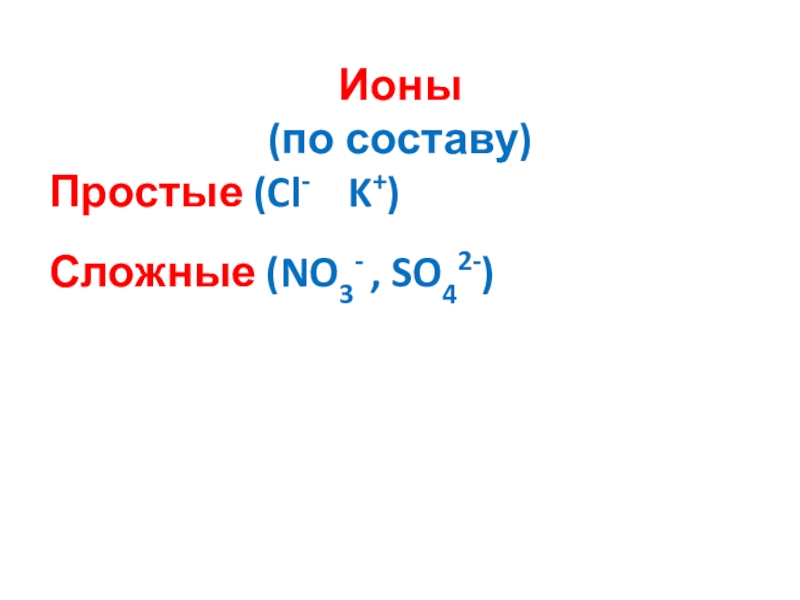
- 8. Ионы (по составу)Простые (Cl- K+)Сложные (NO3- , SO42-)
- 9. Атомы – одинаковое число протонов и электронов,
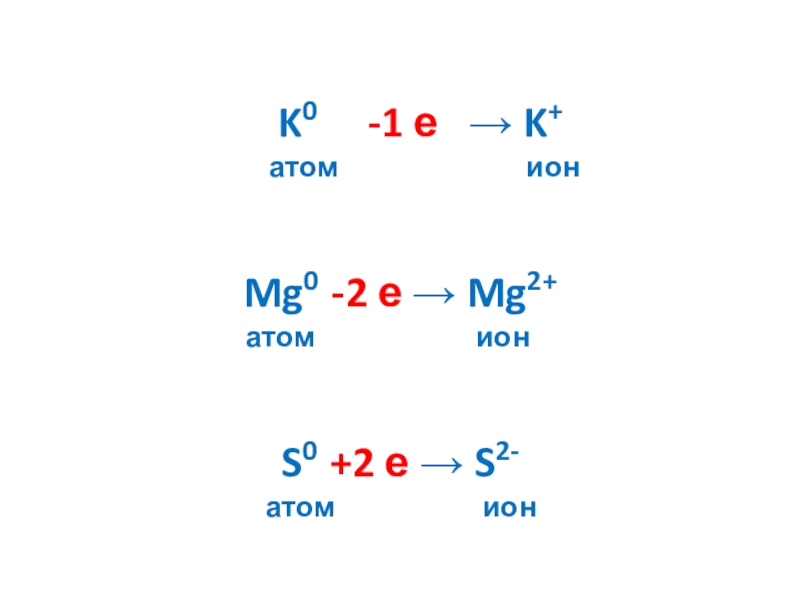
- 10. K0 -1 е
- 11. Кальций – это элемент главной подгруппы II
- 12. Хлор – это элемент главной подгруппы VII
- 13. Задание:Какие из перечисленных атомов и ионов имеют
- 14. Задание:А) натрий теряет электрон, показать конфигурацию образовавшегося
Учащиеся должны:-понимать, что для заполнения своей внешней оболочки атомы могут присоединять или отдавать электроны, в результате этого образуется ион
Слайд 2Учащиеся должны:
-понимать, что для заполнения своей внешней оболочки атомы могут присоединять
или отдавать электроны, в результате этого образуется ион
Слайд 3 Атомы благородных газов имеют завершенный внешний энергетический уровень.
Он наиболее устойчив и стабилен, что является причиной инертности атомов благородных газов.
Слайд 4Атомы других элементов пытаются приобрести конфигурацию ближайшего благородного газа и перейти
в наиболее устойчивое состояние.
Такое состояние атомы приобретают, взаимодействуя между собой, в результате между ними возникает химическая связь.
Такое состояние атомы приобретают, взаимодействуя между собой, в результате между ними возникает химическая связь.
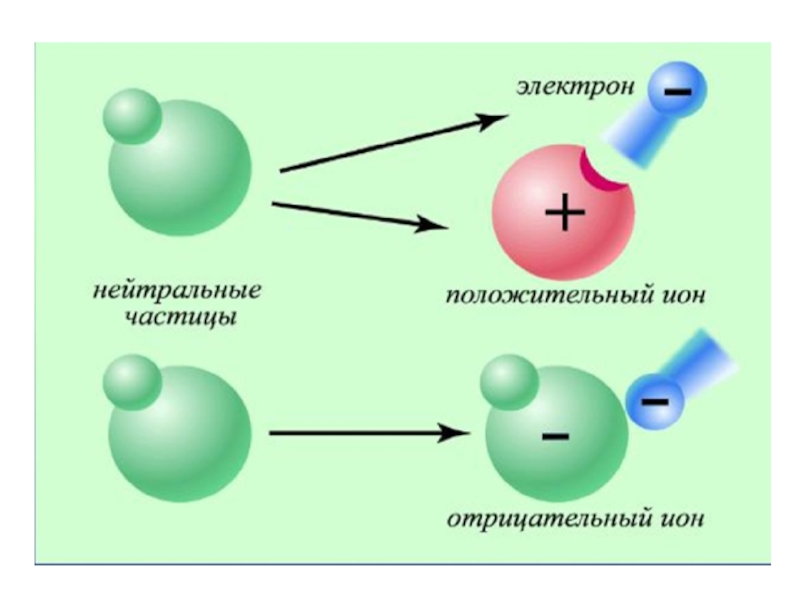
Слайд 5Ионы- заряженные частицы, которые
образуются в результате
присоединения или отдачи электронов.
Если
электроны отдаются, то ион
заряжается положительно.
Если электроны присоединяются,
то ион заряжается отрицательно.
заряжается положительно.
Если электроны присоединяются,
то ион заряжается отрицательно.
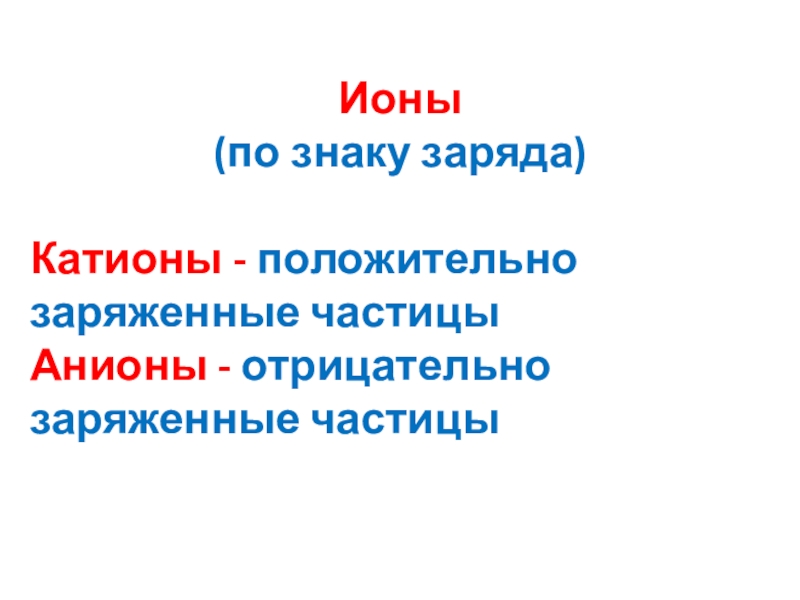
Слайд 7Ионы
(по знаку заряда)
Катионы - положительно заряженные частицы
Анионы - отрицательно заряженные
частицы
Слайд 9Атомы – одинаковое число протонов и электронов, атом нейтрален
Na0 – 1s22s22p63s1
Mg0
– 1s22s22p63s2
Cl0 – 1s22s22p63s23p5
Ионы – разное число протонов и
электронов
Na+ – 1s22s22p63s0
Mg2+ – 1s22s22p63s0
Cl- – 1s22s22p63s23p6
Cl0 – 1s22s22p63s23p5
Ионы – разное число протонов и
электронов
Na+ – 1s22s22p63s0
Mg2+ – 1s22s22p63s0
Cl- – 1s22s22p63s23p6
Слайд 11Кальций – это элемент главной подгруппы II группы, металл. Его атому
легче отдать два внешних электрона, чем принять недостающие шесть:
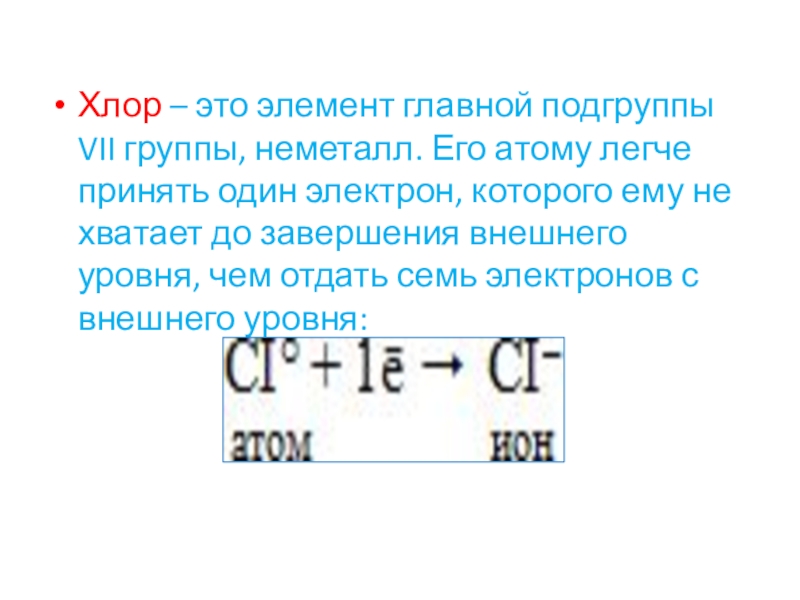
Слайд 12Хлор – это элемент главной подгруппы VII группы, неметалл. Его атому
легче принять один электрон, которого ему не хватает до завершения внешнего уровня, чем отдать семь электронов с внешнего уровня:
Слайд 13Задание:
Какие из перечисленных атомов и ионов имеют электронные конфигурации, одинаковые с
атомом 18Ar:
Ca2+, Cl-, K, Na+, S2-, As3-, Al3+
Ca2+, Cl-, K, Na+, S2-, As3-, Al3+
Слайд 14Задание:
А) натрий теряет электрон, показать конфигурацию образовавшегося иона, написать символ иона
В)
хлор получает электрон, показать конфигурацию образовавшегося иона, написать символ иона
С) кальций теряет два электрона, показать конфигурацию образовавшегося иона, написать символ иона
С) кальций теряет два электрона, показать конфигурацию образовавшегося иона, написать символ иона