- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Гидролиз солей
Содержание
- 1. Гидролиз солей
- 2. Гидролизом соли называется взаимодействие ионов соли с
- 3. Слайд 3
- 4. ОКРАСКА ЛАКМУСОВОЙ БУМАГИ В РАЗЛИЧНЫХ СРЕДАХ
- 5. Слайд 5
- 6. Механизм гидролиза карбоната натрияH2O H+ + OH-Na2CO3
- 7. CO32- +HOH HCO3- +OH- Na2CO3 +H2O
- 8. Схема гидролиза карбоната натрияNa2CO3
- 9. FeCl2 ↔ Fe2+ + 2Cl-Fe2+ + H2O
- 10. Механизм гидролиза хлорида алюминия H2O H+ +
- 11. Al3+ + HOH AlOH2+ + H+
- 12. Схема гидролиза хлорида алюминия
- 13. 4. Соли, образованные катионом сильного основания и
- 14. Механизм гидролиза хлорида натрияH2O H+ + OH-NaСl
- 15. NaCl + Н2О = Сформулируем вывод: Раствор соли, образованной__________________, имеет________________________реакцию, так как в растворе__________________________________.
- 16. Схема гидролиза карбоната натрияNaCl
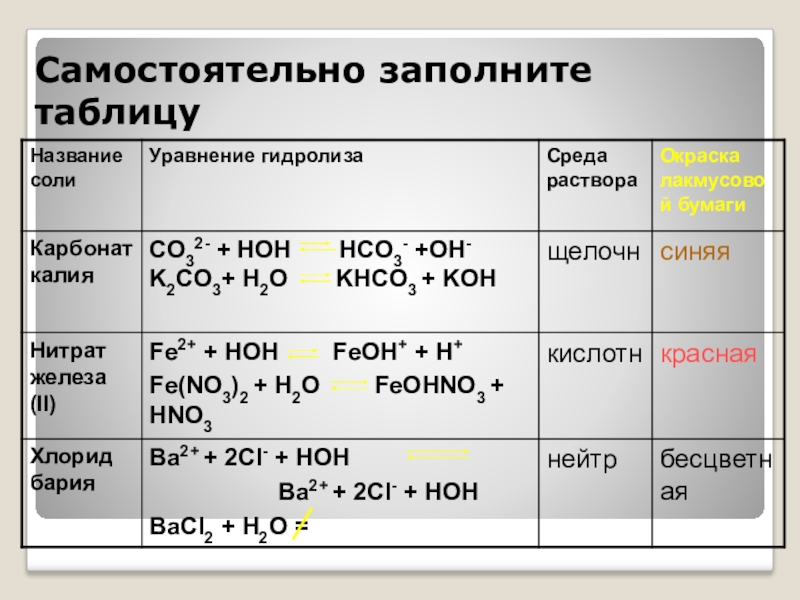
- 17. Самостоятельно заполните таблицу
- 18. Самостоятельно заполните таблицу
- 19. Количественной характеристикой гидролиза является
- 20. Для большинства солей гидролиз
Слайд 2
Гидролизом соли называется взаимодействие ионов соли с водой,
в результате которого изменяется
В процессе гидролиза соли в водном растворе появляется избыток катионов Н+ или анионов ОН-
ГИДРОЛИЗ – это реакция обмена между некоторыми солями и водой приводящая к образованию слабого электролита.
Слайд 5
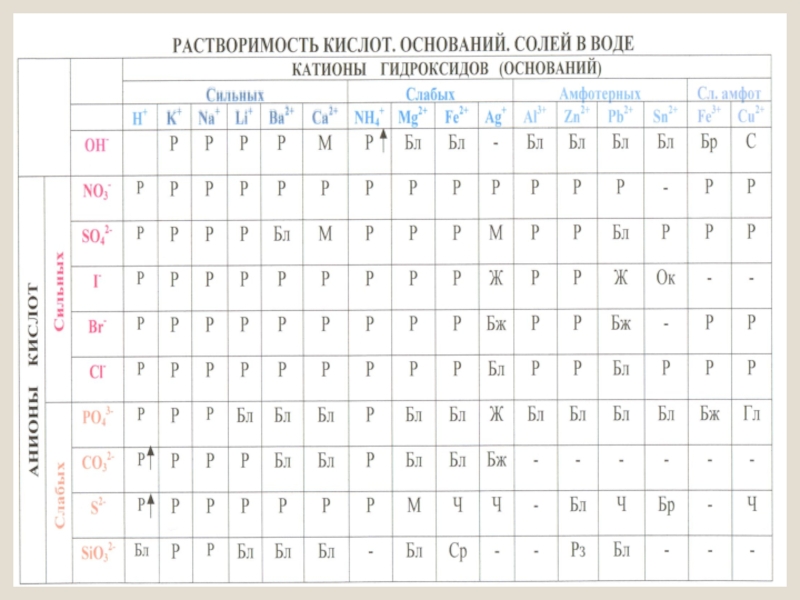
Соли, образованные катионом сильного основания и анионом слабой кислоты. Они подвергаются гидролизу по аниону.
К таким солям относятся: Na2CO3, Na2S, K2SO3, CH3COOK, NaCN, Ba(NO2)2 и т. д.
Их растворы имеют щелочную реакцию среды, рН > 7.
Лакмус в таких растворах синий,
фенолфталеин приобретает малиновую окраску,
метилоранж - жёлтый.
Na2S ↔ 2Na+ + S2-
S2- + H2O ↔ HS- + OH-
Na2S + H2O ↔ NaHS + NaOH
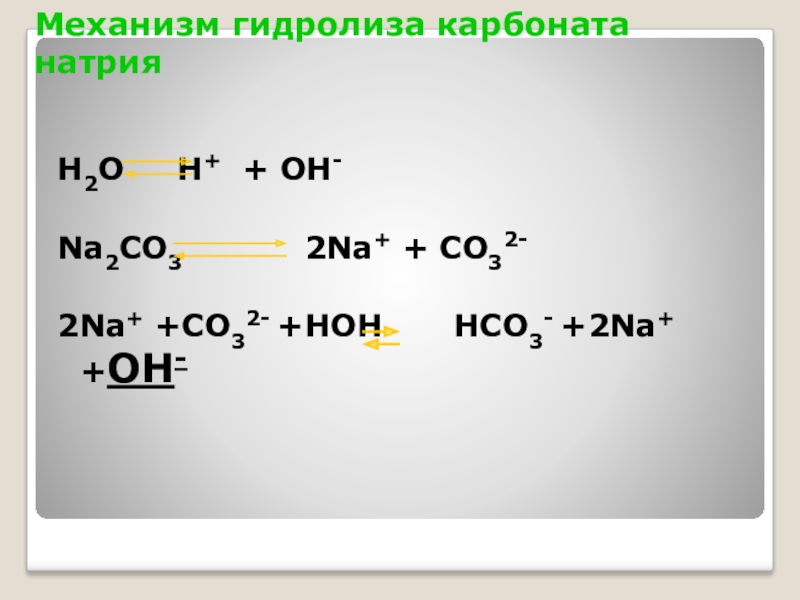
Слайд 6Механизм гидролиза карбоната натрия
H2O H+ + OH-
Na2CO3
2Na+ +CO32- +HOH HCO3- +2Na+ +OH-
Слайд 7CO32- +HOH HCO3- +OH- Na2CO3 +H2O NaHCO3 +NaOH Одним из продуктов
Сформулируем вывод:
Раствор соли, образованной
________________, имеет__________реакцию, так как в растворе избыток ________________.
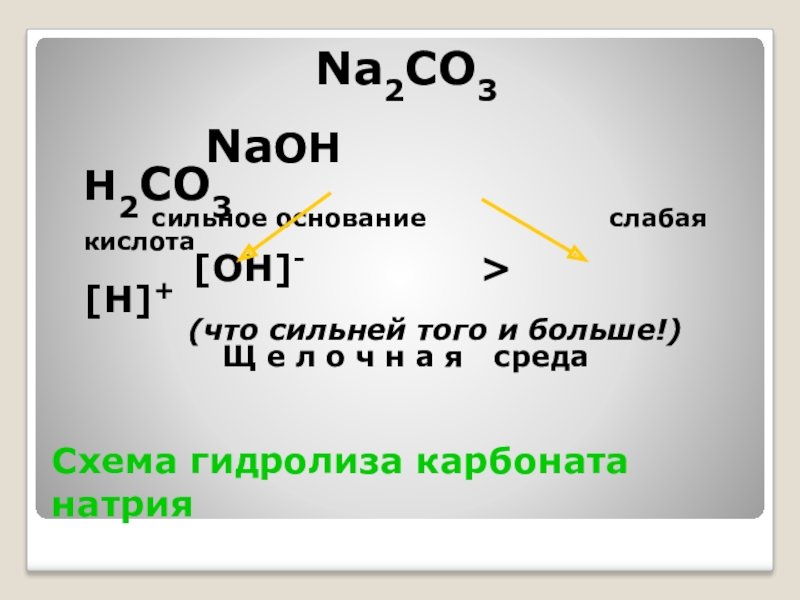
Слайд 8Схема гидролиза карбоната натрия
Na2CO3
NaOH
сильное основание слабая кислота
[OH]- > [H]+
(что сильней того и больше!)
Щ е л о ч н а я среда
Слайд 9FeCl2 ↔ Fe2+ + 2Cl-
Fe2+ + H2O ↔ (FeOH)+ + H+
FeCl2
2. Cоли, образованные катионом слабого основания и анионом сильной кислоты. Они подвергаются гидролизу по катиону.
К таким солям относятся: Zn К таким солям относятся: ZnCl2, FeCl3, CuCl2, NH4I, Al2(SO4)3 и др..
Их растворы имеют кислую реакцию среды, рН < 7.
Лакмус и метилоранж в таких растворах имеют красный цвет, фенолфталеин не изменяет окраски.
Слайд 10Механизм гидролиза хлорида алюминия
H2O H+ + OH-
AlCl3
Al3+ +3Cl- +HOH Al OH2+ +H+ + 3Cl-
Слайд 11Al3+ + HOH AlOH2+ + H+ AlCl3 + H2O
Сформулируем вывод:
Раствор соли, образованной
________________, имеет _____________реакцию, так как в растворе избыток___________________.
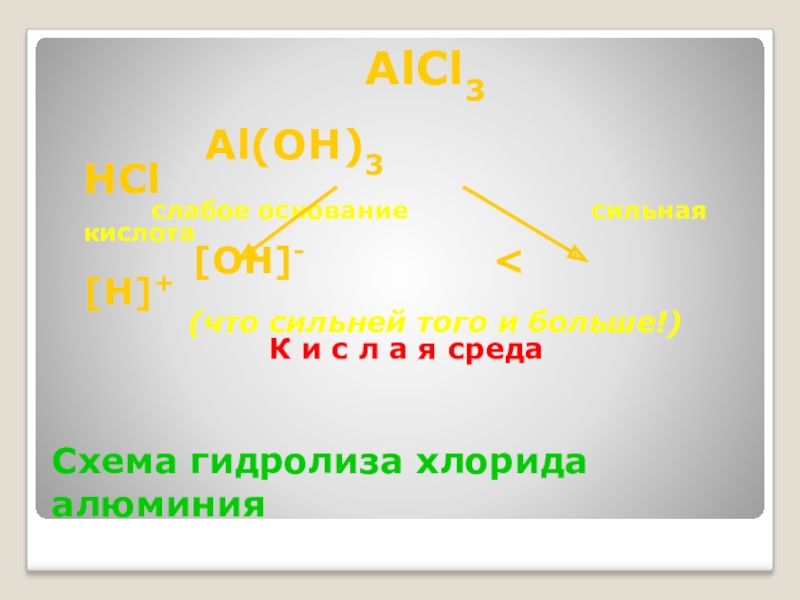
Слайд 12Схема гидролиза хлорида алюминия
Al(OH)3 HCl
слабое основание сильная кислота
[OH]- < [H]+
(что сильней того и больше!)
К и с л а я среда
Слайд 134. Соли, образованные катионом сильного основания и анионом сильной кислоты не
К таким солям относятся: NaCl, K2SO4, NaNO3.
Их растворы имеют нейтральную реакцию среды, рН = 7.
Окраска индикаторов в таких растворах не изменяется.
3. Соли, образованные катионом слабого основания и анионом слабой кислоты. Они подвергаются гидролизу по катиону и по аниону одновременно.
К таким солям относятся: CH3COONH4, (NH4)2S, NH4CN.
Реакция среды их растворов может быть нейтральной, слабо щелочной или слабо кислотной в зависимости константы диссоциации образующихся продуктов.
CH3COONH4 ↔ CH3COO- + NH4+
CH3COO- + NH4+ + H2O ↔ CH3COOH + NH4OH
CH3COONH4 + H2O ↔ CH3COOH + NH4OH
КД (СН3СООН) = КД (NH4OН) , поэтому рН раствора =7
Слайд 14Механизм гидролиза хлорида натрия
H2O H+ + OH-
NaСl Na+
Na+ +Cl- +HOH Cl- + Na+ + HOH
Данная соль гидролизу не подвергается.
Слайд 15NaCl + Н2О =
Сформулируем вывод:
Раствор соли, образованной__________________, имеет________________________реакцию, так
Слайд 16Схема гидролиза карбоната натрия
NaCl
сильное основание сильная кислота
[OH]- = [H]+
Н е й т р а л ь н а я среда
Слайд 19
Количественной характеристикой гидролиза является степень гидролиза α (которую
где n - число моль формульных единиц соли подвергшихся гидролизу, N - общее число моль формульных единиц соли в растворе.
Степень гидролиза зависит от природы соли, концентрации и температуры раствора, наличия в растворе одноименных ионов.
Степень гидролиза увеличивается при разбавлении раствора и повышении температуры.
Степень гидролиза уменьшается с понижением температуры раствора, повышением концентрации раствора, введением в раствор одноименных ионов.
Так, если в раствор фторида калия (F- + H2O ↔ HF + OH-) добавить щелочь, то равновесие гидролиза сместится влево и гидролиз уменьшится.
Факторы, влияющие на степень гидролиза
Слайд 20 Для большинства солей гидролиз обратимый процесс.
Такими солями являются: Al2S3, (NH4)2S, Fe2(CO3)3, (NH4)2SiO3
В уравнениях необратимого гидролиза солей ставится знак равенства:
Al2S3 + 6H2O = 2Al(OH)3↓+ 3H2S↑.
Необратимому гидролизу подвергаются также бинарные соединения:
Mg3N2, CaC2, Р2S5
Необратимый гидролиз
Запишите гидролиз бинарных соединений самостоятельно