- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок физии в 10 классе. Первый закон термодинамики.
Содержание
- 1. Урок физии в 10 классе. Первый закон термодинамики.
- 2. Цель урокаРассмотреть и сформулировать 1-й
- 3. Актуализация знаний учащихся Физический диктант.Напиши формулы
- 4. Энергия ни откуда не берется
- 5. Обмен энергией между термодинамической системой и окружающими
- 6. Первый закон термодинамикиИзменение внутренней энергии системы при
- 7. Соотношение, выражающее первый закон термодинамикиQ = ΔU + AКоличество теплоты, полученное
- 8. В законе речь идетоб изменении внутренней энергии теларабота и количество теплоты характеризуют этот процесс изменения
- 9. Применение I закона термодинамики к изопроцессам:В изохорном
- 10. Слайд 10
- 11. Слайд 11
- 12. Слайд 12
- 13. Слайд 13
- 14. Закрепление 1. Чему равно изменение внутренней энергии
- 15. Рефлексия. (Самоконтроль учащихся) 1. Как изменилась
- 16. Рефлексия. (Самоконтроль учащихся) 4. Переход газа из
- 17. Вариант I1. Как изменится внутренняя энергия идеального
- 18. Вариант 21. Как изменится внутренняя энергия идеального газа
- 19. Ответы1-й Вариант1-б;2-а;3-д;4-б.2-й Вариант1-а;2-а;3-б;4-б.
- 20. Итог С каким законом мы познакомились. Как
Слайд 2Цель урока
Рассмотреть и сформулировать
1-й закон термодинамики, выяснить
Сформировать понятие о адиабатном процессе
Расширить представление о изопроцессах и показать применение 1-го закона термодинамики к ним
Доказать единство закона сохранения энергии для различных явлений в природе
Слайд 3Актуализация знаний учащихся
Физический диктант.
Напиши формулы
I вариант II вариант
1. Закон Гей- Люссака 1. Закон Шарля
2. Бойля- Мариотта 2. Менделеева-Клапейрона
3. Клапейрона 3. Внутренняя энергия
4. Работы в термодинамике 4. Количество теплоты на нагревание
5. Количество теплоты на плавление 5. Количество теплоты на парообразование
6. Сгорает топливо 6.КПД тепловой машины
Слайд 4 Энергия ни откуда не берется и бесследно не исчезает, она
Открыт он был Гельмгольцем, Мейером, Джоулем и связывает все явления природы воедино.
Этот закон распространяется и на тепловые явления.
При изменении температуры механическая энергия не меняется.
Г.Гельмгольц (1821-1894) Р.Мейер (1814-1878) Д.Джоуль (1818-1889)
Слайд 5
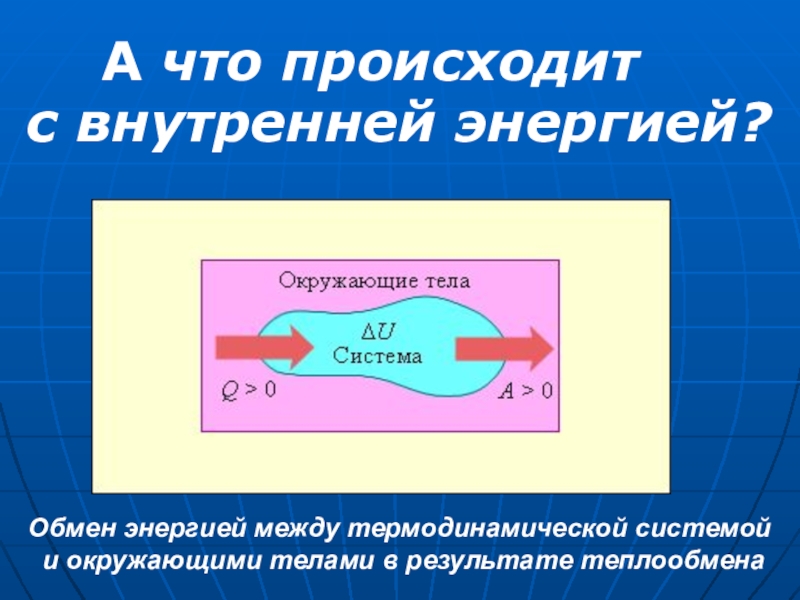
Обмен энергией между термодинамической системой
и окружающими телами в результате теплообмена
с внутренней энергией?
Слайд 6Первый закон термодинамики
Изменение внутренней энергии системы при переходе её из одного
ΔU = A+Q
Слайд 7Соотношение, выражающее первый закон термодинамики
Q = ΔU + A
Количество теплоты, полученное системой, идет на изменение
Работа газа всегда отрицательна.
Из I закона термодинамики вытекает невозможность создания вечного двигателя, который должен совершать работу без затрат энергии топлива.
Слайд 8В законе речь идет
об изменении внутренней энергии тела
работа и количество теплоты
Слайд 9Применение I закона термодинамики к изопроцессам:
В изохорном процессе (V = const) газ работы
Q = ΔU = U (T2) – U (T1).
Здесь U (T1) и U (T2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением
A = p (V2 – V1) = p ΔV. Первый закон термодинамики для изобарного процесса дает:
Q = U (T2) – U (T1) + p (V2 – V1) = ΔU + p ΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T2 < T1; внутренняя энергия убывает, ΔU < 0.
В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа,
ΔU = 0.
Первый закон термодинамики для изотермического процесса выражается соотношением
Q = A.
Газ совершает работу за счет полученного количество теплоты.
Проверить и разобрать выводы.
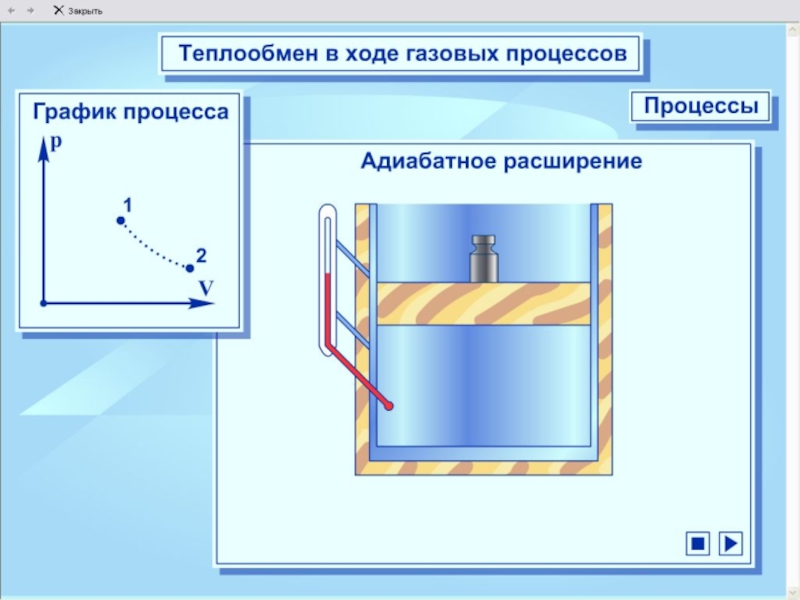
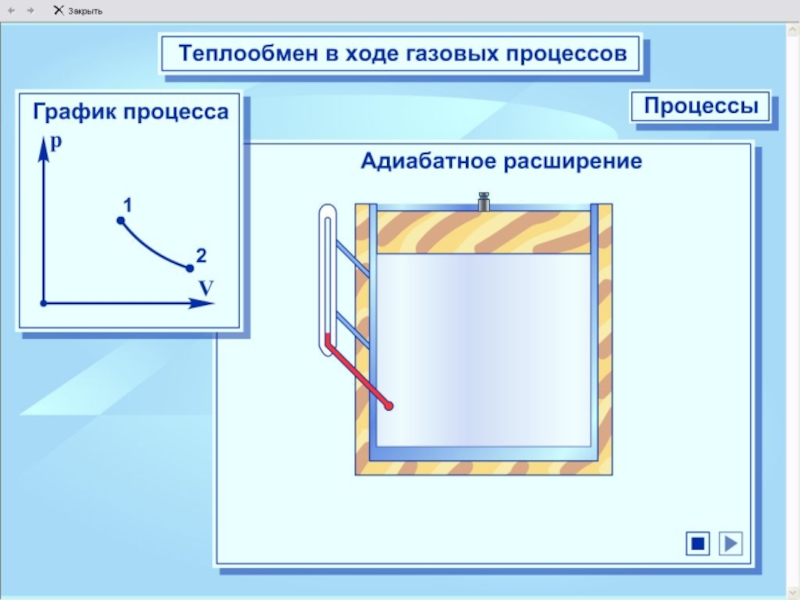
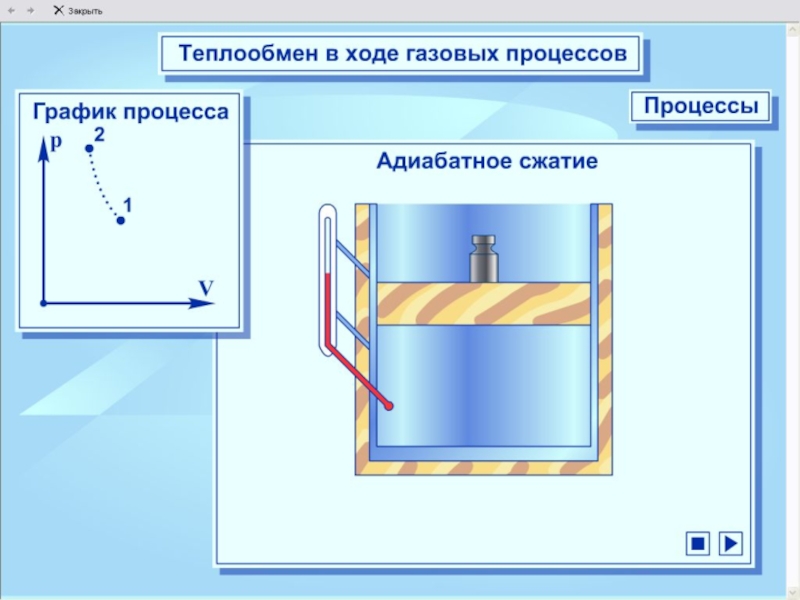
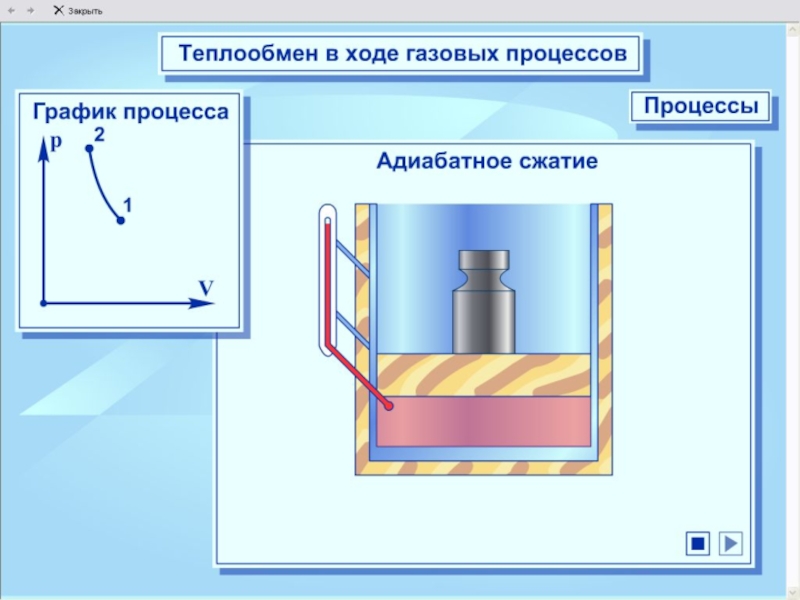
Адиабатный процесс - это процесс без теплопередаче.
При быстром сжатии работа совершается над газом внутренняя энергия и температура – увеличивается; при быстром расширении газ совершает работу и внутренняя энергия и температура уменьшается.
Применение: в двигателях Дизеля, при работе компрессоров, для получения сжиженных газов, в грандиозных масштабах в атмосфере Земли. Получение облаков, выпадение осадков.
Модель. Адиабатический процесс
В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид
A = –ΔU, т. е. газ совершает работу за счет убыли его внутренней энергии
Слайд 14Закрепление
1. Чему равно изменение внутренней энергии газа если ему
2. При адиабатным расширением совершена работа 200 Дж. Найти изменение внутренней энергии.
3.
Найти работу при переходе из состояния 1-2
4. Какой процесс, если 1) А=0;
2) ∆U = 0
2
2
4
4
6
6
Ответ: 800 Дж; 200 Дж; 16.103 Дж; Vпостоянная; Т постоянная
Р,103Па
V,м3
1
2
Слайд 15Рефлексия.
(Самоконтроль учащихся)
1. Как изменилась внутренняя энергия идеального газа
2. Как изменилась внутренняя энергия газа, если ему передано количество теплоты 200 Дж и внешние силы совершают над ним работу 600 Дж.
3. Какую работу совершил газ при переходе из состояния 1 в состояние 2?
Ответ: a) ∆U =0; б)∆U>0; b)∆U<0; г)∆U=A; д)∆U =А'.
Ответ: а)0; б)400Дж; в)500Дж; г)800Дж; д)200Дж.
100
200
300
2
1
1
2
3
Р,Па
V,м3
Слайд 16Рефлексия.
(Самоконтроль учащихся)
4. Переход газа из состояния М в состояние N
5. Выделяется или поглощается
теплота при конденсации водяного
пара?
Ответ: а) выделяется; б) поглощается;
в) не выделяется и не поглощается; г) процесс может идти как с выделением, так и с поглощением теплоты.
М
1
Р
V
Ответ: а)1;б)2; в)3; г)4;
д) при всех способах одинаковая
Ответы: 1 -А, 2 - Г, 3- В, 4 - А, 5 – А
Слайд 17Вариант I
1. Как изменится внутренняя энергия идеального газа при адиабатном расширении,
2. В каком процессе изменения внутренней энергии системы равно количеству переданной теплоты.
а)изохорном; б) изобарном; в) изотермическом; г) адиабатном; д) нет ответа.
3. Газу передано 100 Дж количества теплоты и внешние силы совершили над ним работу 300 Дж. Чему равно изменение внутренней энергии. а) нулю; б) 100 Дж; в) 200Дж; г) 300Дж; д) 400Дж
4. Чему равна работа, совершенная газом, при переходе из состояния 1 в состояние2.
1
2
3
4
50
100
1
2
Р, Па
V,м3
а) 0; б) 300Дж; в)200Дж;
г) 900Дж; д) нет ответа.
Слайд 18Вариант 2
1. Как изменится внутренняя энергия идеального газа при изотермическом сжатии.
2. Какой процесс произошел при сжатии идеального газа, если работа, совершенная внешними силами над газами, равна изменению внутренней энергии газа?
а) адиабатный; б) изобарный; в) изохорный; г)изотермический; д) нет ответа.
3. Газ получил количество теплоты 300 Дж, его внутренняя энергия увеличилась на 200 Дж.
Чему равна работа, совершенная газом?
а) нулю ;б) 100 Дж; в) 200Дж; г) З00Дж; д) 400Дж.
4. Чему равна работа, совершенная газом, при переходе из состояния 1 в состояние2.
500
1000
1
2
Р, Па
V,м3
1
2
3
а) 3000Дж; б)2000 Дж; в) 1200Дж; г) 0; д) нет ответа.
Слайд 20Итог
С каким законом мы познакомились.
Как читается этот закон
Оценки за урок:
- за физический диктант
- самооценка учащихся
- оценка учителем самостоятельной работы учащихся
На дом
§ 80, 81; Упражнение 15 (10,3,7, рис. на стр.183) (Учебник «Физика 10» Г.Я.Мякишев, Б.Б.Буховцев.М.2003г.)