- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Строение атома. Опыт Резерфорда
Содержание
- 1. Строение атома. Опыт Резерфорда
- 2. Гипотезы о строении веществаГипотеза о том, что
- 3. Развитие представлений о строении атомаКонкретные представления о
- 4. 1896г. -Дж.Дж.Томсон - выдающийся ученый, директор знаменитой
- 5. Модель атома Томсона
- 6. Через несколько лет в опытах великого английского
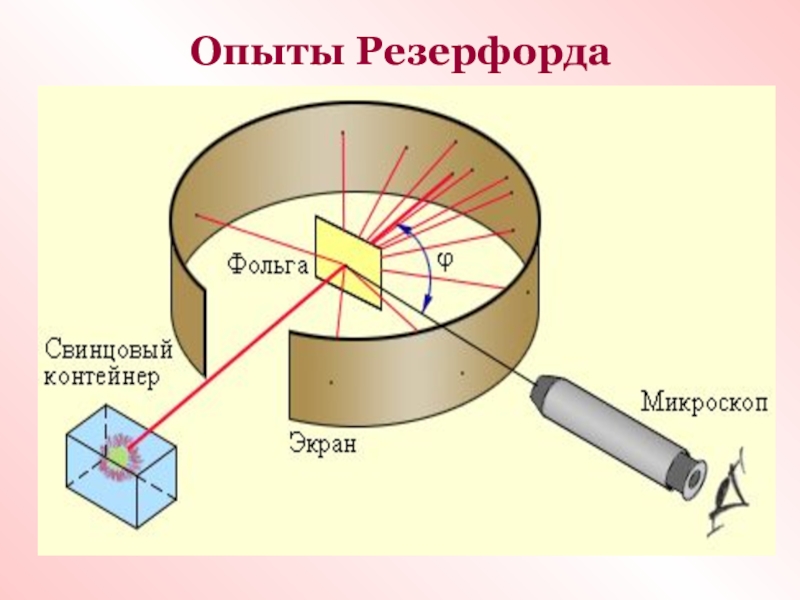
- 7. Опыты Резерфорда
- 8. Модель атома РезерфордаРезерфорд показал, что модель Томсона
- 9. I ПОСТУЛАТ БОРА Атомная система может находится только
- 10. II ПОСТУЛАТ БОРА При переходе атома из стационарного
- 11. II ПОСТУЛАТ БОРА При переходе атома из стационарного
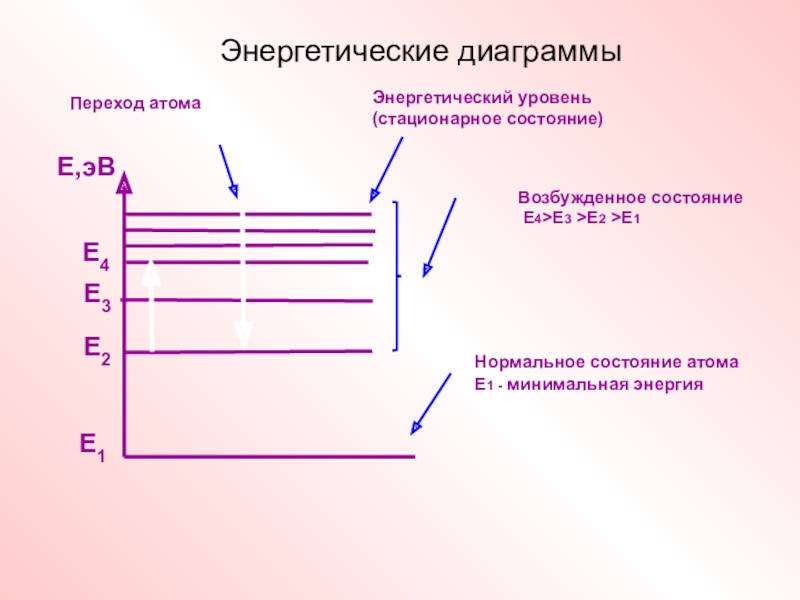
- 12. Энергетические диаграммы Е1Е2Е3Е,эВЕ4Энергетический уровень (стационарное состояние)Нормальное состояние атома
- 13. Правило квантования III постулат Бора
- 14. Выберите правильный ответВ состав ядра атома входят
- 15. 3) Кто предложил ядерную модель строения атома?
- 16. Проверь себя ... Б Б Г Б А
- 17. Домашнее задание § 94, 95 выполнить
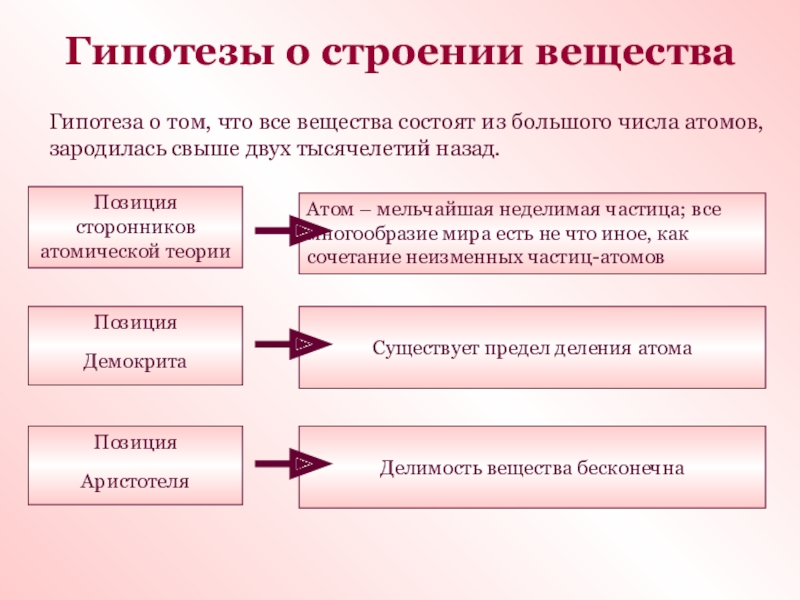
Слайд 2Гипотезы о строении вещества
Гипотеза о том, что все вещества состоят из
Позиция сторонников атомической теории
Атом – мельчайшая неделимая частица; все многообразие мира есть не что иное, как сочетание неизменных частиц-атомов
Позиция
Демокрита
Существует предел деления атома
Позиция
Аристотеля
Делимость вещества бесконечна
Слайд 3Развитие представлений о строении атома
Конкретные представления о строении атома развивались по
В начале 19 века молекулярно-кинетическая теория установила примерные размеры атомов и небольших молекул: около 10-10 м
В конце 19 века был открыт электрон, а также измерена его масса и заряд
В.Вебер впервые высказывает мысль об электронном строении атома
Х.Лоренц в 1896 году создал электронную теорию: электроны входят в состав атома
в 1896 году А.Беккерель открыл явление радиоактивности
Каково строение атома?
Слайд 41896г. -Дж.Дж.Томсон - выдающийся ученый, директор знаменитой Кавендишской лаборатории, лауреат Нобелевской
1903г. - Дж.Дж.Томсон выдвинул гипотезу о том, что электрон находится внутри атома. Но атом в целом нейтральный, поэтому ученый предположил, что отрицательные электроны окружены в атоме положительно заряженным веществом. Атом, по мысли Дж. Томсона, очень похож на "пудинг с изюмом", где "каша" - положительно заряженное вещество атома., а электроны- " изюм" в ней.
Дж.Дж.Томсон
Слайд 6Через несколько лет в опытах великого английского физика Э. Резерфорда было доказано,
Первые прямые эксперименты по исследованию внутренней структуры атомов были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909–1911 годах. Резерфорд предложил применить зондирование атома с помощью α-частиц, которые возникают при радиоактивном распаде радия и некоторых других элементов.
Эрнест Резерфорд
Слайд 8Модель атома Резерфорда
Резерфорд показал, что модель Томсона находится в противоречии с
атом имеет ядро, размеры которого малы по сравнению с размерами самого атома (dя ≈ 10-12 – 10-13 см);
в ядре сконцентрирована почти вся масса атома;
отрицательный заряд всех электронов распределён по всему объему атома
Модель атома Резерфорда
Слайд 9I ПОСТУЛАТ БОРА
Атомная система может находится только в особых стационарных квантовых
В стационарных состояниях атом не излучает.
+
-
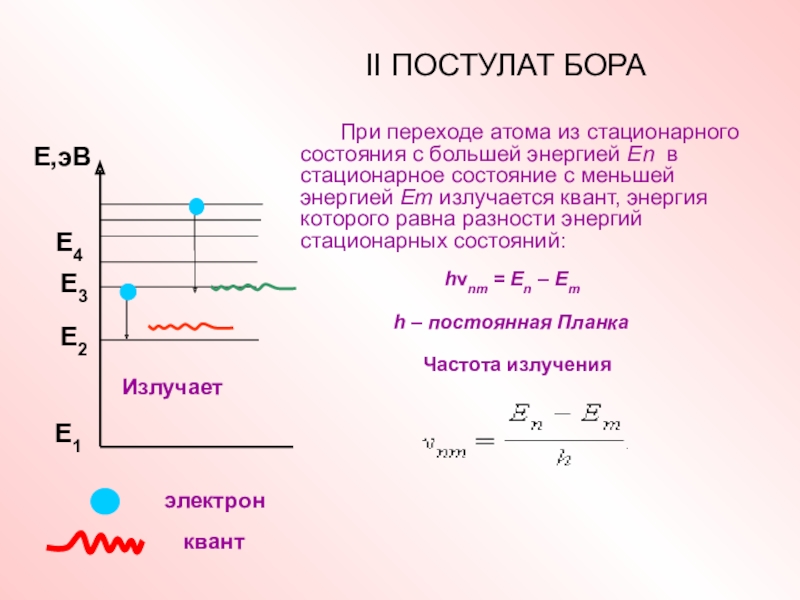
Слайд 10II ПОСТУЛАТ БОРА
При переходе атома из стационарного состояния с большей энергией
Е1
Е2
Е3
Е,эВ
Излучает
Е4
hνnm = En – Em
h – постоянная Планка
Частота излучения
электрон
квант
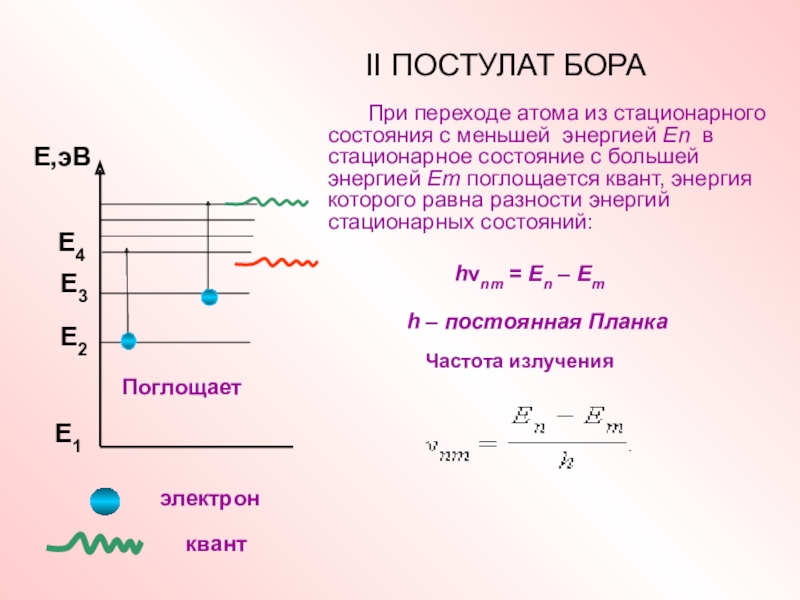
Слайд 11II ПОСТУЛАТ БОРА
При переходе атома из стационарного состояния с меньшей энергией
Е1
Е2
Е3
Е,эВ
Поглощает
Е4
hνnm = En – Em
h – постоянная Планка
Частота излучения
квант
электрон
Слайд 12Энергетические диаграммы
Е1
Е2
Е3
Е,эВ
Е4
Энергетический уровень (стационарное состояние)
Нормальное состояние атома
Е1 - минимальная энергия
Возбужденное
Е4>Е3 >Е2 >Е1
Переход атома
Слайд 13Правило квантования
III постулат Бора
В стационарном состоянии
me - масса электрона,
υ – скорость электрона
rn – радиус стационарной круговой
орбиты
Правило квантования Бора позволяет вычислить радиусы стационарных орбит электрона в атоме водорода и определить значения энергий
Слайд 14Выберите правильный ответ
В состав ядра атома входят следующие частицы:
Ядерная модель атома представляет из себя: А. положительно заряженный шар радиусом 10-10 м, в котором «плавают» электроны, нейтрализующие положительный заряд. Б. Вся масса атома сконцентрирована в ядре, которое имеет положительный заряд. Вокруг ядра подобно планете вращаются электроны. В. Комбинация центрального положительного атома, равномерно размазанного по сфере, и электронов, которые располагаются по сферическим концентрическим поверхностям.
Слайд 153) Кто предложил ядерную модель строения атома?
4) С помощью опытов Резерфорд установил, что … А. Положительный заряд распределен равномерно по всему объему атома. Б. Положительный заряд сосредоточен в центре атома и занимает очень малый объем. В. В состав атома входят электроны. Г. Атом не имеет внутренней структуры.
5) Современная модель структуры атома обоснована опытами: А. По рассеянию α-частиц Б. По сжимаемости жидкости В. По электризации Г. По тепловому расширению
Слайд 17Домашнее задание
§ 94, 95
выполнить буклет на одну из
«Эрнест Резерфорд. Опыты по рассеиванию α-частиц»
«Планета по имени атом»
«Модели строения атома»