- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Природа электрического тока в растворах и расплавах электролитов
Содержание
- 1. Природа электрического тока в растворах и расплавах электролитов
- 2. http://dvsschool.zz.mu/Электролиты
- 3. http://dvsschool.zz.mu/Электролиты — жидкие проводники, в которых подвижными носителями зарядов являются ионы.Электролитическая диссоциация
- 4. http://dvsschool.zz.mu/Интенсивность электролитической диссоциации зависит:1. От температуры раствора.От концентрации
- 5. Сопротивление растворов электролитовУменьшается R с повышением температуры.Справедлив
- 6. http://dvsschool.zz.mu/Закон электролиза Фарадея
- 7. http://dvsschool.zz.mu/Закон электролиза ФарадеяМайкл ФарадейПервый закон электролиза Фарадея:
- 8. http://dvsschool.zz.mu/Закон электролиза ФарадеяПри электролизе на электродах происходит
- 9. http://dvsschool.zz.mu/Определение заряда электрона
- 10. http://dvsschool.zz.mu/1. В гальваностегии (никелирование, серебрение).2. В гальванопластике (изготовление копий);
- 11. http://dvsschool.zz.mu/Источники и литература:1. ТРУБЕЦКОВА С. В., ФИЗИКА.
Слайд 1Природа электрического тока в растворах и расплавах электролитов
http://dvsschool.zz.mu/
"Нет стремления более естественного,
М. Монтень
Слайд 3http://dvsschool.zz.mu/
Электролиты — жидкие проводники, в которых подвижными носителями зарядов являются ионы.
Электролитическая
Слайд 4http://dvsschool.zz.mu/
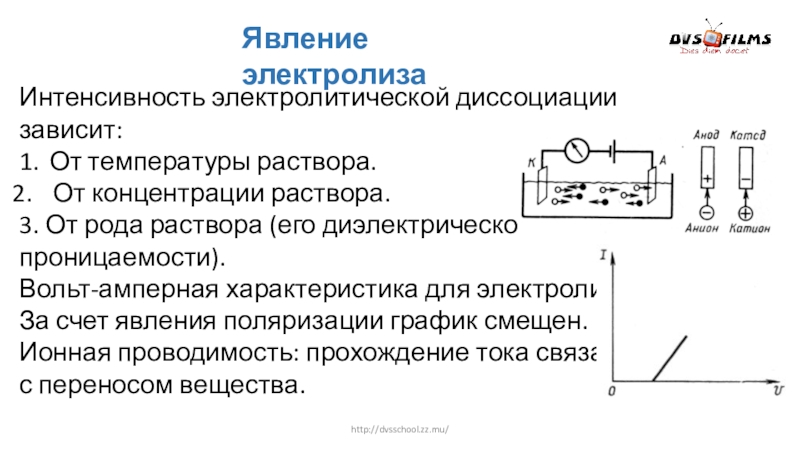
Интенсивность электролитической диссоциации зависит:
1. От температуры раствора.
От концентрации раствора.
3. От рода раствора
Вольт-амперная характеристика для электролитов.
За счет явления поляризации график смещен.
Ионная проводимость: прохождение тока связано
с переносом вещества.
Явление электролиза
Слайд 5Сопротивление растворов электролитов
Уменьшается R с повышением температуры.
Справедлив закон Ома при неизменной
http://dvsschool.zz.mu/
Удельная электропроводность - проводимость единицы объема раствора, обратно пропорциональна удельному сопротивлению
Удельная электропроводность (k)раствора электролита - это электрическая проводимость объёма раствора, заключённого между двумя параллельными электродами площадью 1 м2 каждый, расположенными на расстоянии 1 м друг от друга.
Слайд 7http://dvsschool.zz.mu/
Закон электролиза Фарадея
Майкл Фарадей
Первый закон электролиза Фарадея: масса вещества, осаждённого на
Второй закон электролиза Фарадея: для данного количества электричества (электрического заряда) масса химического элемента, осаждённого на электроде, прямо пропорциональна эквивалентной массе элемента. Эквивалентной массой вещества является его молярная масса, делённая на целое число,
зависящее от химической реакции, в которой
участвует вещество.
Слайд 8http://dvsschool.zz.mu/
Закон электролиза Фарадея
При электролизе на электродах происходит выделение вещества:
Где eNA=F —
Слайд 10http://dvsschool.zz.mu/
1. В гальваностегии (никелирование, серебрение).
2. В гальванопластике (изготовление копий); 1838 г., Б. С. Якоби.
3. Электронатирание.
4. Промышленный
5. Очистка металлов, полученных при выплавке из руды, от посторонних примесей.
6. Электрополировка поверхностей.
Применение электролиза
Борис Семёнович Якоби
Слайд 11http://dvsschool.zz.mu/
Источники и литература:
1. ТРУБЕЦКОВА С. В., ФИЗИКА. ВОПРОСЫ — ОТВЕТЫ. ЗАДАЧИ
2. Луппов Г.Д., Молекулярная физика и электродинамика в опорных конспектах и тестах., Кн. для учителя. — М.: Просвещение, 1992.
3. Мякишев, Буховцев, Сотский: Физика. 10 класс. Учебник.
4. https://phys-ege.sdamgia.ru/