- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по физике на тему Электрический ток в жидкостях (10 класс)
Содержание
- 1. Презентация по физике на тему Электрический ток в жидкостях (10 класс)
- 2. По электрическим свойствам все жидкости можно разделить
- 3. Электролитическая диссоциацияЭлектролитическая диссоциация – распад молекул электролитов
- 4. Рекомбинация ионовНаряду с диссоциацией в электролите одновременно
- 5. Ионная проводимостьНосителями заряда в водных растворах или
- 6. Электролиз При ионной проводимости прохождение тока связано
- 7. Применение электролизаЭлектролиз широко применяют в технике для
- 8. Список источников Физика. 10 класс: учеб. для
Слайд 2По электрическим свойствам все жидкости можно разделить на 2 группы:
Содержащие
Не содержащие свободные заряженные частицы (недиссоциирующие)
К ним относятся растворы (чаще всего водные) и расплавы солей, кислот и оснований
К ним относятся дистилированная вода, спирт, минеральное масло
ЖИДКОСТИ
ПРОВОДЯЩИЕ
НЕПРОВОДЯЩИЕ
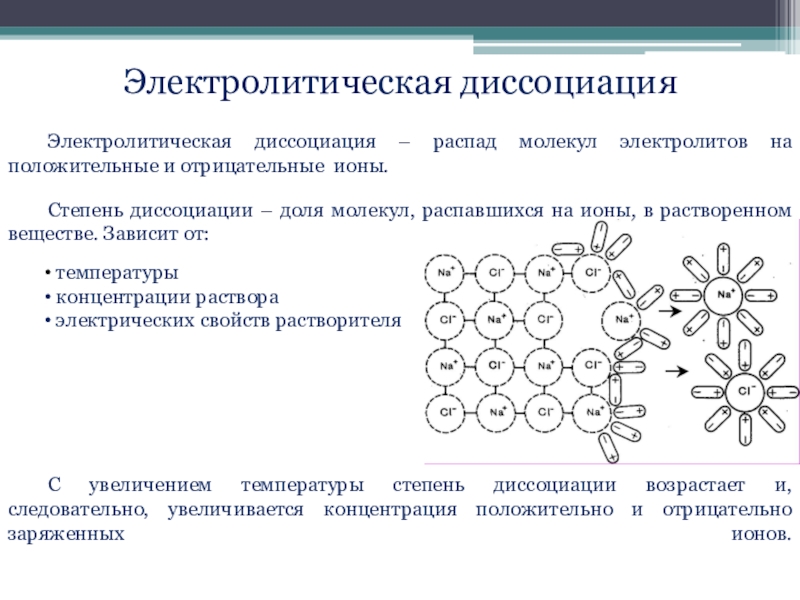
Слайд 3Электролитическая диссоциация
Электролитическая диссоциация – распад молекул электролитов на положительные и отрицательные
Степень диссоциации – доля молекул, распавшихся на ионы, в растворенном веществе. Зависит от:
температуры
концентрации раствора
электрических свойств растворителя
С увеличением температуры степень диссоциации возрастает и, следовательно, увеличивается концентрация положительно и отрицательно заряженных ионов.
Слайд 4Рекомбинация ионов
Наряду с диссоциацией в электролите одновременно может происходить процесс восстановления
При неизменных условиях в растворе устанавливается динамическое равновесие, при котором число молекул, распадающихся за секунду на ионы, равно числу пар ионов, которые за то же время вновь объединяются в нейтральные молекулы.
Слайд 5Ионная проводимость
Носителями заряда в водных растворах или расплавах электролитов являются положительно
Если сосуд с раствором электролита включить в электрическую цепь, то отрицательные ионы начнут двигаться к положительному электроду - аноду, а положительные - к отрицательному - катоду. В результате установится электрический ток. Поскольку перенос заряда в водных растворах или расплавах электролитов осуществляется ионами, такую проводимость называют ионной.
Слайд 6Электролиз
При ионной проводимости прохождение тока связано с переносом вещества. На
Слайд 7Применение электролиза
Электролиз широко применяют в технике для различных целей. Электролитическим путем
Если обеспечить хорошее отслаивание электролитического покрытия от поверхности, на которую осаждается металл (этого достигают, например, нанося на поверхность графит), то можно получить копию с рельефной поверхности.
Процесс получения отслаиваемых покрытий - гальванопластика - был разработан русским ученым Б. С. Якоби (1801-1874), который в 1836 г. применил этот способ для изготовления полых фигур для Исаакиевского собора в Санкт-Петербурге.
Еще одним способом применения электролиза является получение чистого металла из примесей. С помощью электролиза изготавливают печатные платы для различных цифровых устройств.
Слайд 8Список источников
Физика. 10 класс: учеб. для общеобразоват. учреждений: базовый
http://class-fizika.narod.ru/10_12.htm
http://www.nado5.ru/e-book/ehlektricheskii-tok-v-zhidkostyakh
http://rza.org.ua/glossary/image-246.html (картинка)
http://www.electrofaq.com/ETMbook/CONDUCT/CON5A.HTM (картинка)
http://lib.convdocs.org/docs/index-280240.html (картинка)