- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по предмету Естествознание, раздел Химия
Содержание
- 1. Презентация по предмету Естествознание, раздел Химия
- 2. Атомы благородных газов имеют завершённый внешний энергетический
- 3. Химическая связь – это силы взаимодействия, которые
- 4. В образовании химической связи участвуют только валентные
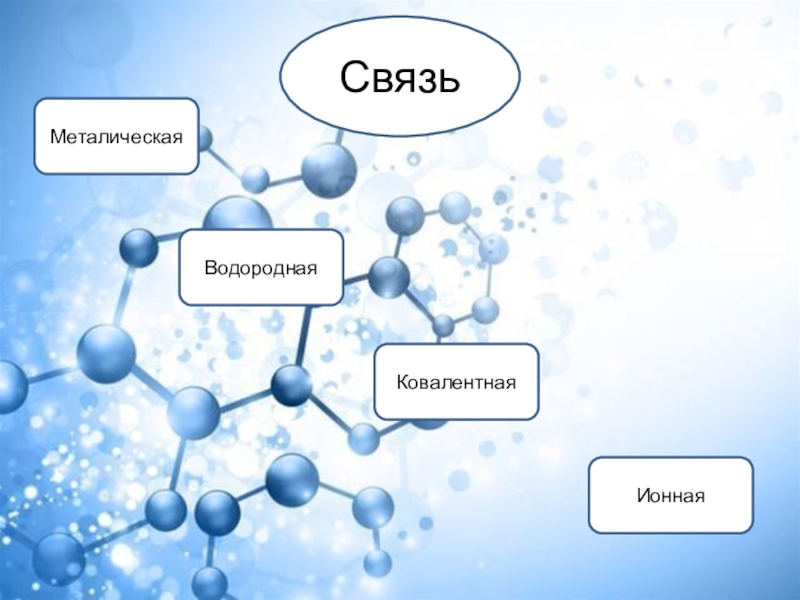
- 5. СвязьМеталическаяКовалентнаяВодороднаяИонная
- 6. Ковалентная связь.Ковалентная связь – это химическая связь
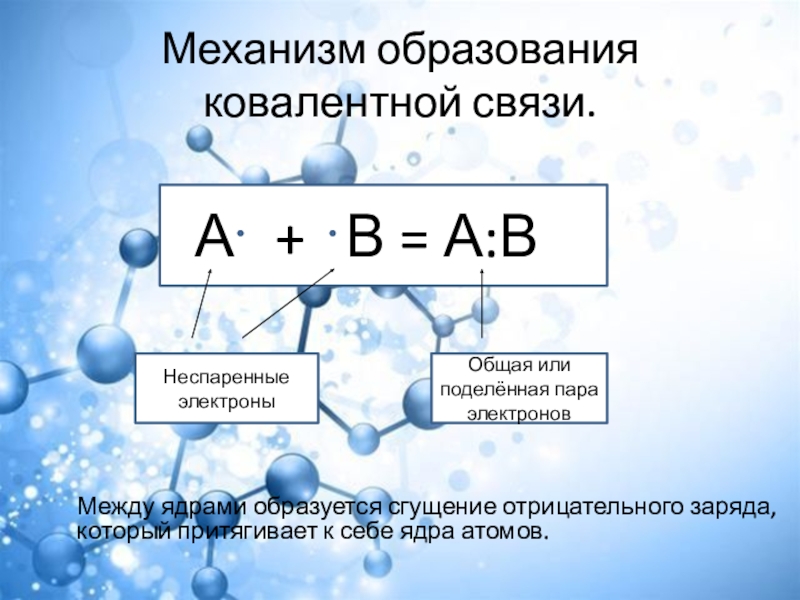
- 7. Механизм образования ковалентной связи. Между ядрами образуется
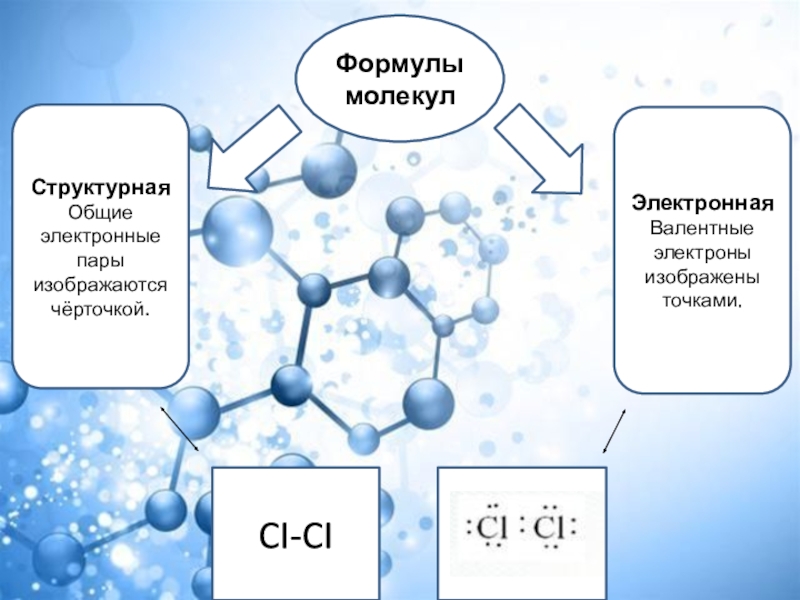
- 8. Формулы молекулСтруктурная Общие электронные пары изображаются чёрточкой.Электронная Валентные электроны изображены точками.CI-CI
- 9. Спасибо за внимание.
Атомы благородных газов имеют завершённый внешний энергетический уровень. Он наиболее устойчив и стабилен, что является причиной инертности атомов благородных газов. Атомы других элементов пытаются приобрести конфигурацию ближайшего благородного газа и перейти в наиболее устойчивое состояние. Такое
Слайд 2Атомы благородных газов имеют завершённый внешний энергетический уровень. Он наиболее устойчив
и стабилен, что является причиной инертности атомов благородных газов. Атомы других элементов пытаются приобрести конфигурацию ближайшего благородного газа и перейти в наиболее устойчивое состояние. Такое состояние атомы приобретают, взаимодействуя между собой, в результате между ними возникает химическая связь.
Слайд 3Химическая связь – это силы взаимодействия, которые соединяют отдельные атомы в
молекулы, ионы, кристаллы.
Валентность – это способность атома элемента образовывать различное число химических связей с другими атомами. Величина валентности элемента определяется числом химических связей, которые атом элемента образует с другими атомами.
Валентность – это способность атома элемента образовывать различное число химических связей с другими атомами. Величина валентности элемента определяется числом химических связей, которые атом элемента образует с другими атомами.
Слайд 4В образовании химической связи участвуют только валентные электроны. У элементов главных
подгрупп это электроны внешнего энергетического уровня. Они расположены дальше от ядра и менее прочно связаны с ним. В зависимости от способа образования завершённых электронных структур атомов различают несколько видов химической связи.
Слайд 6Ковалентная связь.
Ковалентная связь – это химическая связь между атомами, осуществляемая при
помощи общих электронных пар.
В образовании ковалентной связи принимают участие неспаренные валентные электроны атома, которые располагаются на внешнем уровне по одному. Число неспаренных электронов = 8 – номер группы элемента Например, у серы число неспаренных электронов равно 8 – 6 = 2.
В образовании ковалентной связи принимают участие неспаренные валентные электроны атома, которые располагаются на внешнем уровне по одному. Число неспаренных электронов = 8 – номер группы элемента Например, у серы число неспаренных электронов равно 8 – 6 = 2.
Слайд 7Механизм образования ковалентной связи.
Между ядрами образуется сгущение отрицательного заряда, который
притягивает к себе ядра атомов.
А + В = А:В
Неспаренные электроны
Общая или поделённая пара электронов