Подготовила:
учитель
МКОУ Большеверейской СОШ
Свиридова Наталья Анатольевна
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Проектно-исследовательская деятельность обучающихся на уроках биологии и во внеурочное время
Содержание
- 1. Презентация по теме Проектно-исследовательская деятельность обучающихся на уроках биологии и во внеурочное время
- 2. Метод проектовМетод проектов – личностно ориентированный способ
- 3. Таблица 1Классификация исследовательских проектов
- 4. Работы над проектами начинаю в 5-7 классах
- 5. Примерные темы проектов по химииВ 8-9 классах-
- 6. Анализ воды природного источника в разные
- 7. Методика работы Отбор проб для анализа производился
- 8. Методика проведения: 1. В посуду
- 9. Реакции ионного обменаSО4. Для обнаружения ионов
- 10. Слайд 10
- 11. ВыводВода из природного источника не имеет вредных
- 12. Литература1. Шалашова М. М. Особенности организации образовательного
- 13. СПАСИБО ЗА ВНИМАНИЕ.
Метод проектовМетод проектов – личностно ориентированный способ эффективного выстраивания исследовательской деятельности учащихся, интегрирующий в себе проблемный подход, групповые методы, рефлексивные, презентативные, исследовательские, поисковые и прочие методики.
Слайд 1Проектно- исследовательская деятельность обучающихся на уроках химии и биологии и во внеурочное
время
(из опыта работы)
Слайд 2Метод проектов
Метод проектов – личностно ориентированный способ эффективного выстраивания исследовательской деятельности
учащихся, интегрирующий в себе проблемный подход, групповые методы, рефлексивные, презентативные, исследовательские, поисковые и прочие методики.
Слайд 4Работы над проектами начинаю в 5-7 классах при изучении предмета «Природоведение»
и «Биология».
Создаем небольшие проекты («Комнатные растения нашей школы», «Семейства растений», «Отряды животных» и т.д.)
Создаем небольшие проекты («Комнатные растения нашей школы», «Семейства растений», «Отряды животных» и т.д.)
Слайд 5Примерные темы проектов по химии
В 8-9 классах- «Химическое производство», «Химия в
быту», «Химия и здоровье», «Жизнь и деятельность великих химиков», «Роль кислот», «Значение удобрений», «Определение нитратов в овощах и фруктах» и т.д.
В 10-11 классах- информационные карты, «Определение здоровья человека по смывам», «Определение качества питьевой воды методами химического анализа» и т.д.
В 10-11 классах- информационные карты, «Определение здоровья человека по смывам», «Определение качества питьевой воды методами химического анализа» и т.д.
Слайд 6Анализ воды природного источника
в разные периоды времени
Цель работы:
определить
наличие в воде химических соединений загрязняющего характера;
научиться проводить качественные реакции;
выявлять основные компоненты природных и антропогенных систем.
научиться проводить качественные реакции;
выявлять основные компоненты природных и антропогенных систем.
Слайд 7Методика работы
Отбор проб для анализа производился в несколько приёмов в
июле (1), в августе (2), в сентябре (3). Одновременно проводился анализ питьевой воды из уличного водопровода (4). Для контроля использовали дистиллированную воду (5).
Метод основан на проведении обменных реакций между ионами.
Метод основан на проведении обменных реакций между ионами.
Слайд 8
Методика проведения:
1. В посуду для микрометода помещаются пробы воды.
2.
Пипеткой медицинской добавляем по 1-2 капли реактива.
3. По изменению окраски, выпадению осадка, выделению газа делаем вывод о наличии ионов.
4. Каждый опыт повторяем 5 раз.
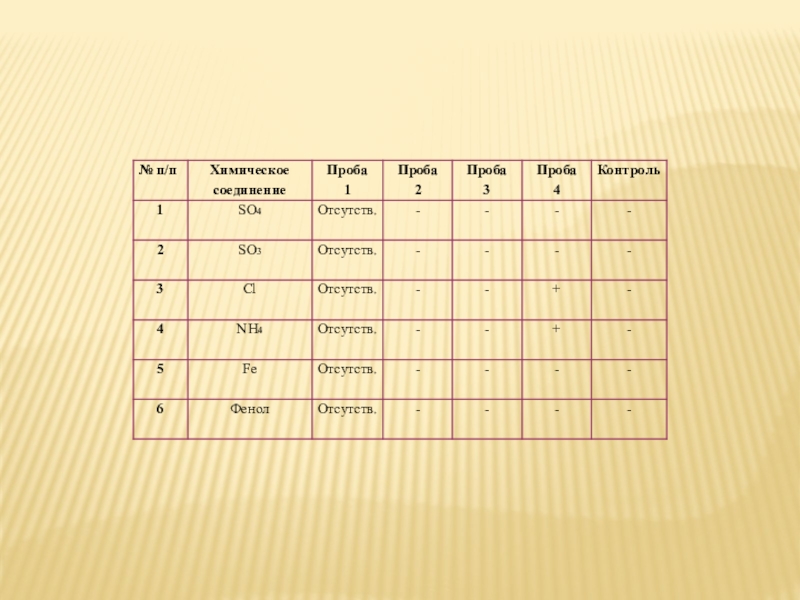
5. Результат заносим в таблицу № 1.
SО4. Для обнаружения ионов добавляем раствор хлорида бария. При содержании ионов возникают помутнения.
SО3. Прибавляем слабый раствор марганцовокислого калия. При содержании ионов SО3 розовый цвет исчезает.
3. По изменению окраски, выпадению осадка, выделению газа делаем вывод о наличии ионов.
4. Каждый опыт повторяем 5 раз.
5. Результат заносим в таблицу № 1.
SО4. Для обнаружения ионов добавляем раствор хлорида бария. При содержании ионов возникают помутнения.
SО3. Прибавляем слабый раствор марганцовокислого калия. При содержании ионов SО3 розовый цвет исчезает.
Слайд 9
Реакции ионного обмена
SО4. Для обнаружения ионов добавляем раствор хлорида
бария. При содержании ионов SО4 возникают помутнения.
SО3. Прибавляем слабый раствор марганцовокислого калия. При содержании ионов SО3 розовый цвет исчезает.
Cl. Приливаем раствор нитрата серебра. При содержании ионов Cl появляется слабое помутнение.
NH4. К раствору воды добавляем сильно концентрированный раствор щёлочи и нагреваем. При наличии NH4 появляется запах аммиака.
Fe. Добавляем концентрированный раствор роданита калия. При наличии ионов Fe появляется розовый или красный цвет.
Фенол. К пробе воды добавляем 2-3 капли раствора хлорида железа. Если есть фенол, то проба окрашивается в фиолетовый цвет.
SО3. Прибавляем слабый раствор марганцовокислого калия. При содержании ионов SО3 розовый цвет исчезает.
Cl. Приливаем раствор нитрата серебра. При содержании ионов Cl появляется слабое помутнение.
NH4. К раствору воды добавляем сильно концентрированный раствор щёлочи и нагреваем. При наличии NH4 появляется запах аммиака.
Fe. Добавляем концентрированный раствор роданита калия. При наличии ионов Fe появляется розовый или красный цвет.
Фенол. К пробе воды добавляем 2-3 капли раствора хлорида железа. Если есть фенол, то проба окрашивается в фиолетовый цвет.
Слайд 11Вывод
Вода из природного источника не имеет вредных примесей и полностью пригодна
для питья. Вода из уличного водопровода имеет примеси ионов хлора (возможно это связано с дезинфекцией водопровода) и примеси ионов аммония (водонапорная башня находится возле молочной фермы и возможно поступление в воду отходов жизнедеятельности животных)
Слайд 12Литература
1. Шалашова М. М. Особенности организации образовательного процесса в условиях реализации
ФГОС // Справочник заместителя директора школы № 9, сентябрь, 2012. – С. 30-34
2. Морозов В.Е. Химия. 9 класс. Выпуск 3. Волгоград, 2007
3. Фадеев Г.А. Химия и экология, 8-11 классы, Волгоград,
4. Денисова В.Г., Химия 9 класс, Волгоград, 2006
5. Князев Р.Н., Артемьев В.П., задания по химии для учащихся малокомплектной школы, М, 1993
6. Пичугина Г. В. , Сорокина Н.В., Основы ведения крестьянского хозяйства, М, 2003
7. Пичугина Г. В. Химия в технологиях сельского хозяйства. М.: - 2003.
8. Титова И. М. Обучение химии. С-П.: Каро, - 2002
9. Ширшина Н. В. Химия для гуманитариев 10, 11 классы. В.: , - 2005.
2. Морозов В.Е. Химия. 9 класс. Выпуск 3. Волгоград, 2007
3. Фадеев Г.А. Химия и экология, 8-11 классы, Волгоград,
4. Денисова В.Г., Химия 9 класс, Волгоград, 2006
5. Князев Р.Н., Артемьев В.П., задания по химии для учащихся малокомплектной школы, М, 1993
6. Пичугина Г. В. , Сорокина Н.В., Основы ведения крестьянского хозяйства, М, 2003
7. Пичугина Г. В. Химия в технологиях сельского хозяйства. М.: - 2003.
8. Титова И. М. Обучение химии. С-П.: Каро, - 2002
9. Ширшина Н. В. Химия для гуманитариев 10, 11 классы. В.: , - 2005.