- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по биологии на тему Белки
Содержание
- 1. Презентация по биологии на тему Белки
- 2. Тема урока «Белки»
- 3. Цели и задачи урока:Установить зависимость между строением, химическими свойствами белков и их биологическими функциями.
- 4. «Жизнь есть способ существования белковых тел»
- 5. Проверка домашнего заданияБлок I «Решение
- 6. Блок II «Теоретический» по теме «Химический состав
- 7. Проверка домашнего заданияБлок II «Теоретический» по теме
- 8. Объяснение нового материала1.Строение молекул белков 2.Многообразие белков3.Аминокислоты 4.Пептидная связь5.Структура белковой молекулы 6.Свойства белков7.Выводы
- 9. Белки входят в состав всех клеток. Голландский
- 10. Скульптурная композиция, изображающая изящную пространственную структуру калиевого
- 11. Первой аминокислотой, открытой в живой природе, оказался
- 12. В чем проявляется многообразие белков? Благодаря чему белки выполняют различные функции в организме?
- 13. 1.Строение молекул белковБелки- наиболее существенный компонент живого.
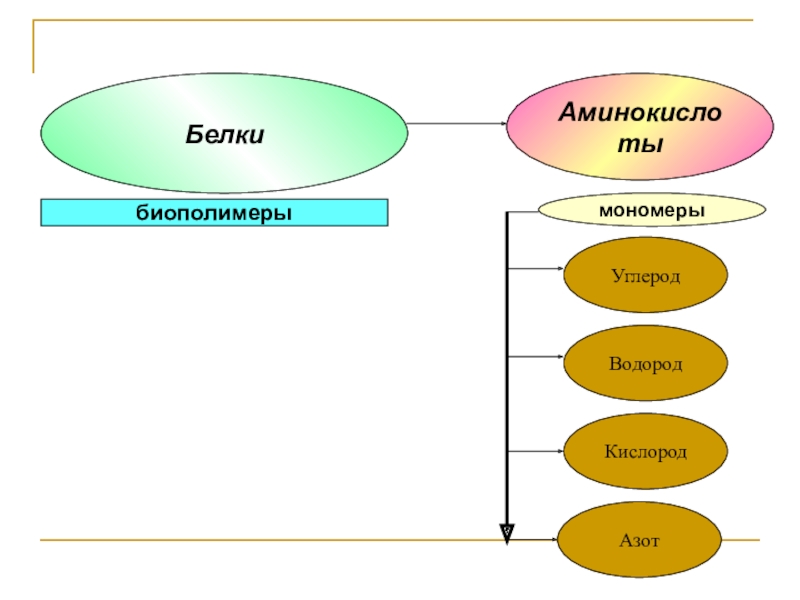
- 14. мономерыАминокислотыбиополимерыБелкиУглеродВодородАзотКислород
- 15. Мономеры белков – это аминокислоты. Двадцать природных
- 16. 2.Простые и сложные белки В зависимости
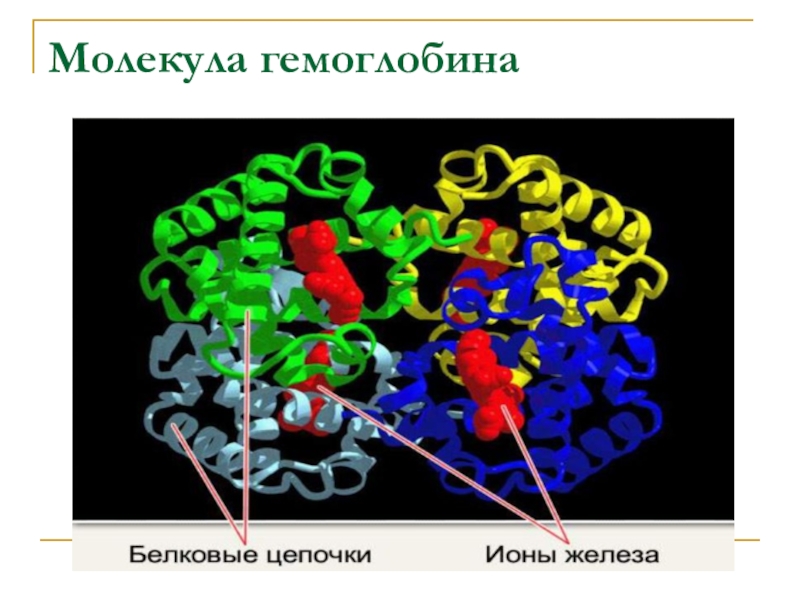
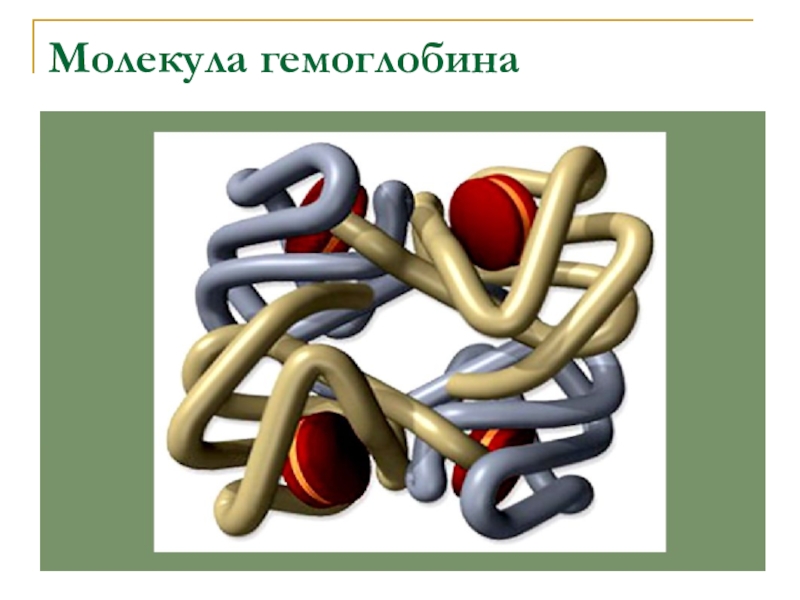
- 17. Молекула гемоглобина
- 18. 3. АминокислотыАминокислоты - бесцветные кристаллические вещества, растворимые
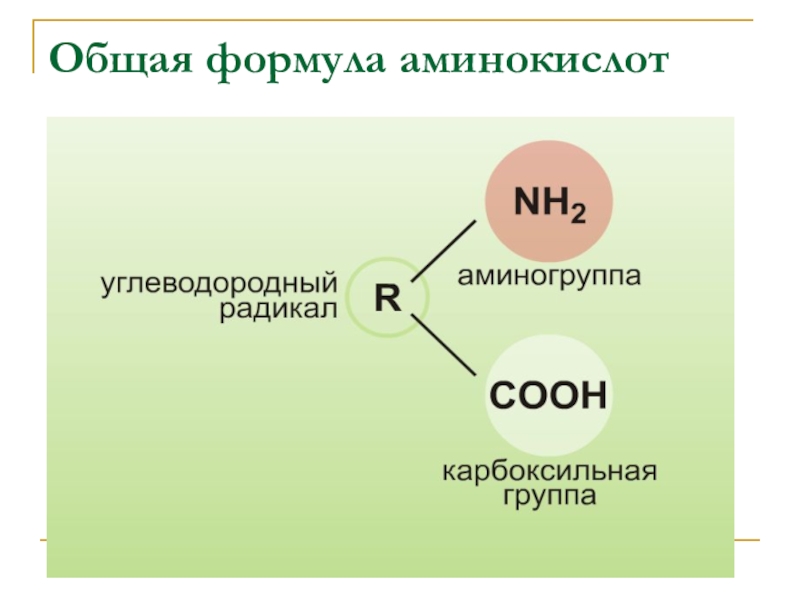
- 19. Общая формула аминокислот
- 20. Слайд 20
- 21. 5.Первичная структура белковой молекулы Макромолекула белка
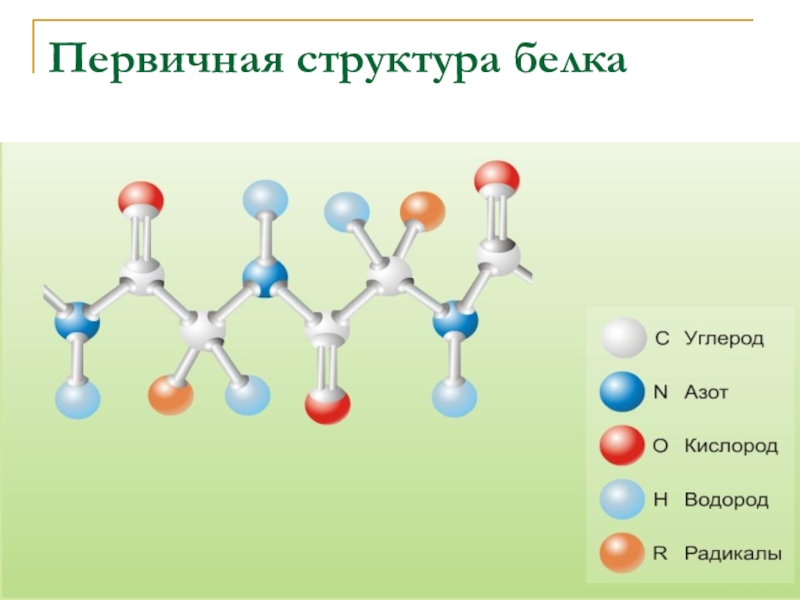
- 22. Первичная структура белка
- 23. Вторичная структура белковой молекулы Вторичная структура
- 24. Вторичная структура белковой молекулы
- 25. Третичная структура белковой молекулы Третичная структура
- 26. Четвертичная структура молекулы белкаЧетвертичная структура – взаимное
- 27. Молекула гемоглобина
- 28. 6.Свойства белков Естественное состояние белка называется
- 29. Типы денатурацииДенатурация бывает частичной и полной. При
- 30. Лабораторная работа Опыт №1. Белок + нагревание
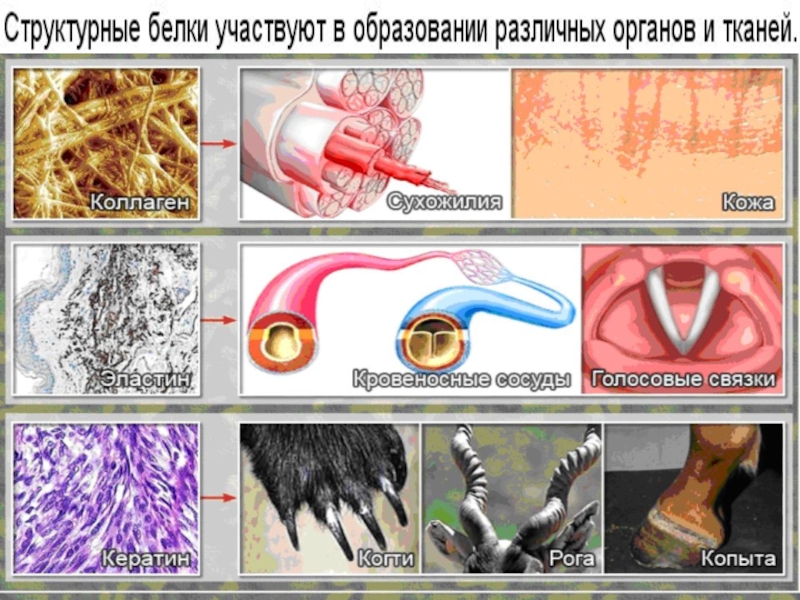
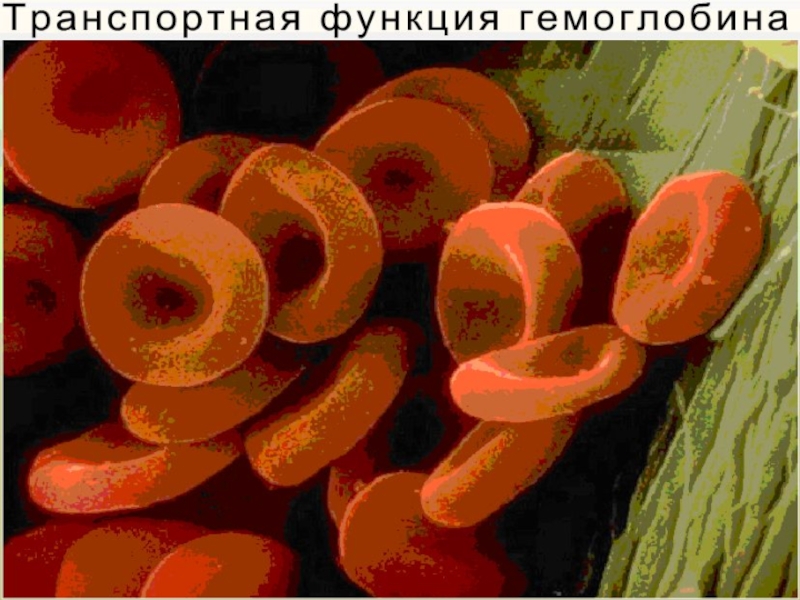
- 31. Функции белков
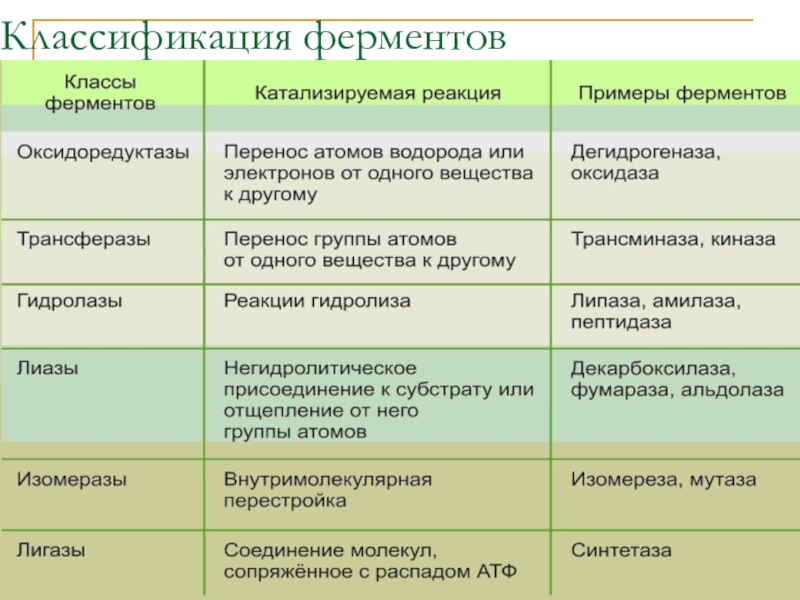
- 32. Классификация ферментов
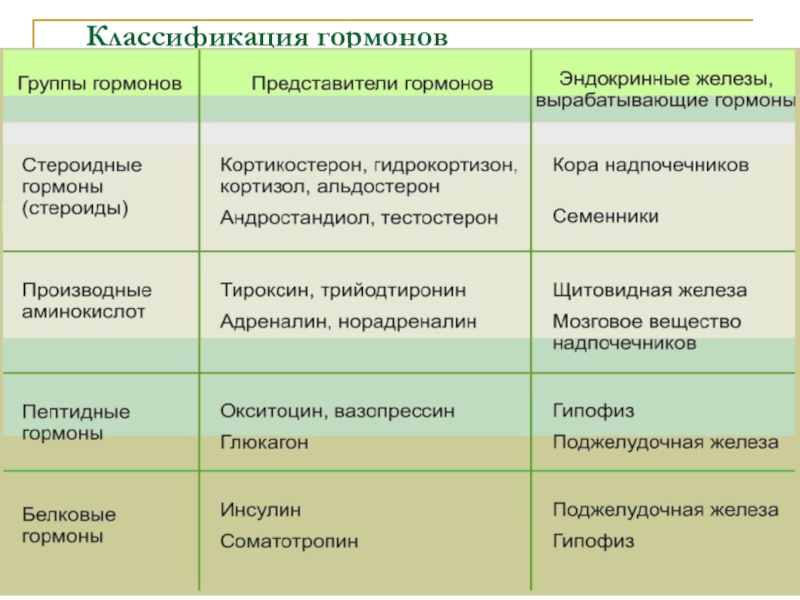
- 33. Классификация гормонов
- 34. Слайд 34
- 35. Слайд 35
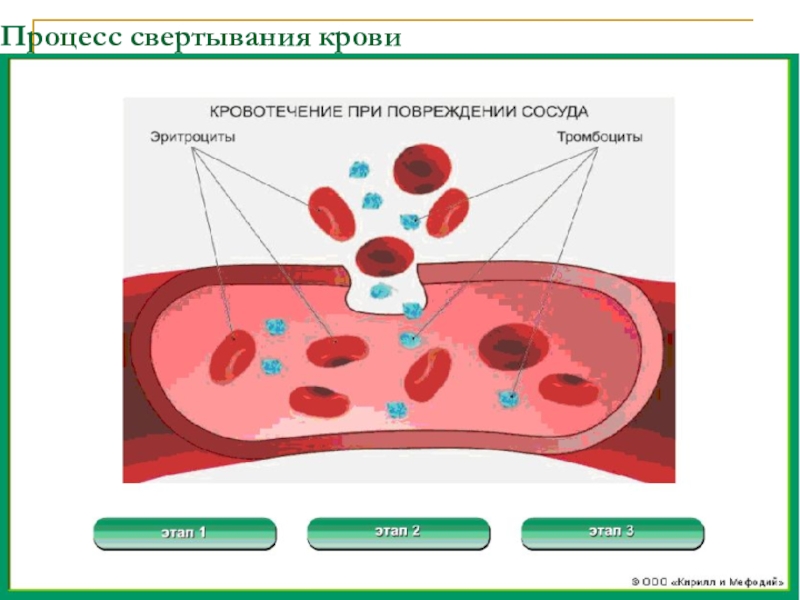
- 36. Процесс свертывания крови
- 37. Семена бобовых содержат большое количество растительных веществ
- 38. 7.ВыводыКлетки содержат тысячи различных белков.Белки обладают видовой
- 39. Повторение и закрепление знанийI. Допишите фразу:1. Природные
- 40. II. Верно или нет данное утверждение ?
- 41. Домашнее задание1. Лекция № 6.2. §§ 7,
- 42. Благодарю всех за хорошую работу!
Тема урока «Белки»
Слайд 3Цели и задачи урока:
Установить зависимость между строением, химическими свойствами белков и
их биологическими функциями.
Слайд 5 Проверка домашнего задания
Блок I «Решение задач по молекулярной биологии»:
1 тип. Фрагмент одной цепи ДНК имеет следующий состав: Т-А-Г-Т-Ц-Ц-А-Т-А-А-Г-Г
Достройте вторую цепь. Найдите : длину цепи; массу фрагмента ДНК; процентный состав каждого нуклеотида.
2 тип. Дана молекула ДНК, количество адениновых нуклеотидов составляет 300, а гуаниновых – 450. Определите длину данного фрагмента и процентный состав каждого нуклеотида.
Слайд 6Блок II «Теоретический» по теме «Химический состав клетки»
1. Найдите пару:
1- Анатомия 2- Психология 3- Валеология
4- Цитология
4- Цитология
А- Наука, изучающая строение клетки.
Б- Наука, изучающая строение организма, его органов и тканей.
В- Наука, изучающая закономерности психических процессов человека, его поведение.
Г- Наука о здоровом образе жизни.
Слайд 7Проверка домашнего задания
Блок II «Теоретический» по теме «Химический состав клетки»
2. Разбить
на логические группы:
1- Вода 6- Углекислый газ
2- ДНК, РНК 7- Хитин
3- Крахмал 8- Ретинол (А)
4- Глюкоза 9- Кислород
5- Хлорид натрия 10- Аскорбиновая
кислота (С)
1- Вода 6- Углекислый газ
2- ДНК, РНК 7- Хитин
3- Крахмал 8- Ретинол (А)
4- Глюкоза 9- Кислород
5- Хлорид натрия 10- Аскорбиновая
кислота (С)
Слайд 8Объяснение нового материала
1.Строение молекул белков
2.Многообразие белков
3.Аминокислоты
4.Пептидная связь
5.Структура белковой молекулы
6.Свойства белков
7.Выводы
Слайд 9Белки входят в состав всех клеток. Голландский ученый Мюльдер первый предугадал
их центральную роль в жизненных процессах и назвал эти соединения в 1838 году протеинами. В течение последующих 150 лет многие ученые проявляли большой интерес к исследованию белков, и поэтому к настоящему времени об их структуре и функциях известно много. Клетки различных типов содержат тысячи разных белков.
Слайд 10Скульптурная композиция, изображающая изящную пространственную структуру калиевого комплекса пептида валиномицина, украшает
лужайку перед главным входом в Институт биоорганической химии им. М.М. Шемякина и Ю.А. Овчинникова Российской Академии наук в Москве. Эта композиция олицетворяет большую работу, посвященную детальному изучению пептидного антибиотика, выполненную именно в этом институте
Слайд 11Первой аминокислотой, открытой в живой природе, оказался аспарагин (N). Его в
1806 г. выделили Луи Никола Воклен (1763–1829) и Пьер Жан Робике (1780–1840) во Франции. Открытие всех 20 стандартных аминокислот длилось больше века и завершилось лишь в 1937 г. открытием треонина (Т).
Первым ученым, внесшим весомый вклад в установление химической природы белков, был выдающийся немецкий химик-органик Герман Эмиль Фишер (1852–1919), который в 1902 г. открыл то, что аминокислоты в белках соединены пептидными связями.
Первым ученым, внесшим весомый вклад в установление химической природы белков, был выдающийся немецкий химик-органик Герман Эмиль Фишер (1852–1919), который в 1902 г. открыл то, что аминокислоты в белках соединены пептидными связями.
Слайд 12В чем проявляется многообразие белков?
Благодаря чему белки выполняют различные функции
в организме?
Слайд 131.Строение молекул белков
Белки- наиболее существенный компонент живого. Ни один процесс, происходящий
в живой клетке, не обходится без их участия.
Молекулы белков очень крупные в сравнении с другими органическими соединениями.
Молекулярная масса белков огромна.
Белки самые сложные среди органических соединений.
Белки являются полимерами.
Молекулы белков очень крупные в сравнении с другими органическими соединениями.
Молекулярная масса белков огромна.
Белки самые сложные среди органических соединений.
Белки являются полимерами.
Слайд 15Мономеры белков – это аминокислоты. Двадцать природных аминокислот состоят из углерода,
водорода, кислорода и азота. Две аминокислоты, участвующих в построении белков, содержат также серу.
Линейные молекулы белков образуются благодаря соединению аминокислот друг с другом. Известно несколько коротких белков, состоящих из 3-8 аминокислот, и очень длинных белков из 1500 аминокислот.
Линейные молекулы белков образуются благодаря соединению аминокислот друг с другом. Известно несколько коротких белков, состоящих из 3-8 аминокислот, и очень длинных белков из 1500 аминокислот.
Слайд 162.Простые и сложные белки
В зависимости от состава различают простые
и сложные белки.
Простые белки, или протеины состоят только из аминокислот.
Сложные белки (протеиды) содержат или липиды, или углеводы, или металлы. Например, в состав белка гемоглобина входят ионы железа.
Простые белки, или протеины состоят только из аминокислот.
Сложные белки (протеиды) содержат или липиды, или углеводы, или металлы. Например, в состав белка гемоглобина входят ионы железа.
Слайд 183. Аминокислоты
Аминокислоты - бесцветные кристаллические вещества, растворимые в воде. В природе
обнаружено свыше 170 разных аминокислот, но лишь 20 из них входят в состав белков.
Существование огромного многообразия белков обусловлено различной последовательностью соединения и числом входящих в них аминокислот.
Главное различие аминокислот состоит в строении боковых цепей- радикалов- R.
Существование огромного многообразия белков обусловлено различной последовательностью соединения и числом входящих в них аминокислот.
Главное различие аминокислот состоит в строении боковых цепей- радикалов- R.
Слайд 215.Первичная структура белковой молекулы
Макромолекула белка состоит из сотен аминокислотных
остатков. Каждому белку присущ определенный характер укладки. Молекулы белков различаются по своей структуре.
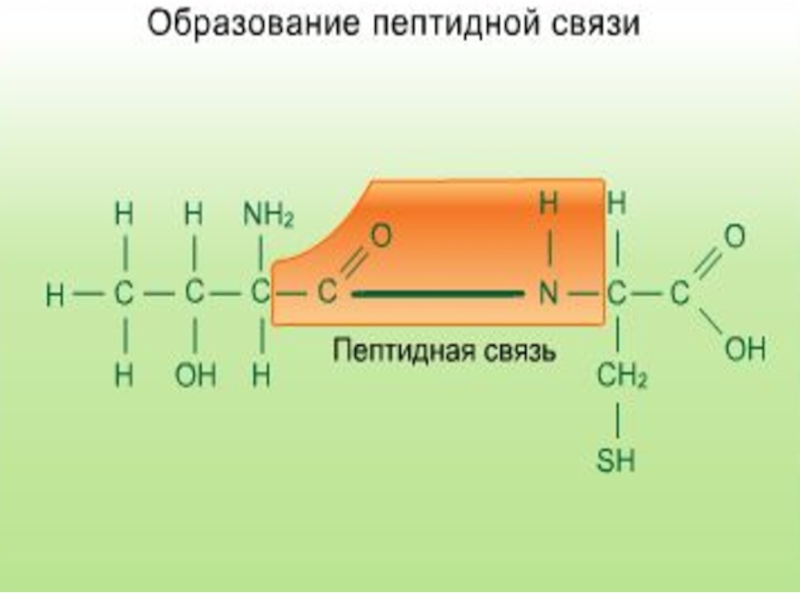
Первичная структура – это определенная последовательность расположения аминокислотных остатков в полипептидной цепи, соединенных пептидными связями.
Замена даже 1 аминокислотного звена другим в белковой молекуле изменяет ее свойства.
Первичная структура – это определенная последовательность расположения аминокислотных остатков в полипептидной цепи, соединенных пептидными связями.
Замена даже 1 аминокислотного звена другим в белковой молекуле изменяет ее свойства.
Слайд 23Вторичная структура белковой молекулы
Вторичная структура белка – это упорядоченное
строение полипептидных цепей, обусловленное водородными связями между группами С=О и N-H разных аминокислот. Вторичная структура имеет вид спирали.
Слайд 25Третичная структура белковой молекулы
Третичная структура белка – это пространственная
конфигурация полипептида, имеющего вторичную структуру, и обусловленная взаимодействиями между радикалами.
Слайд 26Четвертичная структура молекулы белка
Четвертичная структура – взаимное расположение в пространстве нескольких
одинаковых или разных полипептидных цепей, имеющих третичную структуру и составляющих белковую молекулу.
Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуноглобулин, инсулин.
Четвертичной структурой обладает около 5% белков, в том числе гемоглобин, иммуноглобулин, инсулин.
Слайд 286.Свойства белков
Естественное состояние белка называется нативным. Нарушение нативной структуры
молекул белков называют денатурацией. Во время денатурации свойства белка сильно изменяются.
Слайд 29Типы денатурации
Денатурация бывает частичной и полной. При частичной денатурации первичная структура
белковой молекулы сохраняется, и молекула белка может вновь принять естественную форму. При полной денатурации первичная структура разрушается, и белковая молекула не может вернуться в исходное состояние.
Вывод. Свойства белков зависят от его аминокислотного состава и структуры.
Вывод. Свойства белков зависят от его аминокислотного состава и структуры.
Слайд 30Лабораторная работа
Опыт №1. Белок + нагревание ---- денатурация (выпадение осадка)
Опыт
№2. Белок + СН3 СООН ---- денатурация (выпадение осадка)
Опыт №3. Белок + СuSO4 ---- денатурация (выпадение осадка)
Реакции, используемые для определения состава вещества, называются качественными.
Опыт №4. Ксантопротеиновая реакция.
Белок + HNO3 (конц) + нагрев ---- желтое окрашивание
Опыт №5. Биуретовая реакция.
Белок + СuSO4 + NaOH ---- фиолетовое окрашивание
СuSO4 + 2NaOH ---- Сu (OH)2 + Na2SO4
Белок + Сu (OH)2 ---- фиолетовое окрашивание
Опыт №3. Белок + СuSO4 ---- денатурация (выпадение осадка)
Реакции, используемые для определения состава вещества, называются качественными.
Опыт №4. Ксантопротеиновая реакция.
Белок + HNO3 (конц) + нагрев ---- желтое окрашивание
Опыт №5. Биуретовая реакция.
Белок + СuSO4 + NaOH ---- фиолетовое окрашивание
СuSO4 + 2NaOH ---- Сu (OH)2 + Na2SO4
Белок + Сu (OH)2 ---- фиолетовое окрашивание
Слайд 387.Выводы
Клетки содержат тысячи различных белков.
Белки обладают видовой специфичностью.
Белки состоят из остатков
аминокислот, соединяющихся пептидными связями.
Различают простые и сложные белки.
Молекулы белков имеют первичную, вторичную, третичную, четвертичную структуры.
Белки выполняют разнообразные функции в организме, которые определяются особенностями строения их молекул.
Различают простые и сложные белки.
Молекулы белков имеют первичную, вторичную, третичную, четвертичную структуры.
Белки выполняют разнообразные функции в организме, которые определяются особенностями строения их молекул.
Слайд 39Повторение и закрепление знаний
I. Допишите фразу:
1. Природные полимеры, мономерами которых являются
аминокислоты, называются … .
2. Уровнями организации белковой молекулы являются … .
3. Между аминокислотами в первичной структуре возникают … связи.
4. Нарушение нативной структуры молекул белков называют … .
5. Основными функциями белков являются … .
2. Уровнями организации белковой молекулы являются … .
3. Между аминокислотами в первичной структуре возникают … связи.
4. Нарушение нативной структуры молекул белков называют … .
5. Основными функциями белков являются … .
Слайд 40II. Верно или нет данное утверждение ?
1. В состав белков входят
аминокислоты, прочно связанные между собой водородными связями.
2. Белок – макромолекула.
3. Белки составляют основную часть органических веществ клетки.
4. Белок – мономер.
5. катализаторы клетки – это белки.
2. Белок – макромолекула.
3. Белки составляют основную часть органических веществ клетки.
4. Белок – мономер.
5. катализаторы клетки – это белки.
Слайд 41Домашнее задание
1. Лекция № 6.
2. §§ 7, стр. 33- 38.
3. Составить
кроссворд по теме «Белки».
4. Придумать и решить задачи по теме «ДНК» 1 и 2 типа.
4. Придумать и решить задачи по теме «ДНК» 1 и 2 типа.