- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Разработка урока Обобщение и закрепление темы Металлы
Содержание
- 1. Разработка урока Обобщение и закрепление темы Металлы
- 2. Цели урока:Закрепить знания о положении металлов в
- 3. Вопросы для повторения:Где находятся металлы в таблице
- 4. Вопросы для повторения:Даны металлы: барий, кальций, бериллий.
- 5. Вопросы для повторения:Какая связь характерна для атомов
- 6. Вопросы для повторения:Назовите особенности атомов металлов.Какие химические свойства характерны для металлов?Напишите уравнения возможных реакций:
- 7. Уравнения возможных реакций:Cu + O2 → 2Cu + O2 → 2CuO
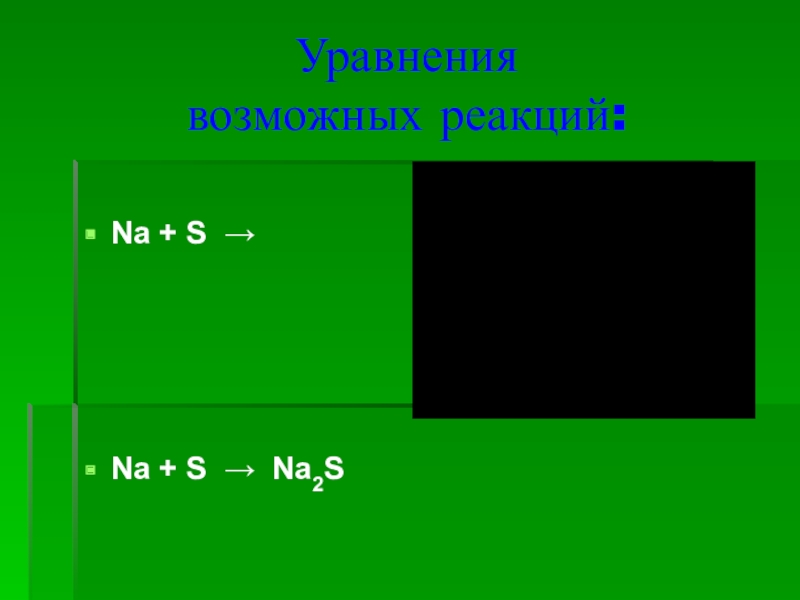
- 8. Уравнения возможных реакций:Na + S → Na + S → Na2S
- 9. Уравнения возможных реакций:Fe + CI2 → 2Fe + 3CI2 → 2FeCI3
- 10. Уравнения возможных реакций:Hg + H2O →
- 11. Уравнения возможных реакций:Cu + HNO3 →
- 12. Уравнения возможных реакций:Cu + HCI →
- 13. Уравнения возможных реакций:Сu + FeSO4 →Сu
- 14. Уравнения возможных реакций:Na + H2O → 2Na + 2H2O → 2NaOH + H2↑
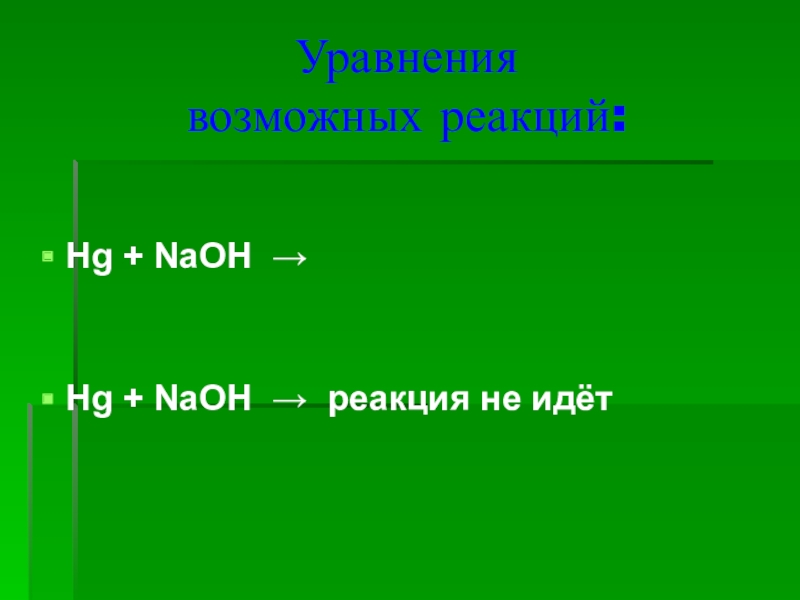
- 15. Уравнения возможных реакций:Hg + NaOH → Hg + NaOH → реакция не идёт
- 16. Уравнения возможных реакций:K + Br2 →2K + Br2 → 2KBr
- 17. Вопросы для повторения:Что называется коррозией? Какие виды
- 18. Уравнения возможных реакций:AI + СuO →2AI + 3CuO → AI2O3 + 3Cu
- 19. Уравнения возможных реакций:Cu + HgCl2 → Cu + HgCl2 → CuCl2 + Hg
- 20. Уравнения возможных реакций:
- 21. Уравнения возможных реакций:
- 22. Слайд 22
- 23. Проверочная работа
- 24. Домашнее задание:1. Повторить §§ 5 – 14 2. Решить
- 25. Домашнее задание:3. Написать уравнение реакции и расставить коэффициенты
- 26. Оцените урок и свою работу на урокеУрок
- 27. Спасибо за внимание!!!
Цели урока:Закрепить знания о положении металлов в таблице Д. И. Менделеева, их физических и химических свойствах, получении.Уметь писать уравнения реакций, характеризующих химические свойства и получение металлов.
Слайд 2Цели урока:
Закрепить знания о положении металлов в таблице Д. И. Менделеева,
их физических и химических свойствах, получении.
Уметь писать уравнения реакций, характеризующих химические свойства и получение металлов.
Уметь писать уравнения реакций, характеризующих химические свойства и получение металлов.
Слайд 3Вопросы для повторения:
Где находятся металлы в таблице Д. И. Менделеева?
Как изменяются
металлические (восстановительные) свойства в группе?
Как изменяются металлические (восстановительные) свойства в периоде?
Как изменяются металлические (восстановительные) свойства в периоде?
Слайд 4Вопросы для повторения:
Даны металлы: барий, кальций, бериллий.
Назовите самый активный металл.
Даны металлы:
барий, стронций, магний, калий.
Расположите эти металлы в порядке возрастания восстановительных свойств.
Слайд 5Вопросы для повторения:
Какая связь характерна для атомов металлов?
Какая связь характерна
для соединений металлов?
Какая кристаллическая решётка характерна для металлов?
Перечислите физические свойства металлов.
Какая кристаллическая решётка характерна для металлов?
Перечислите физические свойства металлов.
Слайд 6Вопросы для повторения:
Назовите особенности атомов металлов.
Какие химические свойства характерны для металлов?
Напишите
уравнения возможных реакций:
Слайд 13Уравнения
возможных реакций:
Сu + FeSO4 →
Сu + FeSO4 → реакция не
идёт
Fe + CuSO4 →
Fe + CuSO4 → FeSO4 + Cu
Fe + CuSO4 →
Fe + CuSO4 → FeSO4 + Cu
Слайд 17Вопросы для повторения:
Что называется коррозией?
Какие виды коррозии вы знаете?
Почему на
оцинкованном баке на месте царапины цинк разрушается, а железо не ржавеет?
Перечислите способы получения металлов.
Перечислите способы получения металлов.
Слайд 21Уравнения
возможных реакций:
Эл. ток
KI + H2O → раствор
Эл. ток
2KI + H2O → 2KOH + H2 + I2 раствор в р-ре К А
KI + H2O → раствор
Эл. ток
2KI + H2O → 2KOH + H2 + I2 раствор в р-ре К А
КиМ
Слайд 24Домашнее задание:
1. Повторить §§ 5 – 14
2. Решить задачу:
При взаимодействии железа с
20 г 10 %-ного раствора соляной кислоты выделилось 0,5 л водорода. Выразите этот выход водорода в процентах от теоретически возможного. Рассчитайте массу образовавшегося хлорида железа (II).
3. Написать уравнение реакции и расставить коэффициенты с помощью электронного баланса. Na + HNO3 → … + N2O + H2O
3. Написать уравнение реакции и расставить коэффициенты с помощью электронного баланса. Na + HNO3 → … + N2O + H2O
Слайд 25Домашнее задание:
3. Написать уравнение реакции и расставить коэффициенты с помощью электронного баланса.
Na
+ HNO3 → … + N2O + H2O
конц.
Слайд 26Оцените урок и свою работу на уроке
Урок не понравился, не узнал(а)
ничего нового
Урок прошел как обычно
Урок понравился, узнал(а) много нового