- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок -презентация Кислоты
Содержание
- 1. Урок -презентация Кислоты
- 2. «Считай несчастным тот день или
- 3. Взаимопроверка домашнего задания.Упражнение 1, с. 161.2Cu +
- 4. Упражнение 8, с. 162.SiO2 – оксид кремния
- 5. Что нас объединяет?
- 6. Кислый вкус лимону придает лимонная кислота, яблоку
- 7. План изучения темы:Состав, названия и определение кислот.Классификация кислот.Физические свойства кислот.Химические свойства кислот.
- 8. Кислоты.
- 9. СтранаКислотраздел Воспоминаний (состав, названия и определение кислот)
- 10. Антуан Лавуазье
- 11. Кислотами называются сложные вещества, молекулы которых состоят
- 12. СтранаКислотраздел Классификаций
- 13. Классификация кислотУксуснаяЛимоннаяЯблочнаяМуравьинаяHClH2SO4H3PO4H2CO3H2SiO3НеорганическиеОрганические
- 14. По какому признаку кислоты разделены на группы?Design Inc.Contents 1Contents 2
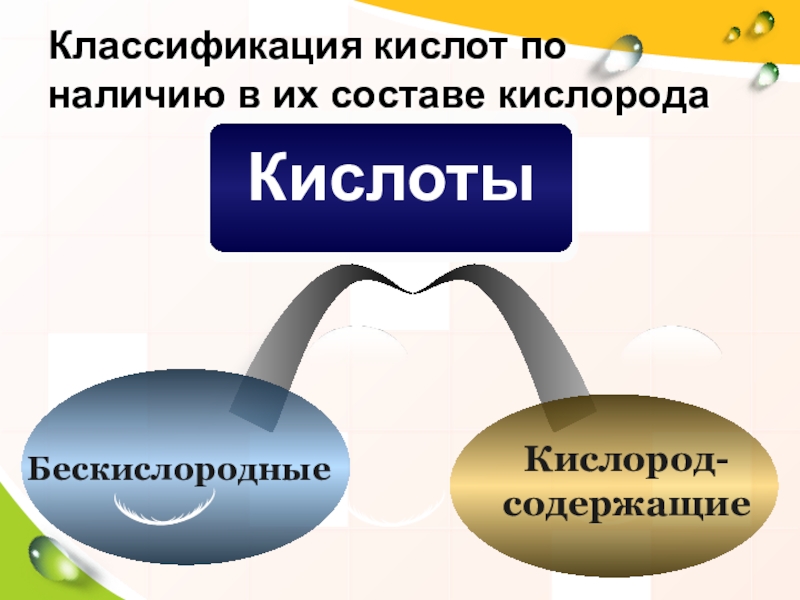
- 15. Классификация кислот по наличию в их составе кислородаКислород-содержащиеБескислородные
- 16. По какому признаку кислоты разделены на группы?HF
- 17. ОдноосновныеHCl, HNO3ДвухосновныеH2SO4,H2SiO3ТрехосновныеH3PO4Классификация кислот по числу атомов водорода.Кислоты
- 18. Работаем с тестом
- 19. СтранаКислот раздел Физический (свойства)
- 20. Физические свойства кислотПо агрегатному состоянию:Газообразные
- 21. Кремниевая кислотаH2SiO3Единственная нерастворимая кислотаОна соответ-ствует кислот- ному оксиду - SiO2
- 22. ФизкультминуткаЛ. Бетховен - К Элизе (Fur Elise) (1 часть).mp4
- 23. СтранаКислот раздел Химический (свойства)
- 24. ПРАВИЛА БЕЗОПАСНОСТИЕдкое вещество—кислота! Разрушает и раздражает кожу,
- 25. Химические свойства кислот. Кислоты…1). Изменяют окраску
- 26. Взаимодействие с индикаторамиПомни! Нерастворимые кислоты не меняют окраску индикаторов.
- 27. Взаимодействие с солямиВзаимодействие кислот с солями.wmv
- 28. Взаимодествие с солями
- 29. Кислоты реагируют с солями, если образуется осадок или газ.
- 30. 2004200520062007МехОуМе(ОН)хМе
- 31. Д/З § 37, у. 1, 3б, 4б, 5бг, 7 с. 165
- 32. Спасибо за урок!
«Считай несчастным тот день или тот час, в который ты не усвоил ничего нового и ничего не прибавил к своему образованию»
Слайд 2 «Считай несчастным тот день или тот час, в который
ты не усвоил ничего нового и ничего не прибавил к своему образованию»
Я. А. Коменский
Я. А. Коменский
Слайд 3Взаимопроверка домашнего задания.
Упражнение 1, с. 161.
2Cu + O2 = 2CuO (р.
соединения)
Cu(OH)2 = CuO + H2O (р. разложения)
или CuCO3 = CuO + CO2 (р.разложения)
Упражнение 2, с. 161.
ВаСО3 = ВаО + СО2
Карбонат бария оксид бария оксид углерода (IV)
Cu(OH)2 = CuO + H2O (р. разложения)
или CuCO3 = CuO + CO2 (р.разложения)
Упражнение 2, с. 161.
ВаСО3 = ВаО + СО2
Карбонат бария оксид бария оксид углерода (IV)
Слайд 4
Упражнение 8, с. 162.
SiO2 – оксид кремния (IV), песок, кремнезем не
растворяется в воде.
Ему соответствует кремниевая кислота - H2SiO3.
Ему соответствует кремниевая кислота - H2SiO3.
Слайд 6Кислый вкус лимону придает лимонная кислота, яблоку — яблочная кислота, скисшему
молоку — молочная кислота. Щавель имеет кислый вкус благодаря наличию в его листьях щавелевой кислоты.
Слайд 7План изучения темы:
Состав, названия и определение кислот.
Классификация кислот.
Физические свойства кислот.
Химические свойства
кислот.
Слайд 11Кислотами называются сложные вещества, молекулы которых состоят из атомов водорода и
кислотных остатков.
HCl – хлороводородная
H2SO4 – серная
H3PO4 - фосфорная
Слайд 13Классификация кислот
Уксусная
Лимонная
Яблочная
Муравьиная
HCl
H2SO4
H3PO4
H2CO3
H2SiO3
Неорганические
Органические
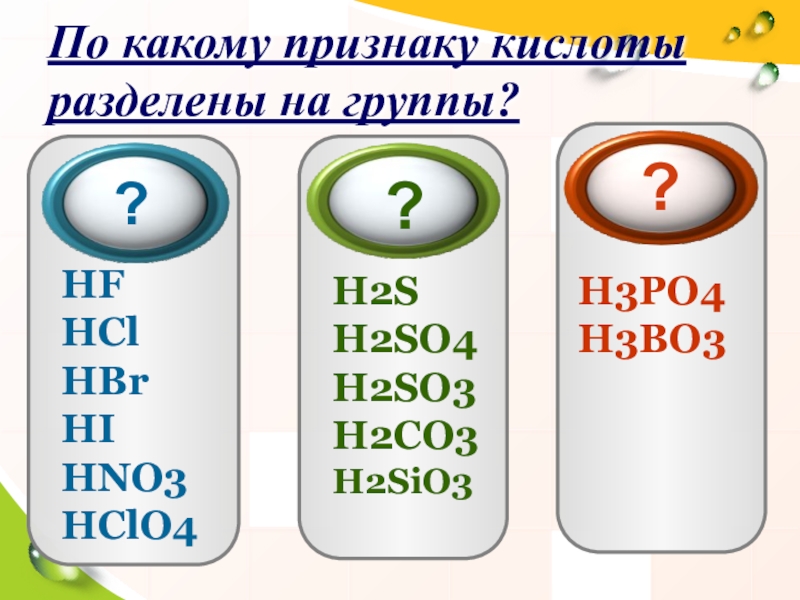
Слайд 16По какому признаку кислоты разделены на группы?
HF
HCl
HBr
HI
HNO3
HClO4
H2S
H2SO4
H2SO3
H2CO3
H2SiO3
H3PO4
H3BO3
?
?
?
Слайд 17
Одноосновные
HCl, HNO3
Двухосновные
H2SO4,H2SiO3
Трехосновные
H3PO4
Классификация кислот по числу атомов водорода.
Кислоты
Слайд 20Физические свойства кислот
По агрегатному
состоянию:
Газообразные (HCl, H2S)
Жидкие (HNO3, H2SO4)
Твердые
(H3PO4, H2SiO3)
Цвет кислот – ?
Запах – ?
Вкус – ?
Цвет кислот – ?
Запах – ?
Вкус – ?
Слайд 21Кремниевая кислота
H2SiO3
Единственная нерастворимая кислота
Она соответ-ствует кислот-
ному оксиду - SiO2
Слайд 24ПРАВИЛА БЕЗОПАСНОСТИ
Едкое вещество—кислота! Разрушает и раздражает кожу, слизистые оболочки.
Попавшие на кожу
капли раствора кислоты немедленно смойте сильной струей холодной воды, а затем обработайте поврежденную поверхность 2%-м раствором питьевой соды.
Слайд 25Химические свойства кислот.
Кислоты…
1). Изменяют окраску индикатора;
Взаимодействуют:
2).
с металлами;
3). с основными оксидами;
4). с основаниями;
5). с солями.
3). с основными оксидами;
4). с основаниями;
5). с солями.