- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Урок по химии на тему Непредельные углеводороды. Этилен (9 класс)
Содержание
- 1. Урок по химии на тему Непредельные углеводороды. Этилен (9 класс)
- 2. Цель урока:Обеспечить усвоение знаний об алкенах как
- 3. НОВЫЙ МАТЕРИАЛ УРОКА
- 4. Классификация углеводородов
- 5. Этилен - непредельный углеводород
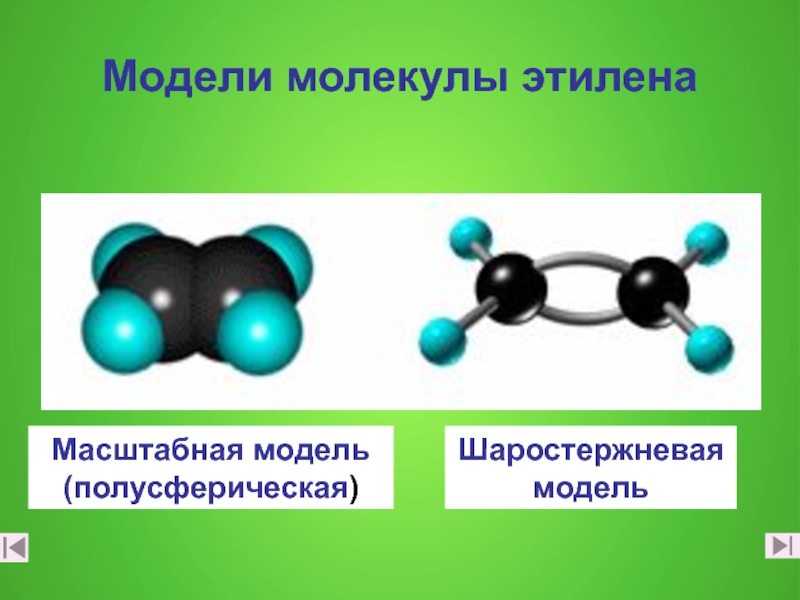
- 6. Модели молекулы этиленаМасштабная модель(полусферическая)Шаростержневая модель
- 7. Физические свойства
- 8. Этилен в природеэтилен содержится в коксовом газе
- 9. Химические свойства этилена
- 10. Уравнения реакций присоединенияСН2 = СН2 + Вr2
- 11. Взаимодействие этилена с перманганатом калияCН2 = CН2
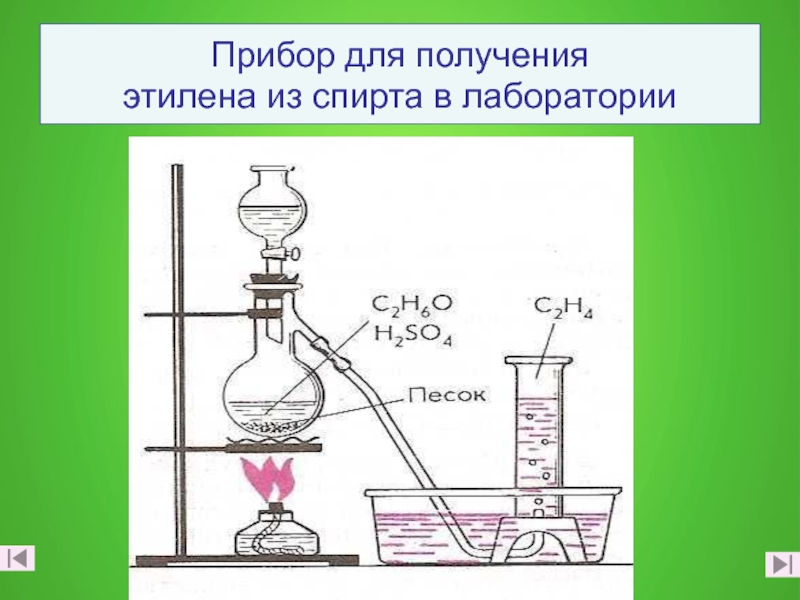
- 12. Прибор для получения этилена из спирта в лаборатории
- 13. Получение этилена
- 14. Горение этиленаC2Н4 + 3О2 ═> 2СО2
- 15. Завод по производству этилена мощностью 300 тыс. т/год
- 16. Комплекс производства этилена и его производных на
- 17. Установка производства этилена ОАО "Нижнекамскнефтехим" Мощность:
- 18. Установка производства этилена и полиэтилена ООО “Ново – Уренгойский” ГХК
- 19. Завод по производству этиленаЗавод «Этилен» является первым
- 20. Сферические газгольдеры - наземное газовое хранилище
- 21. Слайд 21
- 22. Слайд 22
- 23. Изделия из бутадиенового каучука
- 24. Выполните тестКачественной реакцией на непредельные углеводороды является:
- 25. Этилен можно получить из этана в результате реакции:а) дегидрирования;б) дегидратации;в) гидрирования;г) гидратацииВыполните тест
- 26. Выполните тестПолипропилен получают из вещества, формула которого:а) CH2=CH2; б) CH3-CH2-CH3; в) CH2=CH-CH3; г) CH2=C=CH2
- 27. Выполните тестС каким из перечисленных веществ не взаимодействует этилен: а)H2O; б)H2; в)Cl2; г)CH4.
- 28. Спасибо за внимание!
Слайд 2Цель урока:
Обеспечить усвоение знаний об алкенах как классе непредельных углеводородов, физико-химических
Слайд 7Физические свойства
газ ( при об. усл.)
Мr = 28
ρ = 1, 25 г /л ( при н.у.)
немного легче воздуха
tкип = - 103,7 0С
имеет слабый запах
малорастворим в воде
Этилен С2Н4
Слайд 8Этилен в природе
этилен содержится в коксовом газе (3 – 5 %)
этилен образуется в незначительных
количествах в тканях растений и животных как промежуточный продукт обмена веществ;
этилен используют для ускорения созревания
плодов, дефолиации растений, снижения преждевременного опадения плодов
Слайд 9Химические свойства
этилена
C2Н4 + 3О2 ═> 2СО2 + 2Н2О + Q
Этилен горит светящимся пламенем из - за
повышенного содержания углерода в нем
Светимость пламени вызывают
раскаленные частички угля, образующиеся
при распаде молекул этилена от нагревания
Раскаленные частицы угля полностью
сгорают в наружной части пламени
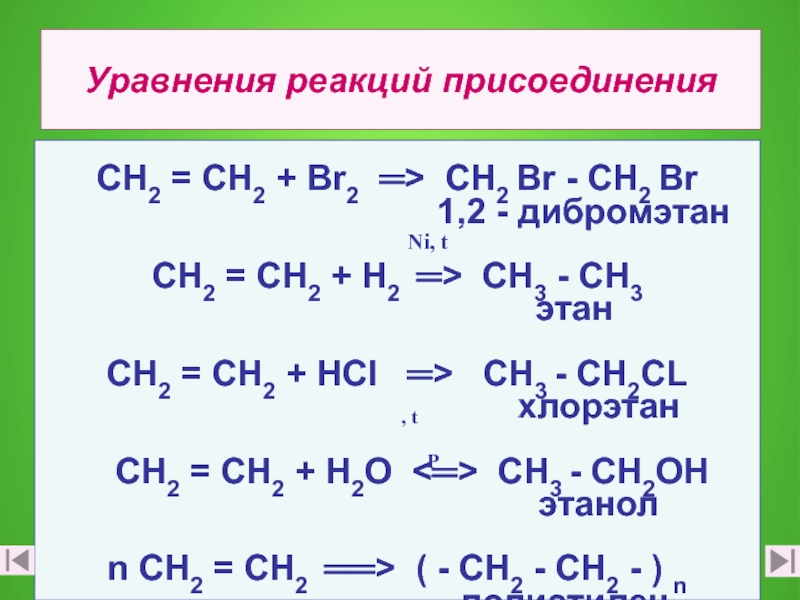
Слайд 10Уравнения реакций присоединения
СН2 = СН2 + Вr2 ═> СН2 Вr -
1,2 - дибромэтан
СН2 = СН2 + Н2 ═> СН3 - СН3
этан
СН2 = СН2 + НСl ═> СН3 - СН2CL
хлорэтан
СН2 = СН2 + Н2О <═> СН3 - СН2ОН
этанол
n СН2 = СН2 ══> ( - СН2 - СН2 - ) n
полиэтилен
Ni, t
, t
P
Слайд 11Взаимодействие этилена с перманганатом калия
CН2 = CН2 + Н -
Раствор перманганата калия обесцвечивается при пропускании через него этилена
р-р КМnО4
Подкисленный р-р КМnО4
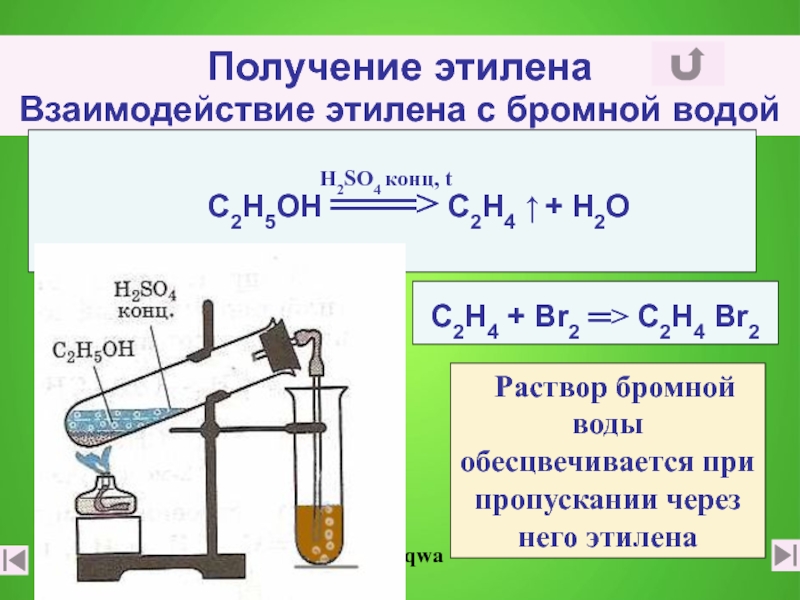
Слайд 13Получение этилена
С2Н4 + Вr2 ═> С2Н4 Вr2
С2Н5ОН ═══> C2Н4 ↑ + Н2О
Раствор бромной воды обесцвечивается при пропускании через него этилена
Н2SO4 конц, t
Вr2 aqwa
Слайд 14Горение этилена
C2Н4 + 3О2 ═> 2СО2 + 2Н2О + Q
В
этилен горит светящимся
пламенем, что
обуславливается
повышенным содержанием
углерода
Слайд 16Комплекс производства этилена и его производных на базе углеводородного сырья
Комплекс
Слайд 17Установка производства этилена
ОАО "Нижнекамскнефтехим"
Мощность:
Дата ввода в эксплуатацию: 2008 год
Слайд 19Завод по производству этилена
Завод «Этилен» является первым в технологической цепочке ОАО
Слайд 24Выполните тест
Качественной реакцией на непредельные углеводороды является:
а) реакция горения;
б) взаимодействие
в) реакция гидратации;
г) обесцвечивание бромной воды.
Слайд 25Этилен можно получить из этана в результате реакции:
а) дегидрирования;
б) дегидратации;
в) гидрирования;
г)
Выполните тест
Слайд 26Выполните тест
Полипропилен получают из вещества, формула которого:
а) CH2=CH2;
б) CH3-CH2-CH3;
в)
г) CH2=C=CH2
Слайд 27Выполните тест
С каким из перечисленных веществ не взаимодействует этилен:
а)H2O;
б)H2;
в)Cl2;
г)CH4.








![Урок по химии на тему Непредельные углеводороды. Этилен (9 класс) Взаимодействие этилена с перманганатом калияCН2 = CН2 + Н - ОН Взаимодействие этилена с перманганатом калияCН2 = CН2 + Н - ОН + [ О ] ═>](/img/tmb/1/57078/e68ad884860ec8e3674195b8a4d5c4f9-800x.jpg)