- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Соли, их классификация
Содержание
- 1. Соли, их классификация
- 2. Соли – это класс химических соединений, состоящих из ионов металла и ионов кислотного остатка.
- 3. Соли – электролиты, которые при диссоциации образуют катионы металла (или аммония NH4+) и анионы кислотных остатков.
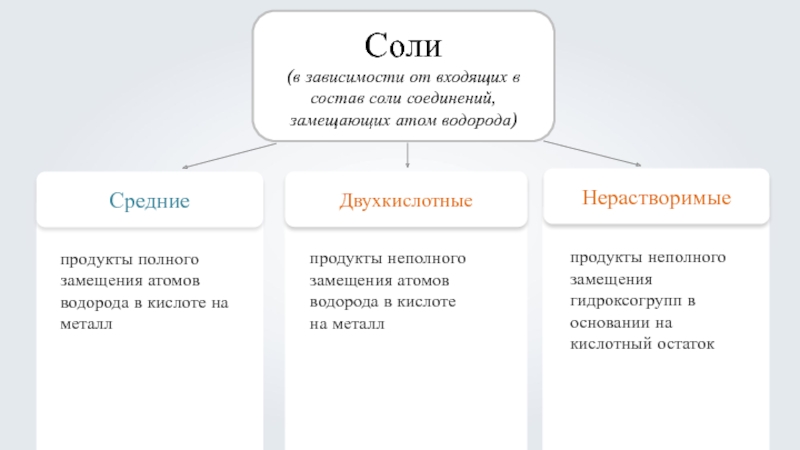
- 4. Соли(в зависимости от входящих в состав соли соединений, замещающих атом водорода)
- 5. Средние солиСредние соли – это продукты полного замещения атомов водорода в кислоте на металл. Карбонат натрия
- 6. Средние солиAl2(SO4)3 = 2Al3+ + 3SO42-анионыкислотного остатка
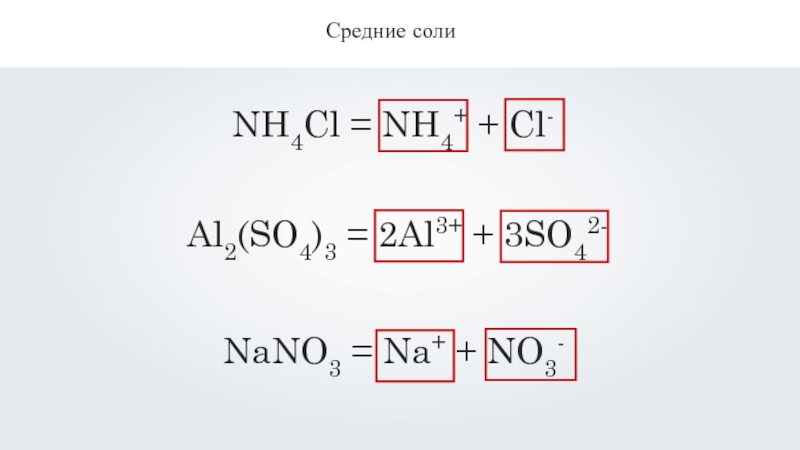
- 7. Средние солиNH4Cl = NH4+ + Cl- Al2(SO4)3 = 2Al3+ + 3SO42-NaNO3 = Na+ + NO3-
- 8. Кислые солиКислые соли – это продукты неполного
- 9. Кислые солиKH2PO4 = K+ + H2SO4- катионыметаллаанионыкислотного
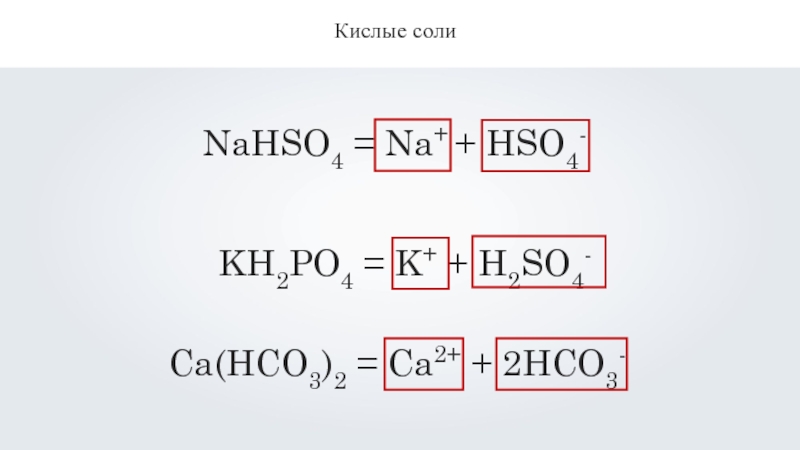
- 10. Кислые солиNaHSO4 = Na+ + HSO4- KH2PO4 = K+ + H2SO4- Ca(HCO3)2 = Ca2+ + 2HCO3-
- 11. Основные солиОсновные соли – это продукты неполного замещения гидроксогрупп в основании на кислотный остаток.Гидроксохлорид алюминия
- 12. Основные соли(CaOH)2SO4 = 2CaOH+ + SO42-атомы металла
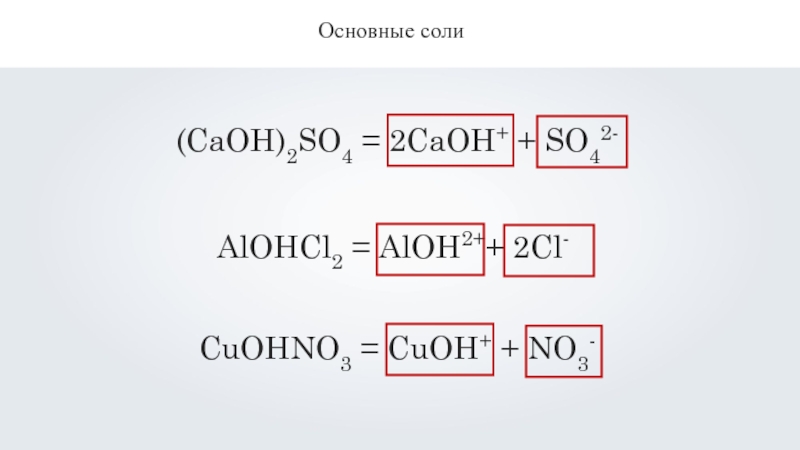
- 13. Основные соли(CaOH)2SO4 = 2CaOH+ + SO42-AlOHCl2 = AlOH2++ 2Cl- CuOHNO3 = CuOH+ + NO3-
- 14. Классификация солей и их электролитическая диссоциация основана
Соли – это класс химических соединений, состоящих из ионов металла и ионов кислотного остатка.
Слайд 2
Соли – это класс химических соединений, состоящих из ионов металла и
ионов кислотного остатка.
Слайд 3
Соли – электролиты, которые при диссоциации образуют катионы металла (или аммония
NH4+) и анионы кислотных остатков.
Слайд 5
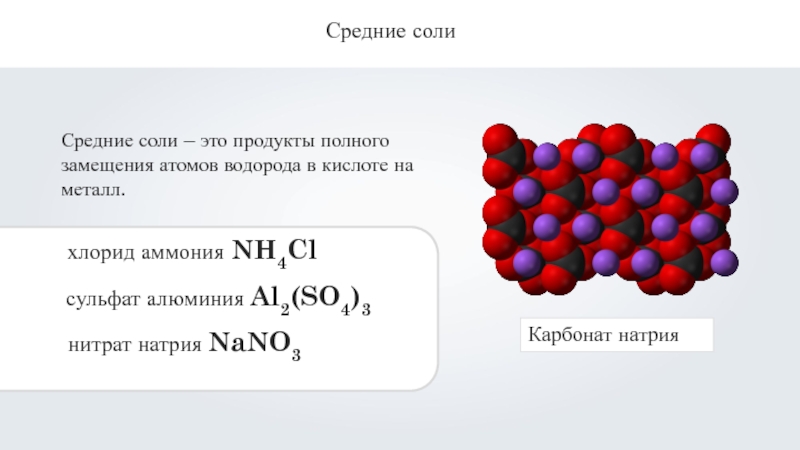
Средние соли
Средние соли – это продукты полного замещения атомов водорода в
кислоте на металл.
Карбонат натрия
Слайд 6
Средние соли
Al2(SO4)3 = 2Al3+ + 3SO42-
анионы
кислотного
остатка
катионы
металла
Связь катионов металла с
кислотным
остатком слабее, чем внутри аниона.
остатком слабее, чем внутри аниона.
Слайд 8
Кислые соли
Кислые соли – это продукты неполного замещения атомов водорода в
кислоте на металл.
гидрофосфат калия
K2HPO4
Слайд 9
Кислые соли
KH2PO4 = K+ + H2SO4-
катионы
металла
анионы
кислотного
остатка + водород
Связь
катионов металла с гидроанионом,
заместивших атом или атомы водорода в кислоте,
слабее, чем внутри гидроаниона.
заместивших атом или атомы водорода в кислоте,
слабее, чем внутри гидроаниона.
Слайд 11
Основные соли
Основные соли – это продукты неполного замещения гидроксогрупп в основании
на кислотный остаток.
Гидроксохлорид алюминия
Слайд 12
Основные соли
(CaOH)2SO4 = 2CaOH+ + SO42-
атомы металла
+ гидроксогруппа
анионы
кислотного
остатка
Связь
катионов металла с гидроксогруппой сильнее, чем с кислотным остатком, заместившим её.
Слайд 14
Классификация солей и их электролитическая диссоциация основана на их строении и
составе, то есть входящих в их состав катионов и анионов.