Каа-Хем. Гойчук Валентина Михайловна.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Серная кислота и её соли
Содержание
- 1. Серная кислота и её соли
- 2. «Просто знать ещё не всё, знания нужно
- 3. Цели урока.Ознакомить учащихся со свойствами серной кислоты.Рассмотреть свойства серной кислоты с точки зрения теории электролитической диссоциации.
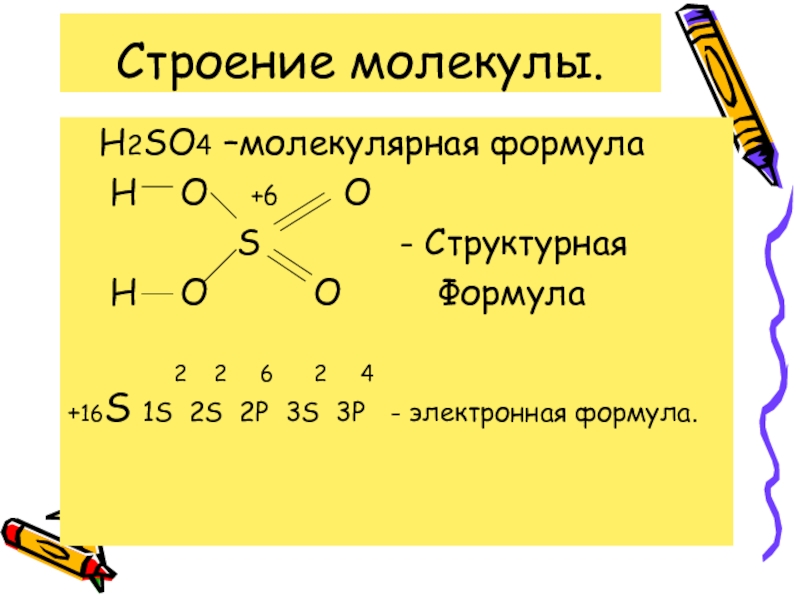
- 4. Строение молекулы. H2SO4 –молекулярная формула
- 5. Физические свойства.H2SO4 – жидкость, без цвета, без
- 6. Химические свойства серной кислоты.Диссоциирует:
- 7. Химические свойства серной кислоты.3. Взаимодействует со щелочами,
- 8. Химические свойства серной кислоты5. Взаимодействует с солями.Na2S
- 9. Соли серной кислоты.Сульфаты (средние соли): Na2SO4,
- 10. Поясните схему уравнениями химических реакций.
«Просто знать ещё не всё, знания нужно уметь использовать». Гёте
Слайд 3Цели урока.
Ознакомить учащихся со свойствами серной кислоты.
Рассмотреть свойства серной кислоты с
точки зрения теории электролитической диссоциации.
Слайд 4Строение молекулы.
H2SO4 –молекулярная формула
H O
+6 O
S - Структурная
H O O Формула
2 2 6 2 4
+16S 1S 2S 2P 3S 3P - электронная формула.
S - Структурная
H O O Формула
2 2 6 2 4
+16S 1S 2S 2P 3S 3P - электронная формула.
Слайд 5Физические свойства.
H2SO4 – жидкость, без цвета, без запаха, тяжёлая.
Правило разведения!
H2SO4
? в воду. Воду ? в H2SO4.
H2SO4 – сильный электролит.
H2SO4 – при взаимодействии с H2O образует гидраты.
H2SO4*xH2O
H2SO4 – сильный электролит.
H2SO4 – при взаимодействии с H2O образует гидраты.
H2SO4*xH2O
Слайд 6Химические свойства серной кислоты.
Диссоциирует:
+ _
I. H2SO4 ⬄ H + HSO4
_ + 2-
II. HSO4 ⬄ H + SO4
2. Взаимодействует с металлами:
Zn + H2SO4 = ZnSO4 + H2
0 _ 2+
Zn - 2e = Zn - восстановитель
+ _ 0
2H +2e =H2 - окислитель
I. H2SO4 ⬄ H + HSO4
_ + 2-
II. HSO4 ⬄ H + SO4
2. Взаимодействует с металлами:
Zn + H2SO4 = ZnSO4 + H2
0 _ 2+
Zn - 2e = Zn - восстановитель
+ _ 0
2H +2e =H2 - окислитель
Слайд 7Химические свойства серной кислоты.
3. Взаимодействует со щелочами, основаниями, амфотерными гидроксидами:
H2SO4 +
2NaOH = Na2SO4 + H2O
H2SO4 + Cu (OH)2 = CuSO4 + H2O
3 H2SO4 + 2 AI(OH)3 = AI2(SO4)3 + H2O
4. Взаимодействует с основными и амфотерными оксидами:
H2SO4 + Cu O = CuSO4 + H2O
H2SO4 + Zn O=ZnSO4 + H2O
H2SO4 + Cu (OH)2 = CuSO4 + H2O
3 H2SO4 + 2 AI(OH)3 = AI2(SO4)3 + H2O
4. Взаимодействует с основными и амфотерными оксидами:
H2SO4 + Cu O = CuSO4 + H2O
H2SO4 + Zn O=ZnSO4 + H2O
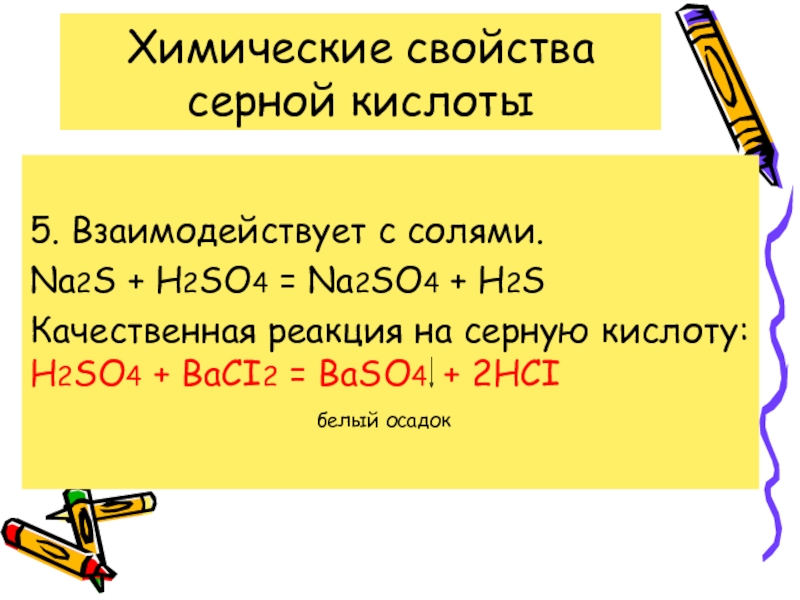
Слайд 8Химические свойства серной кислоты
5. Взаимодействует с солями.
Na2S + H2SO4 = Na2SO4
+ H2S
Качественная реакция на серную кислоту:
H2SO4 + BaCI2 = BaSO4 + 2HCI
белый осадок
Качественная реакция на серную кислоту:
H2SO4 + BaCI2 = BaSO4 + 2HCI
белый осадок
Слайд 9Соли серной кислоты.
Сульфаты (средние соли):
Na2SO4, CaSO4, Fe2(SO4)3,
AI2(SO4)3, FeSO4
2. Гидросульфаты (кислые соли):
NaHSO4, KHSO4, LiHSO4 и другие.
2. Гидросульфаты (кислые соли):
NaHSO4, KHSO4, LiHSO4 и другие.
Слайд 10Поясните схему уравнениями химических реакций.
H2SO4--------------->
Пары воды
Выбросы SO2 <---- O2
кислотный дождь
кислотный снег
Кислотные воды
Пары воды
Выбросы SO2 <---- O2
кислотный дождь
кислотный снег
Кислотные воды