- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Серная и сернистая кислоты
Содержание
- 1. Серная и сернистая кислоты
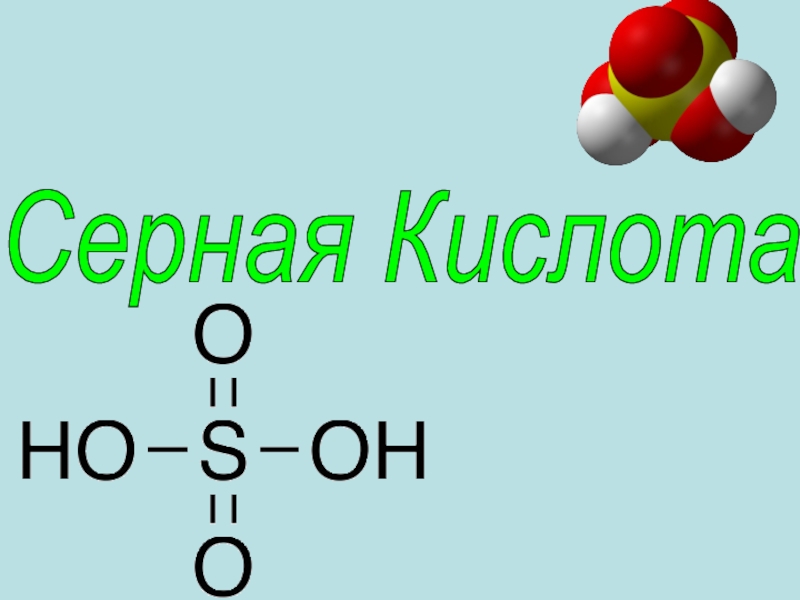
- 2. Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6)
- 3. ПрименениеСерную кислоту применяют:в производстве минеральных удобрений;как электролит
- 4. СвойстваВ концентрированном состоянии (безводном) состоянии - серная
- 5. Химические свойства серной кислоты - химическая реакция
- 6. Химические свойства серной кислоты - химическая реакция с оксидами металлов: H2SO4 + CuO = CuSO4 + H2O
- 7. Химические свойства серной кислоты - химическая реакция
- 8. Химические свойства серной кислоты химическая реакция с серой (кислота
- 9. Химические свойства серной кислоты- химическая реакция с
- 10. Сернистая Кислота
- 11. Сернистая КислотаСернистая кислота — неустойчивая слабая двухосновная неорганическая — неустойчивая
- 12. ПрименениеСернистую кислоту и её соли применяют как
- 13. Спасибо За Внимание
Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6)
Слайд 2Се́рная кислота́ H2SO4 — сильная двухосновная кислота, отвечающая высшей степени окисления серы (+6)
Слайд 3Применение
Серную кислоту применяют:
в производстве минеральных удобрений;
как электролит в свинцовых аккумуляторах;
для получения
различных минеральных кислот и солей;
в производстве химических волокон, красителей, дымообразующих и взрывчатых веществ;
в нефтяной, металлообрабатывающей, и др. отраслях промышленности;
в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513 (эмульгатор);
в промышленном органическом синтезе
в производстве химических волокон, красителей, дымообразующих и взрывчатых веществ;
в нефтяной, металлообрабатывающей, и др. отраслях промышленности;
в пищевой промышленности — зарегистрирована в качестве пищевой добавки E513 (эмульгатор);
в промышленном органическом синтезе
Слайд 4Свойства
В концентрированном состоянии (безводном) состоянии - серная кислота - бесцветная, дымящаяся
на воздухе (из-за паров), маслянистая жидкость с характерным запахом (Т кипения=338 °С). Она является очень сильным окислителем.
Это вещество обладает всеми свойствами кислот:
Слайд 5Химические свойства серной кислоты
- химическая реакция с металлами:
H2SO4 + Fe = FeSO4 +
H2;
2H2SO4 + Cu = CuSO4 + SO2 +2H2O - в этом случае кислота является концентрированной.
Слайд 6Химические свойства серной кислоты
- химическая реакция с оксидами металлов:
H2SO4 + CuO =
CuSO4 + H2O
Слайд 7Химические свойства серной кислоты
- химическая реакция с основаниями и щелочами
(или реакция нейтрализации)
H2SO4 + 2NaOH = Na2SO4 + 2H2O
Слайд 8Химические свойства серной кислоты
химическая реакция с серой (кислота - концентрированная, реакция -
при нагревании):
2H2SO4 + S = 3SO2 + 2H2O
Слайд 9Химические свойства серной кислоты
- химическая реакция с солями (например, со стиральной
содой Na2CO3):
H2SO4 + Na2CO3 = Na2SO4 + CO2 + H2O
Слайд 11Сернистая Кислота
Сернистая кислота — неустойчивая слабая двухосновная неорганическая — неустойчивая слабая двухосновная неорганическая кислота — неустойчивая слабая
двухосновная неорганическая кислота средней силы. Отвечает степени окисления серы +4. Химическая формула H2SO3
Слайд 12Применение
Сернистую кислоту и её соли применяют как восстановители, для беления шерстиСернистую кислоту
и её соли применяют как восстановители, для беления шерсти, шелкаСернистую кислоту и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлораСернистую кислоту и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальцияСернистую кислоту и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция используют для переработки древесины в так называемую сульфитную целлюлозуСернистую кислоту и её соли применяют как восстановители, для беления шерсти, шелка и других материалов, которые не выдерживают отбеливания с помощью сильных окислителей (хлора). Сернистую кислоту применяют при консервировании плодов и овощей. Гидросульфит кальция используют для переработки древесины в так называемую сульфитную целлюлозу (раствор гидросульфита кальция растворяет лигнин
обработанную таким образом древесину используют для получения бумаги)
обработанную таким образом древесину используют для получения бумаги)