Тема урока
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Расчеты с использованием понятий количество вещества, молярная масса, молярный объем газов, постоянная Авогадро.
Содержание
- 1. Расчеты с использованием понятий количество вещества, молярная масса, молярный объем газов, постоянная Авогадро.
- 2. Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов», «постоянная Авогадро»Тема урока
- 3. Сегодня мы должны узнать понятия «Количествовещества»,
- 4. ТестированиеI, 3 вариант – металлы
- 5. Слайд 5
- 6. Что за понятия?1. «количество вещества», 2. «моль», «постоянная Авогадро». 3. «молярный объем» 4. «молярная масса».
- 7. Слайд 7
- 8. Слайд 8
- 9. Значение молярной массы вещества определяется его качественным
- 10. Как вычислить моль? ν = m/M, либоν = V/Vm,
- 11. Слайд 11
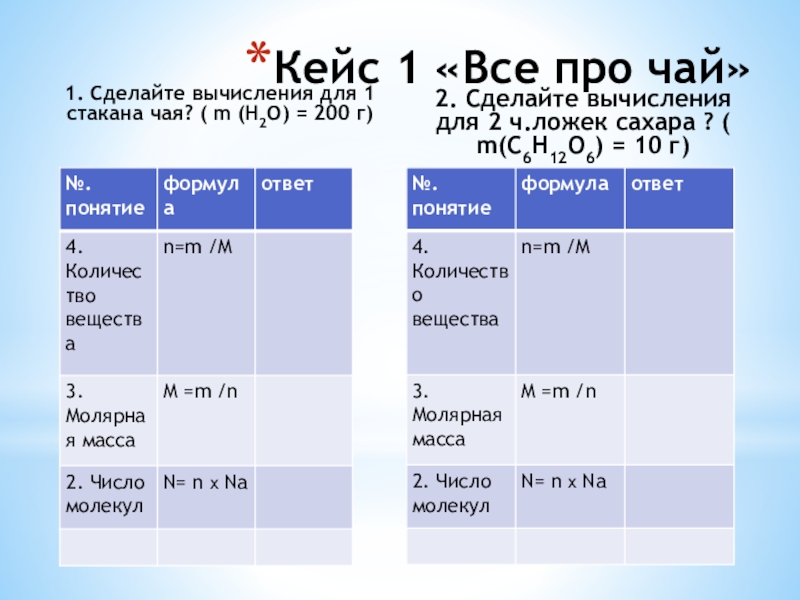
- 12. 1. Сделайте вычисления для 1 стакана чая?
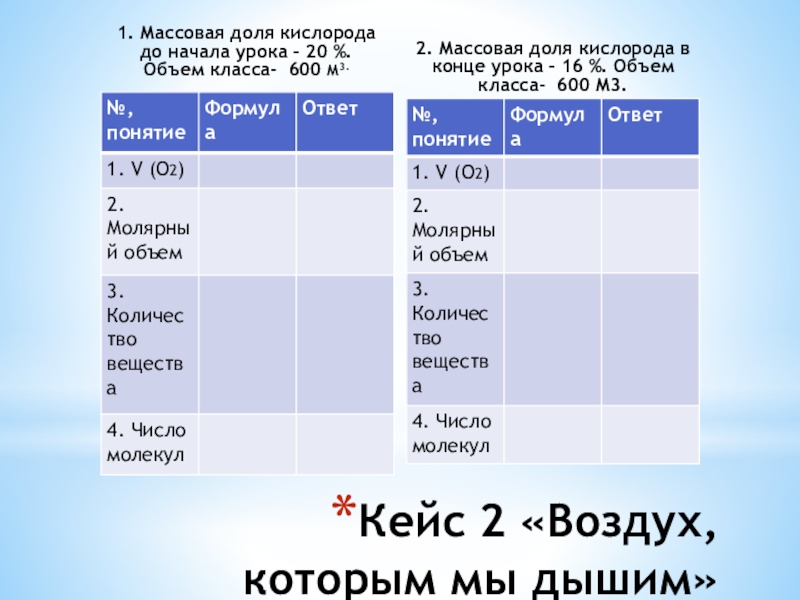
- 13. 1. Массовая доля кислорода до начала урока
- 14. Установите соотношение между названием и размерностью величиныНАЗВАНИЕ
- 15. Задание на дом§15, §16, читатьу. 1-3 с. 82Зад 3, РТ,с.72
- 16. Спасибо за урок!
Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов», «постоянная Авогадро»Тема урока
Слайд 2Расчеты с использованием понятий «количество вещества», «молярная масса», «молярный объем газов»,
«постоянная Авогадро»
Слайд 3Сегодня мы должны
узнать понятия «Количествовещества», «моль», «молярный объем», «постоянная Авогадро».
Уметь
производить расчеты по химическим формулам
Слайд 4Тестирование
I, 3 вариант – металлы
2, 4 вариант – неметаллы
Из приведенных ниже предложений выпишите только те, которые соответствуют; I вариант-металлам; II вариант- неметаллам.
1.Агрегатное состояние: твердое.
2. Электропроводны.
3.Ковкие.
4.Пластичные.
5.Имеют металлический блеск.
6.Не имеют металлического блеска.
7.Нетеплороводные.
8.Газообразные.
9.В твёрдом состоянии-хрупкие
Из приведенных ниже предложений выпишите только те, которые соответствуют; I вариант-металлам; II вариант- неметаллам.
1.Агрегатное состояние: твердое.
2. Электропроводны.
3.Ковкие.
4.Пластичные.
5.Имеют металлический блеск.
6.Не имеют металлического блеска.
7.Нетеплороводные.
8.Газообразные.
9.В твёрдом состоянии-хрупкие
Слайд 6Что за понятия?
1. «количество вещества»,
2. «моль», «постоянная Авогадро».
3.
«молярный объем»
4. «молярная масса».
4. «молярная масса».
Слайд 9Значение молярной массы вещества определяется его качественным и количественным составом, т.е.
зависит от Mr и Ar. Поэтому разные вещества при одинаковом количестве молей имеют различные массы m.
Слайд 10Как вычислить моль?
ν = m/M, либо
ν = V/Vm, где
ν – количество вещества, моль
m –
масса вещества, г
M – молярная масса вещества, г\моль
V – объем вещества, л
Vm – молярный объем, л\моль (молярный объем при нормальных условиях равен 22.4 л/моль)
M – молярная масса вещества, г\моль
V – объем вещества, л
Vm – молярный объем, л\моль (молярный объем при нормальных условиях равен 22.4 л/моль)
Слайд 121. Сделайте вычисления для 1 стакана чая? ( m (Н2О) =
200 г)
2. Сделайте вычисления для 2 ч.ложек сахара ? ( m(C6H12O6) = 10 г)
Кейс 1 «Все про чай»
Слайд 131. Массовая доля кислорода до начала урока – 20 %. Объем
класса- 600 М3.
2. Массовая доля кислорода в конце урока – 16 %. Объем класса- 600 М3.
Кейс 2 «Воздух, которым мы дышим»
Слайд 14Установите соотношение между названием и размерностью величины
НАЗВАНИЕ ВЕЛИЧИНЫ РАЗМЕРНОСТЬ
ВЕЛИЧИНЫ
А) КОЛИЧЕСТВО ВЕЩЕСТВА 1) Г/ МОЛЬ
Б) ОБЪЕМ 2) Г
В) МОЛЯРНАЯ МАССА 3) МОЛЬ
Г) МАССА ВЕЩЕСТВА 4) Л/МОЛЬ
5) МОЛЯРНЫЙ ОБЪЕМ 5) Л
А) КОЛИЧЕСТВО ВЕЩЕСТВА 1) Г/ МОЛЬ
Б) ОБЪЕМ 2) Г
В) МОЛЯРНАЯ МАССА 3) МОЛЬ
Г) МАССА ВЕЩЕСТВА 4) Л/МОЛЬ
5) МОЛЯРНЫЙ ОБЪЕМ 5) Л