Направление: естественнонаучное
Номинация: химии
Тема: «Выращивание кристаллов»
Работу выполнила:
Ревина Диана
ученица 8б класса
Руководитель:
Беляева Елена Михайловна,
учитель химии – биологии
Красный 2016
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Работа победителя районной научно-практической конференции Выращивание кристаллов
Содержание
- 1. Работа победителя районной научно-практической конференции Выращивание кристаллов
- 2. Актуальность исследования: Современной технике необходимы кристаллы высокой степени
- 3. Цель работы: провести исследование по выращиванию
- 4. Методы исследования:Накопление теоретического материала.Проведение опытно-экспериментальной деятельности с
- 5. Объект исследования: кристаллы. Предмет исследования : процесс кристаллизации.
- 6. Гипотеза исследования: мы предположили, что кристаллы могут появляться
- 7. Практическое значение:исследования состоит в том, что оно
- 8. Новизна исследования заключается в представлении выработанных рекомендаций юным исследователям по
- 9. Что такое кристалл? Кристалл - это
- 10. В природе существуют сотни веществ, образующих кристаллы.
- 11. Кристаллы могут иметь всевозможные формы: различных призм,
- 12. Кристаллическими считаются вещества, атомы которых расположены регулярно,
- 13. Существует три способа образования кристаллов: кристаллизация из
- 14. Большинство кристаллических тел являются поликристаллами, т.к. в
- 15. Применения кристаллов в науке и технике многочисленны
- 16. Благодаря своей исключительной твердости алмаз играет громадную
- 17. Ограненный алмаз является самым дорогим драгоценным камнем
- 18. Путь от алмаза до бриллианта долог и
- 19. Корунды.Скромный, невзрачный бурый корунд, непрозрачный, мелкий -
- 20. Рубин и сапфир относятся к самым красивым
- 21. Новая жизнь рубина - это лазер или
- 22. Вся часовая промышленность работает на искусственных рубинах.
- 23. Сапфир прозрачен, поэтому из него делают пластины
- 24. КварцКремень, аметист, яшма, опал, халцедон - все
- 25. Особенно удивительны электрические свойства кварца. Если сжимать
- 26. Опыт №1 Выращивание кристаллов медного купороса.Берем колбу
- 27. Фильтруем насыщенный раствор в чистую плоскодонную колбу.
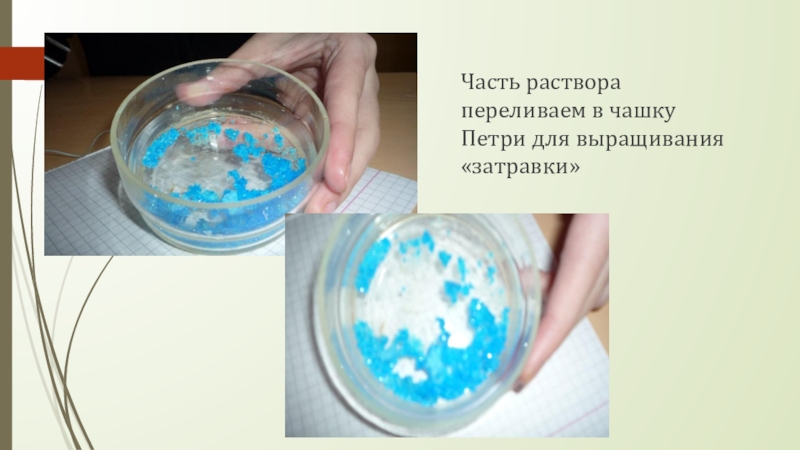
- 28. Часть раствора переливаем в чашку Петри для выращивания «затравки»
- 29. Выбираем из выросшей массы кристалликов один крупный кристалл.
- 30. Привязываем к кристаллу ниточку, получается кристаллик - «затравка»
- 31. После этого в стеклянную колбу опускаем «затравку».
- 32. И уже через пару дней мы видим,
- 33. Мы получили вот такие кристаллы медного купороса.
- 34. Опыт №2 Выращивание кристаллов поваренной соли. Растворяем в
- 35. Выбираем любой понравившийся более крупный кристаллик поваренной
- 36. Уже через пару дней можно заметить значительный для кристаллика рост. С каждым днём он будет увеличиваться.
- 37. Слайд 37
- 38. Результат:мы получили кристаллы поваренной соли и медного
- 39. Быстрее всего кристаллы могут образовываться в насыщенном
- 40. Выращивание кристаллов - очень интересный и увлекательный
- 41. Результаты моей работы можно использовать на уроках
- 42. Список литературы и интернет- ресурсы
Актуальность исследования: Современной технике необходимы кристаллы высокой степени чистоты, поэтому исследователи стремятся разработать методы искусственного выращивания монокристаллов различных веществ, а для большинства юных открывателей это увлекательное занятие, самое простое, доступное и недорогое, при этом образуются различные по
Слайд 2
Актуальность исследования: Современной технике необходимы кристаллы высокой степени чистоты, поэтому исследователи стремятся
разработать методы искусственного выращивания монокристаллов различных веществ, а для большинства юных открывателей это увлекательное занятие, самое простое, доступное и недорогое, при этом образуются различные по форме и цвету кристаллы в любое время года.
Слайд 3Цель работы:
провести исследование по выращиванию кристаллов поваренной
соли и медного купороса в лабораторных условиях.
Задачи исследования:
Проанализировать текстовый и иллюстративный материал по данной теме.
Изучить методики процесса кристаллизации.
Обобщить полученную информацию о строении кристалла.
Выполнить опытно-экспериментальную работу по изученным методикам.
Подготовить презентацию материала по теме исследования.
Задачи исследования:
Проанализировать текстовый и иллюстративный материал по данной теме.
Изучить методики процесса кристаллизации.
Обобщить полученную информацию о строении кристалла.
Выполнить опытно-экспериментальную работу по изученным методикам.
Подготовить презентацию материала по теме исследования.
Слайд 4Методы исследования:
Накопление теоретического материала.
Проведение опытно-экспериментальной деятельности с целью получения кристаллов из
поваренной соли и медного купороса.
Анализ полученных результатов исследования.
Анализ полученных результатов исследования.
Слайд 6Гипотеза исследования:
мы предположили, что кристаллы могут появляться при создании определенных условий;
значит, если изменить условия кристаллизации и растворить различные вещества, то можно получить кристаллы разной формы и цвета в лабораторных условиях.
Слайд 7Практическое значение:
исследования состоит в том, что оно может быть использовано на
уроках химии, окружающего мира, во внеклассных мероприятиях, занятиях кружка «Юный химик».
Слайд 8Новизна исследования
заключается в представлении выработанных рекомендаций юным исследователям по выращиванию кристаллов в лабораторных
условиях, которые способствуют повышению интереса, активности и самостоятельности в опытно-экспериментальной деятельности, а также познания мира младшими школьниками.
Слайд 9Что такое кристалл?
Кристалл - это твердое состояние вещества. Он
имеет определенную форму и определенное количество граней вследствие расположения своих атомов. Все кристаллы одного вещества имеют одинаковую форму, хоть и могут отличаться размерами.
Слайд 10В природе существуют сотни веществ, образующих кристаллы. Вода – одно из
самых распространенных из них. Замерзающая вода превращается в кристаллы льда или снежинки.Вы, конечно, обращали внимание на бесконечное разнообразие снежинок. Еще в 17 веке знаменитый астроном Иоганн Кеплер написал трактат «О шестиугольных снежинках», а спустя три столетия были изданы альбомы, в которых представлены коллекции увеличенных фотографий тысяч снежинок, причем ни одна из них не повторяет другую
.
Слайд 11
Кристаллы могут иметь всевозможные формы: различных призм, основанием которых могут быть
правильный треугольник, квадрат, параллелограмм и шестиугольник Кристаллы могут иметь и разные размеры. Некоторые минералы образуют кристаллы, которые разглядеть можно только с помощью микроскопа. Другие же образуют кристаллы, вес которых составляет несколько сотен фунтов.
Слайд 12Кристаллическими считаются вещества, атомы которых расположены регулярно, так, что образуют правильную
трёхмерную решётку, называемую кристаллической. Кристаллам ряда химических элементов и их соединений присущи замечательные механические, электрические, магнитные и оптические свойства.
Слайд 13Существует три способа образования кристаллов: кристаллизация из расплава, из раствора и
из газовой фазы.
Примером кристаллизации из расплава может служить образование льда из воды, а также образования вулканических пород, кристаллизация из раствора в природе - выпадение сотен миллионов тонн соли из морской воды.
При охлаждении газа (или пара) электрические силы притяжения объединяют атомы или молекулы в кристаллическое твёрдое вещество - так образуются снежинки.
Примером кристаллизации из расплава может служить образование льда из воды, а также образования вулканических пород, кристаллизация из раствора в природе - выпадение сотен миллионов тонн соли из морской воды.
При охлаждении газа (или пара) электрические силы притяжения объединяют атомы или молекулы в кристаллическое твёрдое вещество - так образуются снежинки.
Слайд 14Большинство кристаллических тел являются поликристаллами, т.к. в обычных условиях вырастить монокристаллы
достаточно сложно, этому мешают всевозможные примеси. Современная техника нуждается в кристаллах высокой степени чистоты, поэтому перед наукой встал вопрос о разработке эффективных методов искусственного выращивания монокристаллов различных химических элементов и их соединений.
Слайд 15Применения кристаллов в науке и технике многочисленны и разнообразны. Приведу несколько
примеров.
Алмаз.
Алмаз – это один из самых редких и дорогих в мире минералов. По химическому составу это чистый углерод, в котором все атомы встроены в идеально правильную кристаллическую решетку. Интересно, что такой же химический состав имеют и многие другие вещества, к примеру, уголь или графит, вот только атомарное строение у них совершенно другое.
Алмаз.
Алмаз – это один из самых редких и дорогих в мире минералов. По химическому составу это чистый углерод, в котором все атомы встроены в идеально правильную кристаллическую решетку. Интересно, что такой же химический состав имеют и многие другие вещества, к примеру, уголь или графит, вот только атомарное строение у них совершенно другое.
Слайд 16Благодаря своей исключительной твердости алмаз играет громадную роль в технике. Алмазными
пилами распиливают камни, бурят горные породы, используют в граверных инструментах, делительных машинах, сверлах для камня и металла.
Слайд 17Ограненный алмаз является самым дорогим драгоценным камнем - бриллиантом. Без этого
он не имеет и доли своей привлекательности.
Слайд 18Путь от алмаза до бриллианта долог и сложен, но в конце
из невзрачного камня получается сияющее чудо – идеальная драгоценность.
Слайд 19Корунды.
Скромный, невзрачный бурый корунд, непрозрачный, мелкий - наждак, которым чистят металл,
из которого делают наждачную шкурку. Корунд со всеми его разновидностями - это один из самых твердых камней на Земле, самый твердый после алмаза. Корундом можно сверлить, шлифовать, полировать, точить камень и металл. Из корунда и наждака делают точильные круги и бруски, шлифовальные порошки.
Слайд 20Рубин и сапфир относятся к самым красивым и самым дорогим из
драгоценных камней - это один и тот же минерал корунд. Разница лишь в цвете, которая возникла из-за очень малых примесей.
Слайд 21Новая жизнь рубина - это лазер или оптический квантовый генератор .
В 1960 году был создан первый лазер на рубине. Оказалось, что кристалл рубина усиливает свет. Лазер светит ярче тысячи солнц , его луч обладает громадный мощностью. Он легко прожигает листовой металл, сваривает металлические провода, сверлит тончайшие отверстия в твердых сплавах, алмазе. В глазной хирургии применяется чаще всего неодиновые лазеры и лазеры на рубине.
Слайд 22Вся часовая промышленность работает на искусственных рубинах. На полупроводниковых заводах тончайшие
схемы рисуют рубиновыми иглами. В текстильной и химической промышленности рубиновые нитеводители вытягивают нити из искусственных волокон, из капрона, из нейлона.
Слайд 23Сапфир прозрачен, поэтому из него делают пластины для оптических приборов. Основная
масса кристаллов сапфира идет в полупроводниковую промышленность.
Слайд 24Кварц
Кремень, аметист, яшма, опал, халцедон - все это разновидности кварца. Мелкие
зернышки кварца образуют песок. А самая красивая, самая чудесная разновидность кварца - это и есть горный хрусталь, т.е. прозрачные кристаллы кварца. Поэтому из прозрачного кварца делают линзы, призмы и другие детали оптических приборов.
Слайд 25Особенно удивительны электрические свойства кварца. Если сжимать или растягивать кристалл кварца,
на его гранях возникают электрические заряды. Это - пьезоэлектрический эффект в кристаллах. Пьезоэлектрические кристаллы широко применяются для воспроизведения, записи и передачи звука.
Слайд 26Опыт №1 Выращивание кристаллов медного купороса.
Берем колбу с водой, добавляем медный
купорос, тщательно перемешиваем до тех пор, пока он будет растворяться. Ёмкость с водой лучше всего постепенно подогревать для более быстрого растворения химиката. В процессе вода начнет менять цвет - от светло - голубого, до тёмно - синего.
Слайд 32И уже через пару дней мы видим, что на ниточку с
затравкой наросло множество маленьких кристалликов синего цвета.
Слайд 34Опыт №2 Выращивание кристаллов поваренной соли.
Растворяем в воде соль до тех
пор, пока она не будет растворяться, и станет оседать на дно стакана. Мы получили насыщенный раствор соли.
Отфильтровываем его в чистую колбу.
Отфильтровываем его в чистую колбу.
Слайд 35Выбираем любой понравившийся более крупный кристаллик поваренной соли, привязываем за ниточку
делаем такую же «затравку» и подвешиваем, чтобы он не касался стенок стакана.
Слайд 36Уже через пару дней можно заметить значительный для кристаллика рост. С
каждым днём он будет увеличиваться.
Слайд 38Результат:
мы получили кристаллы поваренной соли и медного купороса.
Выводы:
поваренная соль и медный
купорос состоят из кристаллов и при благоприятных условиях они принимают определенную форму ;
на форму кристаллов оказывает влияние температура;
кристаллы различных веществ имеют различные свойства (одни кристаллы окрашиваются, другие - бесцветны; одни кристаллы растут хорошо, другие плохо;
на форму кристаллов оказывает влияние температура;
кристаллы различных веществ имеют различные свойства (одни кристаллы окрашиваются, другие - бесцветны; одни кристаллы растут хорошо, другие плохо;
Слайд 39Быстрее всего кристаллы могут образовываться в насыщенном растворе поваренной соли и
медного купороса , когда в него помещается кристалл - «затравка».
В лабораторных условиях можно вырастить кристаллы при необходимых условиях: наличие насыщенного солевого раствора и небольшой кристаллической «затравки».
В лабораторных условиях можно вырастить кристаллы при необходимых условиях: наличие насыщенного солевого раствора и небольшой кристаллической «затравки».
Слайд 40Выращивание кристаллов - очень интересный и увлекательный процесс. В результате проведенных
исследований гипотеза полностью подтверждается: нам удалось вырастить кристаллы поваренной соли и медного купороса в лабораторных условиях.
Исследовательская работа мне очень понравилась. В ходе ее выполнения, я познакомилась со способами выращивания кристаллов. Узнала много интересного, познавательного. Но самое главное - самостоятельно вырастила кристаллы соли и медного купороса. Убедились на практике в том, что форма кристаллов бывает довольно разнообразной и это зависит от кристаллической решетки вещества.
Исследовательская работа мне очень понравилась. В ходе ее выполнения, я познакомилась со способами выращивания кристаллов. Узнала много интересного, познавательного. Но самое главное - самостоятельно вырастила кристаллы соли и медного купороса. Убедились на практике в том, что форма кристаллов бывает довольно разнообразной и это зависит от кристаллической решетки вещества.
Слайд 41Результаты моей работы можно использовать на уроках химии при изучении темы:
«Вещества аморфные и кристаллические», «Типы кристаллических решеток», а так же в кружковой работе и для привития интереса к изучению химии.
Слайд 42
Список литературы и интернет- ресурсы
1. Аликберова Л.Ю. Занимательная химия:
Книга для учащихся, учителей и родителей. М.: АСТ- ПРЕСС. 1999.
2. Большая детская энциклопедия: Химия / сост. К. Люцис. М.: Русское энциклопедическое товарищество. 2000.
3. Боровицкий П.И. Краткий справочник преподавателя естествознания. М.: Учпедгиз. 1951.
4. Девяткин В.В. Химия для любознательных или о чём не узнаешь на уроке. Ярославль: Академия Холдинг. 2000.
5. Леенсон И.А. Занимательная химия. М.: Дрофа. 1996.
6. Ф. Крегер «Химия несовершенных кристаллов», 1969
7 . В.С. Урусов «Теоретическая кристаллохимия», 1987
8. Энциклопедический словарь химика. М.: Педагогика. 1990.
Интернет-ресурсы:
http://www.zircon81.narod.ru/Metodica.html
http://www.waynesthisandthat.com/crystals.htm#fast - fast
http://www.crystalgrowing.com/index_e.htm
2. Большая детская энциклопедия: Химия / сост. К. Люцис. М.: Русское энциклопедическое товарищество. 2000.
3. Боровицкий П.И. Краткий справочник преподавателя естествознания. М.: Учпедгиз. 1951.
4. Девяткин В.В. Химия для любознательных или о чём не узнаешь на уроке. Ярославль: Академия Холдинг. 2000.
5. Леенсон И.А. Занимательная химия. М.: Дрофа. 1996.
6. Ф. Крегер «Химия несовершенных кристаллов», 1969
7 . В.С. Урусов «Теоретическая кристаллохимия», 1987
8. Энциклопедический словарь химика. М.: Педагогика. 1990.
Интернет-ресурсы:
http://www.zircon81.narod.ru/Metodica.html
http://www.waynesthisandthat.com/crystals.htm#fast - fast
http://www.crystalgrowing.com/index_e.htm