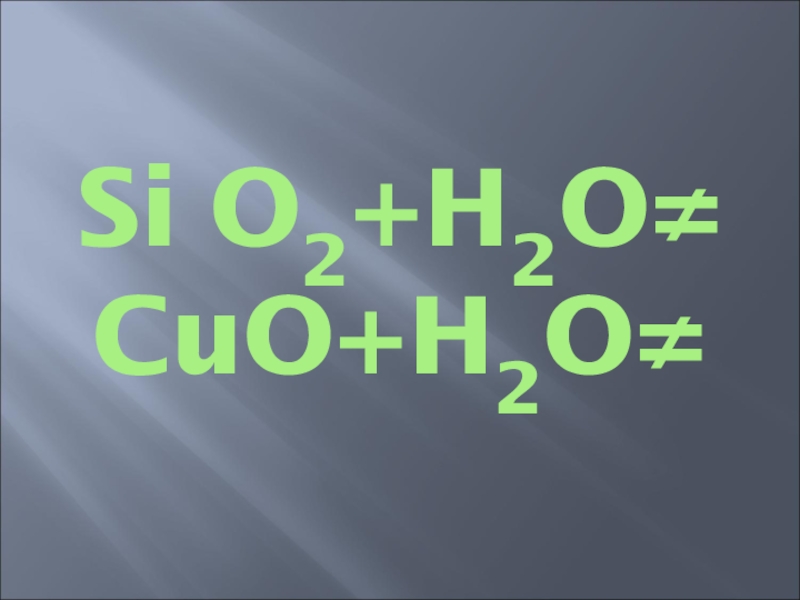изучить их классификацию, свойства основных и кислотных оксидов.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад на тему Оксиды
Содержание
- 1. Оксиды
- 2. Оксиды – это сложные соединения, состоящие из двух химических элементов, один из которых – кислород.
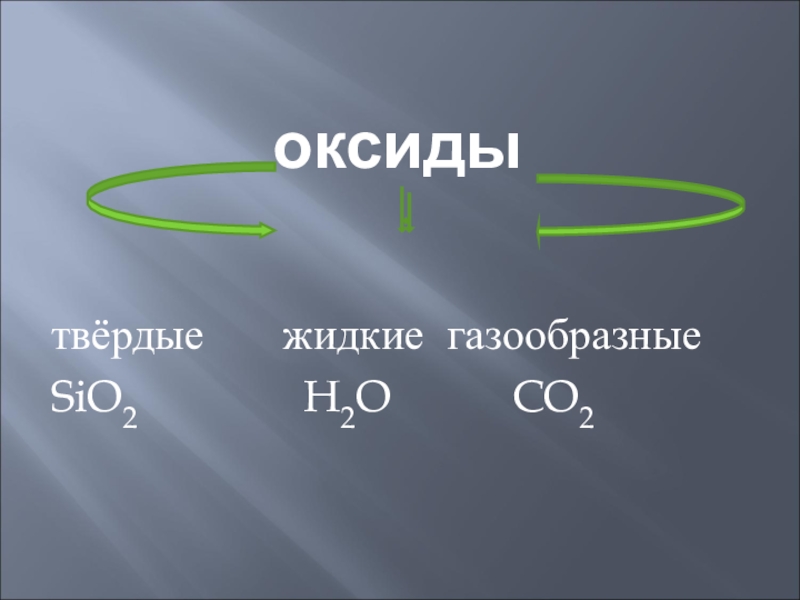
- 3. оксидытвёрдые жидкие газообразныеSiO2
- 4. H2O
- 5. CO2
- 6. SiO2
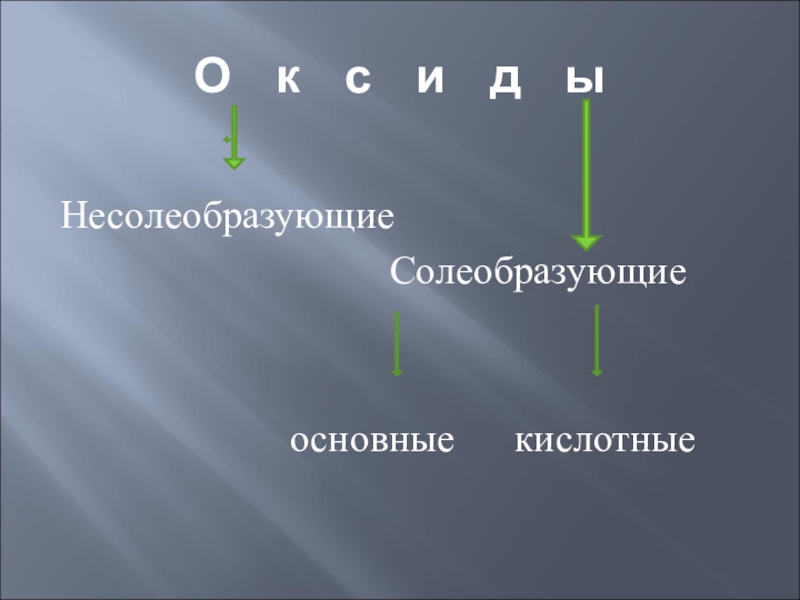
- 7. О к с и
- 8. Несолеобразующими называются такие оксиды, которые не взаимодействуют
- 9. Солеобразующими называются оксиды, которые взаимодействуют с кислотами или щелочами и образуют соль и воду.
- 10. Основные оксиды- это такие оксиды, которым соответствуют
- 11. Кислотные оксиды – это такие оксиды, которым
- 12. Типичные реакции основных оксидов. Основный оксид +
- 13. Типичные реакции кислотных оксидов.Кислотный оксид + щёлочь→соль
- 14. Общее свойство оксидов.Основный оксид + кислотный оксид→
- 15. Si O2+H2O≠ CuO+H2O≠
- 16. Выводы.*повторили определение «оксидов»,*рассмотрели классификацию оксидов по агрегатному
- 17. Домашнее задание:*обязательное: параграф №40, упр.3*дополнительное:
- 18. Дополнительное задание.Как осуществить следующие превращения:алюминий→оксид алюминия→гидроксид алюминия→хлорид алюминия→алюминий.Напишите уравнения реакций.
Оксиды – это сложные соединения, состоящие из двух химических элементов, один из которых – кислород.
Слайд 1ТЕМА: «ОКСИДЫ, КЛАССИФИКАЦИЯ И ХИМИЧЕСКИЕ СВОЙСТВА».
ЦЕЛИ:
обобщить знания учащихся о составе оксидов,
Слайд 2Оксиды – это сложные соединения, состоящие из двух химических элементов, один
из которых – кислород.
Слайд 8Несолеобразующими называются такие оксиды, которые не взаимодействуют ни с кислотами, ни
со щелочами и не образуют солей.
Слайд 9Солеобразующими называются оксиды, которые взаимодействуют с кислотами или щелочами и образуют
соль и воду.
Слайд 10Основные оксиды- это такие оксиды, которым соответствуют основания (Ме со ст.
ок. +1,+2).
K2O – KOH
BaO- Ba(OH)2
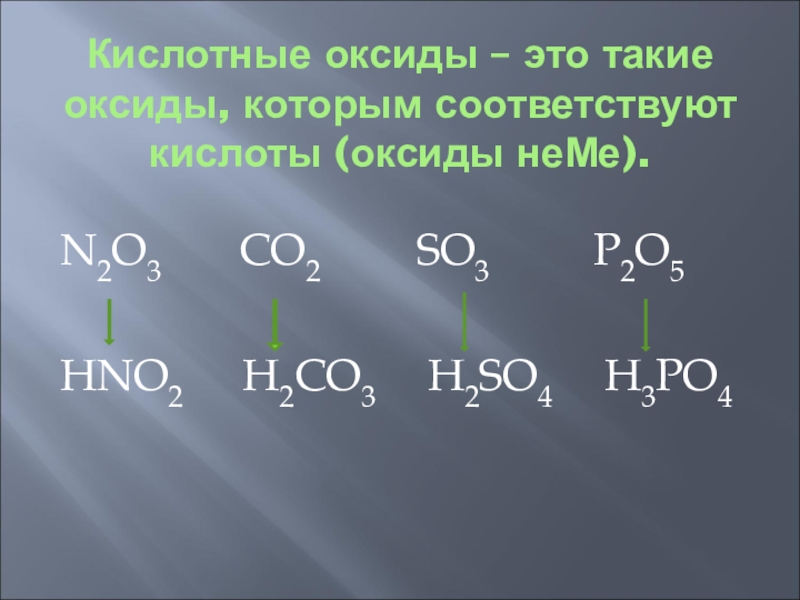
Слайд 11Кислотные оксиды – это такие оксиды, которым соответствуют кислоты (оксиды неМе).
N2O3
CO2 SO3 P2O5
HNO2 H2CO3 H2SO4 H3PO4
HNO2 H2CO3 H2SO4 H3PO4
Слайд 12Типичные реакции основных оксидов.
Основный оксид + кислота→соль + вода
(реакция обмена)
CuO + H2SO4→CuSO4 + H2O
K2O +2HCl→2KCl + H2O
Основный оксид + вода→щёлочь
(реакция соединения)
K2O + H2O→2KOH
Ca O + H2O→Ca(OH)2
CuO + H2SO4→CuSO4 + H2O
K2O +2HCl→2KCl + H2O
Основный оксид + вода→щёлочь
(реакция соединения)
K2O + H2O→2KOH
Ca O + H2O→Ca(OH)2
Слайд 13Типичные реакции кислотных оксидов.
Кислотный оксид + щёлочь→соль + вода (реакция обмена).
SO3+2KOH→K2SO4+H2O
CO2+Ca(OH)2→CaCO3+H2O
Кислотный оксид + вода→кислота
(реакция соединения)
SO3 +H2O→H2SO4
CO2+Ca(OH)2→CaCO3+H2O
Кислотный оксид + вода→кислота
(реакция соединения)
SO3 +H2O→H2SO4
Слайд 14Общее свойство оксидов.
Основный оксид + кислотный оксид→
соль
(реакция соединения)
K2O + CO2 → K2CO3
SO2 + CaO → CaCO3
(реакция соединения)
K2O + CO2 → K2CO3
SO2 + CaO → CaCO3
Слайд 16Выводы.
*повторили определение «оксидов»,
*рассмотрели классификацию оксидов по агрегатному состоянию и способности образовывать
соли,
*изучили свойства основных и кислотных оксидов, а также их общие свойства.
*изучили свойства основных и кислотных оксидов, а также их общие свойства.
Слайд 17Домашнее задание:
*обязательное:
параграф №40, упр.3
*дополнительное:
какие из
данных в-в реагируют с оксидом натрия: соляная к-та, азотная к-та, сероводородная к-та, серная к-та. Напишите уравнения .