Кальций. Соединения кальция, их роль в природе и технике.Важнейшие месторождения кальция.
- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад урока Кальций. 9-класс.
Содержание
- 1. Презентация урока Кальций. 9-класс.
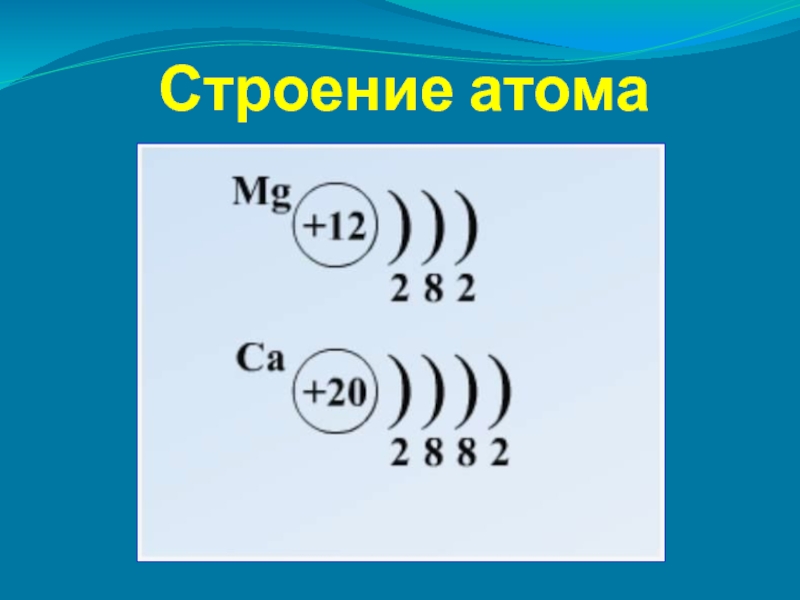
- 2. Строение атома
- 3. Физические свойства кальцияКальций - серебристо-белый металл.На воздухе
- 4. Химические свойства С азотом: 3Ca
- 5. Осуществить превращения:Ca→ CaO → Ca(OH)2 → CaCl2 → CaCO3
- 6. Закончить уравнения реакций, назвать соединения. Сa + H2O? Ca(OH)2+ HCl?3) CaO + H2SO4? CaCO3? CaO+H2O? Ca(OH)2+CO2?
- 7. Слайд 7
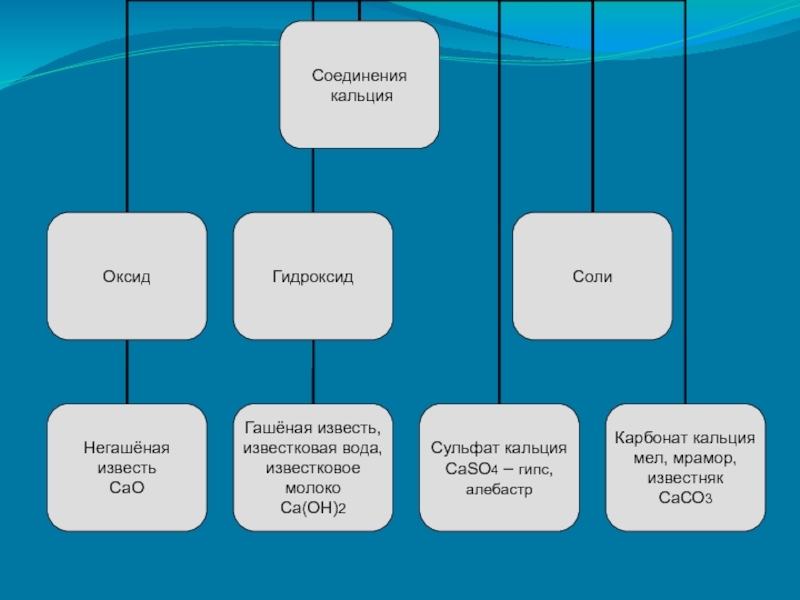
- 8. Оксид кальцияГидроксид кальция
- 9. Гидроксид кальция – известковая вода, известковое молоко
- 10. Гипс
- 11. Мел
- 12. Известняк
- 13. Соединения кальция, их роль в природе и технике.
- 14. Кальций – важнейший строительный материал природы
- 15. МинералыКальцит
- 16. Карстовые пещеры
- 17. Сталактиты
- 18. Сталагмиты
- 19. Самый «живой» металл
- 20. CaЭлемент кальций входит в состав многих овощей
- 21. Слайд 21
- 22. Фосфат и карбонат кальция -
- 23. Как Ca оказывается в клетках живого
- 24. В виде карбоната кальция – накапливается в скелетах коралловых полипов
- 25. Карбонат кальция накапливается
- 26. Недостаток Ca:У РАСТЕНИЙ вызывает нарушения в работе
- 27. Значение кальция в природеФормирует залежи горных пород.
- 28. Где находят применение соединения кальция?
- 29. Слайд 29
- 30. Слайд 30
- 31. Потребность организма
- 32. Слайд 32
- 33. Задание. Заполните таблицу:
- 34. Ответы
- 35. Задание. Из предложенного перечня выберите формулы веществ,
- 36. Ответ: Как основный оксид CaO реагирует с
- 37. Домашнее задание Параграф 32-33 (упр.после 32-33):
Строение атома
Слайд 1 Мощь и сила науки – во множестве фактов, цель – в
обобщении этого множества.
Д. И. Менделеев
Слайд 3Физические свойства кальция
Кальций - серебристо-белый металл.
На воздухе быстро взаимодействует с кислородом
, поэтому его хранят под слоем керосина. Температура плавления-840 гр. по С.
Слайд 4Химические свойства
С азотом: 3Ca + N2 =Ca3N2
С фосфором: 3Ca + 2P =Ca3P2
Ca + H2 = CaH2
2Ca + O2 → 2CaO
Ca+2 H2O → Ca(OH)2 +H2
Ca + H2 = CaH2
2Ca + O2 → 2CaO
Ca+2 H2O → Ca(OH)2 +H2
Слайд 6Закончить уравнения реакций, назвать соединения.
Сa + H2O?
Ca(OH)2+ HCl?
3)
CaO + H2SO4?
CaCO3?
CaO+H2O?
Ca(OH)2+CO2?
CaCO3?
CaO+H2O?
Ca(OH)2+CO2?
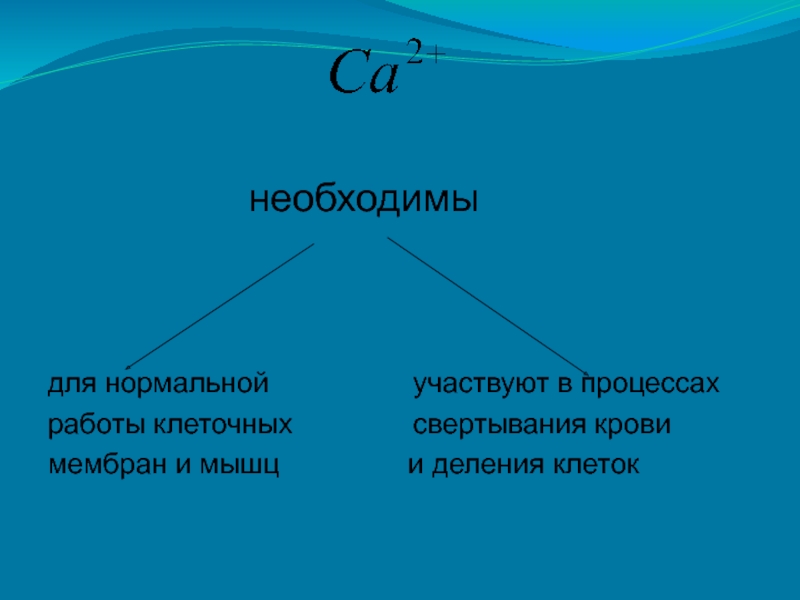
Слайд 21
необходимы
для нормальной участвуют в процессах
работы клеточных свертывания крови
мембран и мышц и деления клеток
для нормальной участвуют в процессах
работы клеточных свертывания крови
мембран и мышц и деления клеток
Слайд 22 Фосфат и карбонат кальция - основные минеральные вещества костей
скелета.
80 % Са3(РО4)2
13% СаСО3
80 % Са3(РО4)2
13% СаСО3
Слайд 23Как Ca оказывается
в клетках живого организма:
РАСТЕНИЯ поглощают ионы Ca из
почвенного раствора
НАЗЕМНЫЕ ЖИВОТНЫЕ получают ионы кальция с пищей и водой
ВОДНЫЕ РАСТЕНИЯ И ЖИВОТНЫЕ извлекают ионы кальция из морской и речной воды
Слайд 26Недостаток Ca:
У РАСТЕНИЙ вызывает нарушения в работе корневой системы
У ЖИВОТНЫХ вызывает
рахит, ослабление сердечной деятельности; кровь, обеднённая кальцием, плохо свертывается.
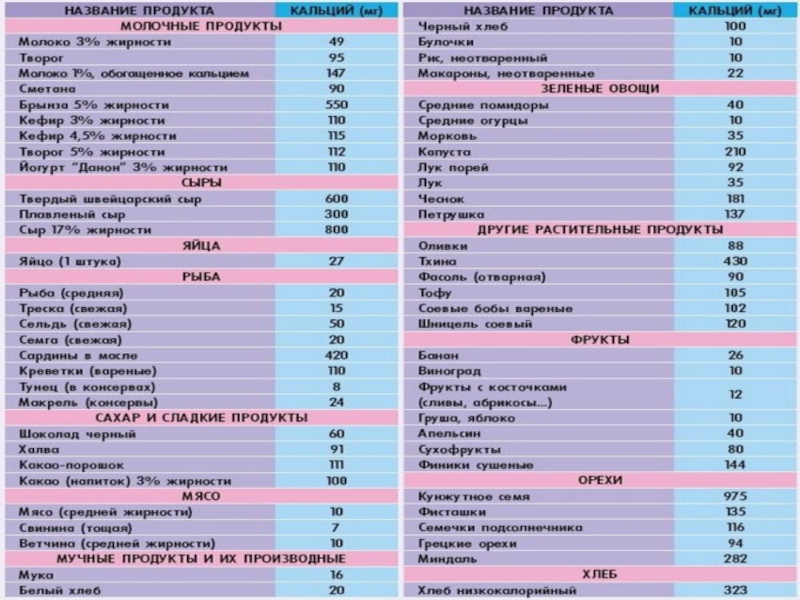
Слайд 31 Потребность организма в кальции:
от 1 года до 6 лет - 1500 мг в сутки
7 - 9 лет - 700мг
10 - 12 лет (мальчики) – 900 мг
(девочки) – 1200 мг
13 - 20 лет – 1200 мг
21 - 50 лет – 1000 мг
старше 50 лет - 1200 – 1500 мг
Слайд 35
Задание. Из предложенного перечня выберите формулы веществ, с которыми может реагировать
оксид кальция. Запишите уравнения возможных реакций (самопроверка).
Na, SO2, MgO, HCl, CaCl2, KOH
Na, SO2, MgO, HCl, CaCl2, KOH
Слайд 36Ответ: Как основный оксид CaO реагирует с кислотными оксидами и кислотами,
образуя соли:
1. СаO + SO2 = CaSO3
2. CaO + 2HCl = CaCl2 +H2O
1. СаO + SO2 = CaSO3
2. CaO + 2HCl = CaCl2 +H2O