- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Растворимость. Растворение. Растворы.
Содержание
- 1. Презентация Растворимость. Растворение. Растворы.
- 2. Познакомить учащихся с растворением как физико-химическим процессом
- 3. Слайд 3
- 4. Современная теорияРастворение – это физико-химический процесс ,
- 5. Признаки химического взаимодействия при растворении :1.
- 6. Слайд 6
- 7. Факторы, от которых зависит растворение твёрдых
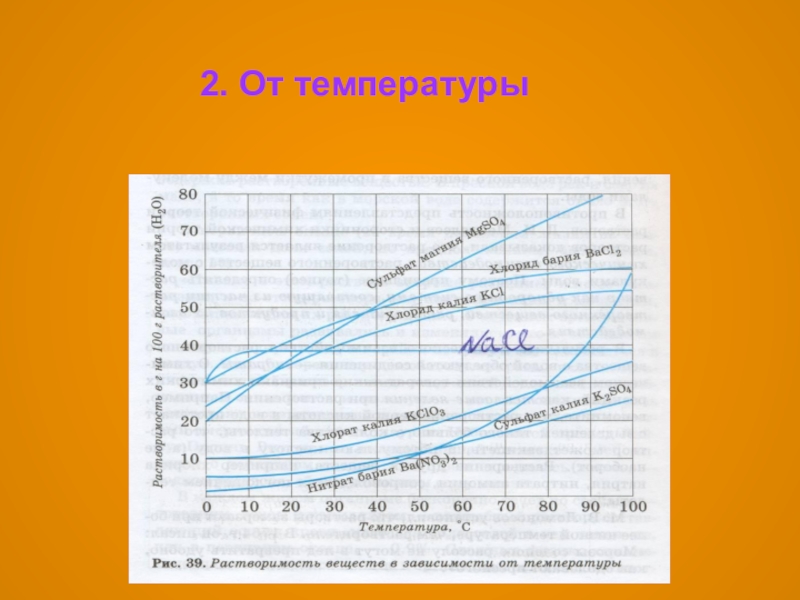
- 8. 2. От температуры
- 9. Слайд 9
- 10. Типы растворов по содержанию растворённого
- 11. Слайд 11
Слайд 1Растворение. Растворимость веществ в воде.
Химия -8 кл.
Подготовила учитель
химии МБОУ СОШ с.Панино
Щенова
Слайд 2Познакомить учащихся с растворением как физико-химическим процессом и с растворами как
Показать зависимость растворимости твёрдых веществ от температуры.
Дать классификацию растворов по признаку растворимости.
Цели урока :
Слайд 3 Растворение. Растворы.
↓ ↓
Физическая теория Химическая теория
(Вант-Гофф, Оствальд, Аррениус). (Менделеев, Каблуков, Кистяковский)
Растворение-это процесс диффузии, Растворение-это процесс химичес-
растворы- это однородные смеси. кого взаимодействия растворяемого
вещества с водой- процесс гидратации,
а растворы- это соединения –гидраты.
--------------------------------------------------
Слайд 4Современная теория
Растворение – это физико-химический процесс ,
а
состоящая из частиц растворённого вещества,
растворителя и продуктов их взаимодействия – гидратов
. ↓
___________________________________________________________________
↓ ↓
непостоянный состав постоянный состав
в растворах в кристаллогидратах
1) медный купорос- Сu SO 4 ∙ 5 H 2 O 2) глауберова соль-Na 2 SO4 ∙ 10 H2O
Слайд 5 Признаки химического взаимодействия при растворении :
1. Тепловые явления
(регистрируются с помощью
↓ ↓
Экзотермические Эндотермические
(растворение H2SO4, NaOH) ( растворение NaCl ) ↓ ↓
Демонстрация разбавления Демонстрация растворения
серной кислоты нитрата аммония
Слайд 6
2.Изменение цвета.
________________________________________________________________
↓ дальнейшее выпаривание ↓
Белые кристаллы → Синие кристаллы
Cu SO4 (безводного) ← Cu SO4 ∙ 5 H2O,
раствор голубого
цвет
приливание воды
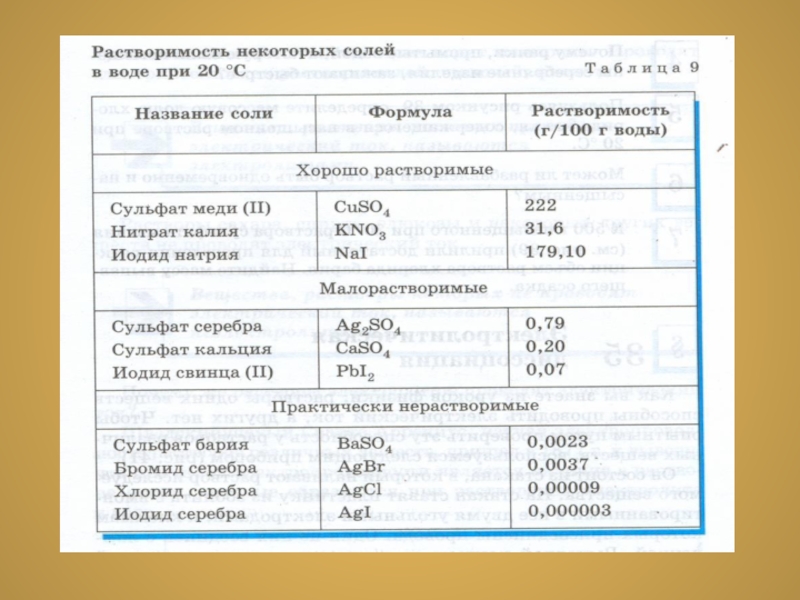
Слайд 7Факторы, от которых зависит
растворение твёрдых веществ
1.От природы веществ (на 1
____________________________________________________
↓ ↓ ↓
Хорошо растворимые Малорастворимые Практически нерастворимые
(более 1 г) (менее 1 г ) (менее 0,01 г )
Р М Н
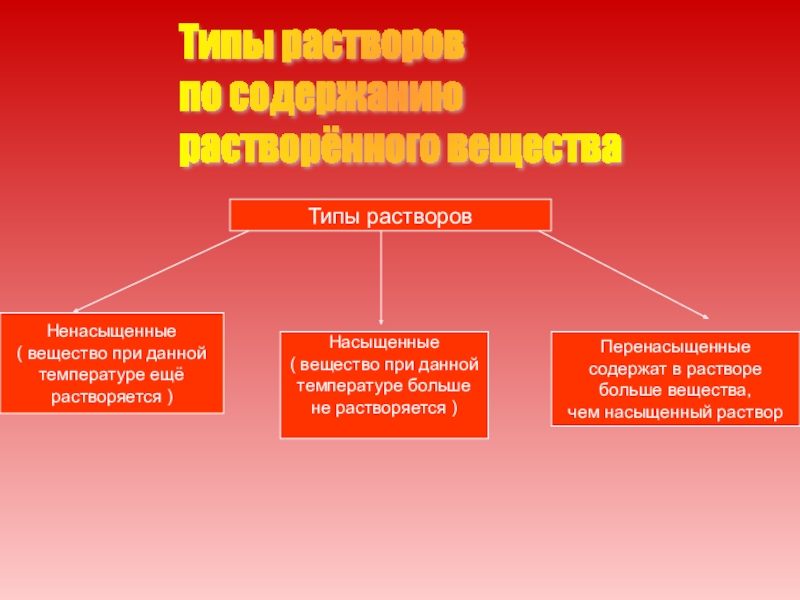
Слайд 10Типы растворов
по содержанию
растворённого вещества
Типы растворов
Ненасыщенные
( вещество при данной
температуре
растворяется )
Насыщенные
( вещество при данной
температуре больше
не растворяется )
Перенасыщенные
содержат в растворе
больше вещества,
чем насыщенный раствор