- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Предмет органической химии
Содержание
- 1. Презентация Предмет органической химии
- 2. Первые попытки классификации веществ на органические и
- 3. Лавуазье в конце 18 века первым высказал
- 4. В начале 19 века назрела необходимость выделить
- 5. Слайд 5
- 6. Слайд 6
- 7. Слайд 7
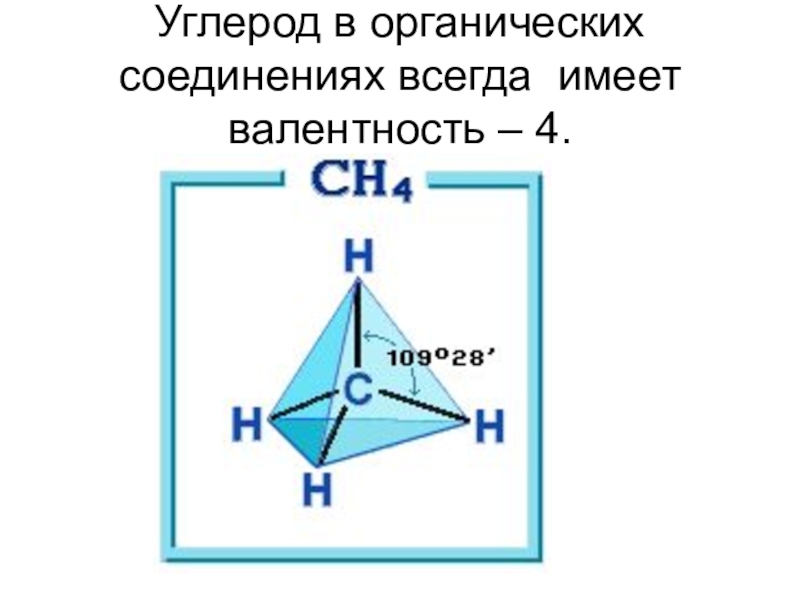
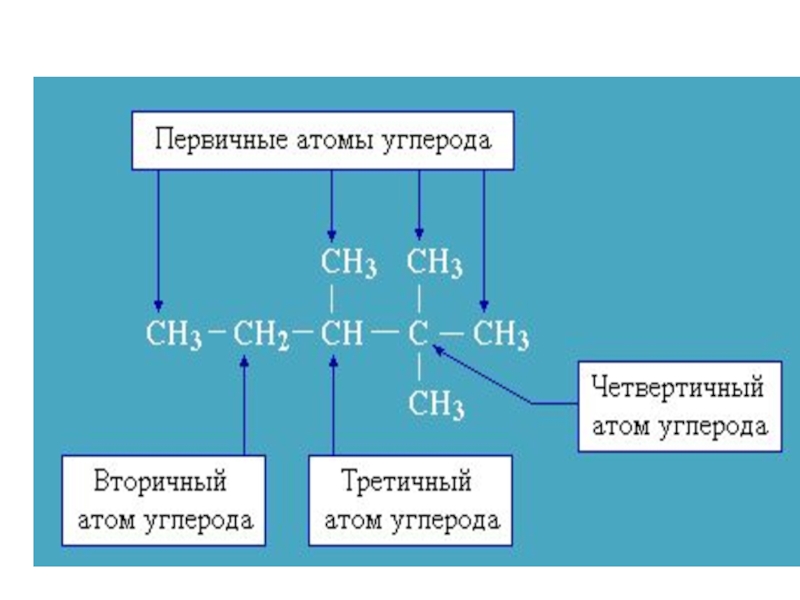
- 8. Углерод в органических соединениях всегда имеет валентность – 4.
- 9. Слайд 9
- 10. Слайд 10
- 11. Слайд 11
- 12. природные и синтетические органические вещества
- 13. Слайд 13
- 14. Слайд 14
- 15. Слайд 15
- 16. Слайд 16
- 17. Слайд 17
- 18. Слайд 18
- 19. Слайд 19
- 20. Слайд 20
- 21. Слайд 21
- 22. Слайд 22
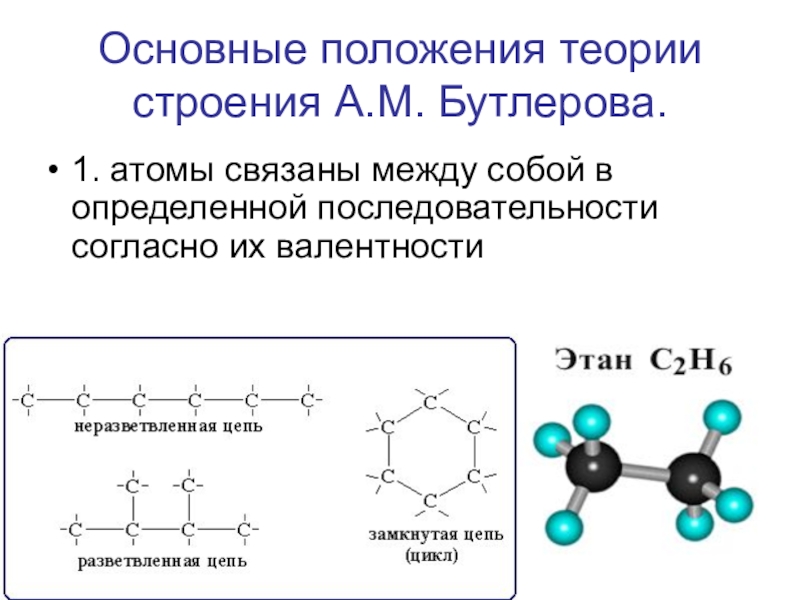
- 23. Основные положения теории строения А.М. Бутлерова.1. атомы связаны между собой в определенной последовательности согласно их валентности
- 24. Химические свойства веществ определяются их строением.Изомеры –
- 25. Слайд 25
- 26. Слайд 26
- 27. Слайд 27
- 28. Общая формулаГомологический рядГомологиНоменклатураСтроение – свойства - применениепредельные углеводороды алканы
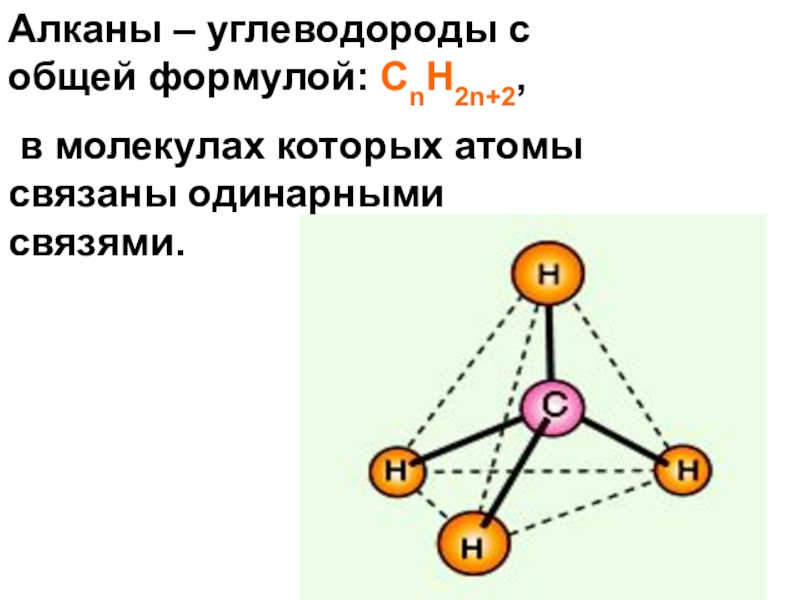
- 29. Алканы – углеводороды с общей формулой: СnH2n+2, в молекулах которых атомы связаны одинарными связями.
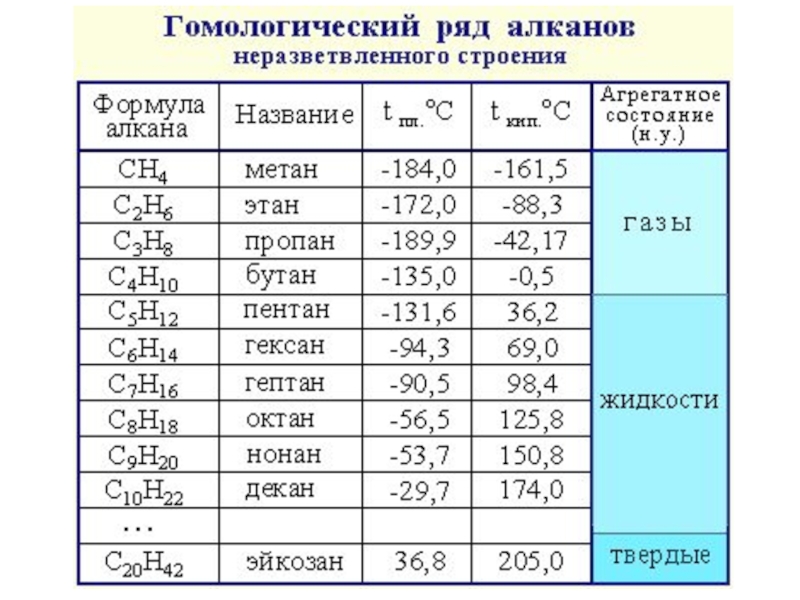
- 30. Гомологический ряд МетанЭтанПропан БутанРяд соединений, обладающих подобным
- 31. Слайд 31
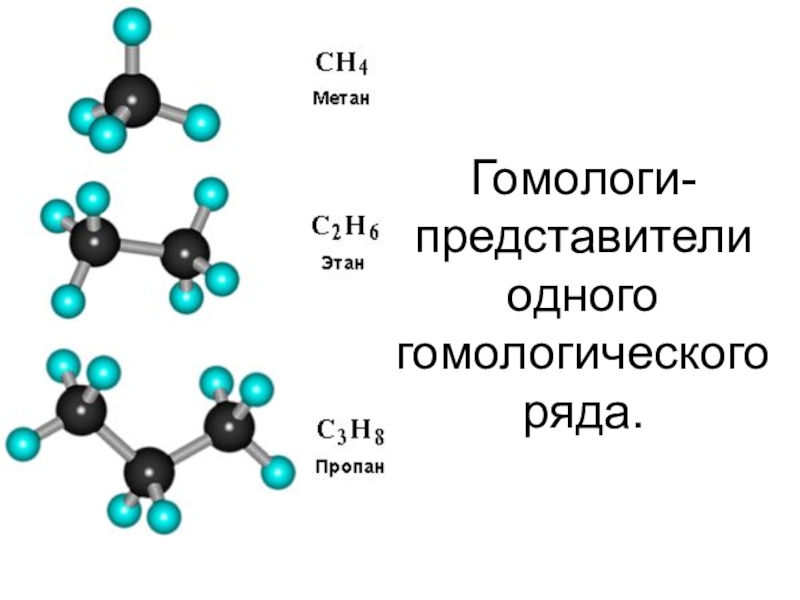
- 32. Гомологи- представители одного гомологического ряда.
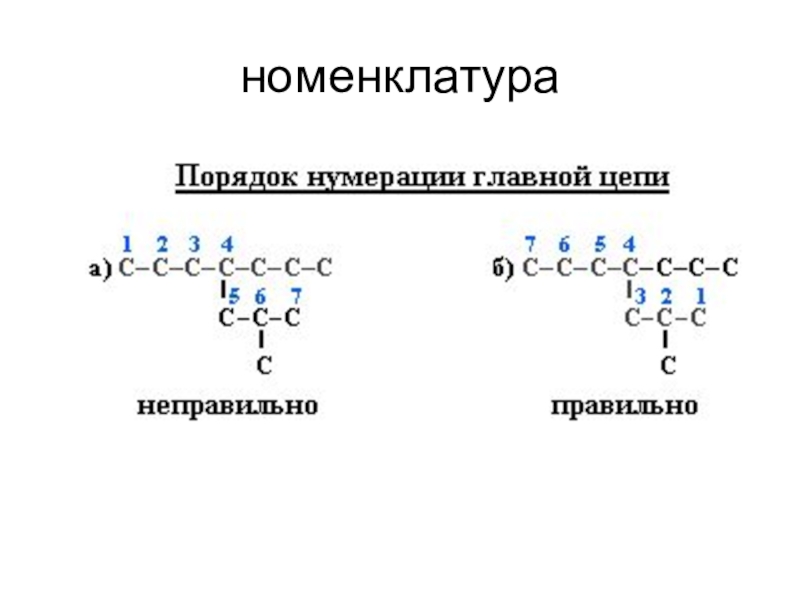
- 33. номенклатура
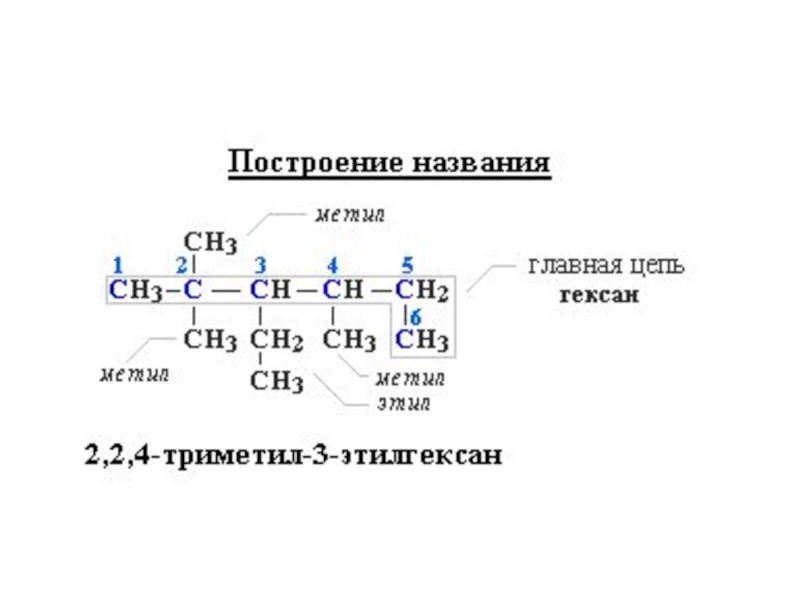
- 34. Слайд 34
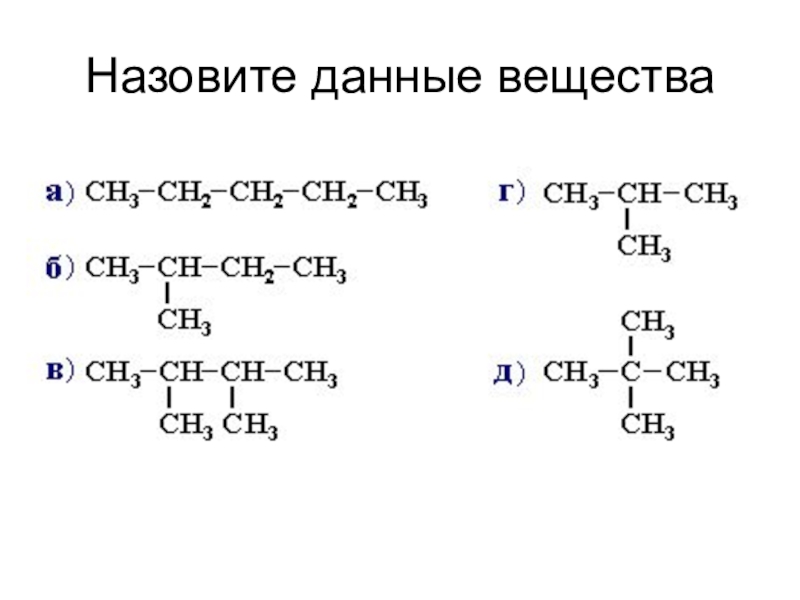
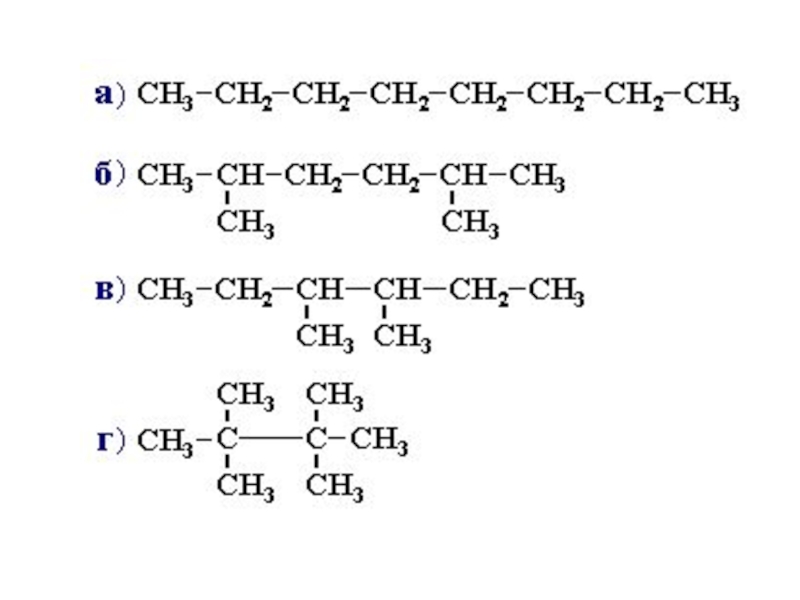
- 35. Назовите данные вещества
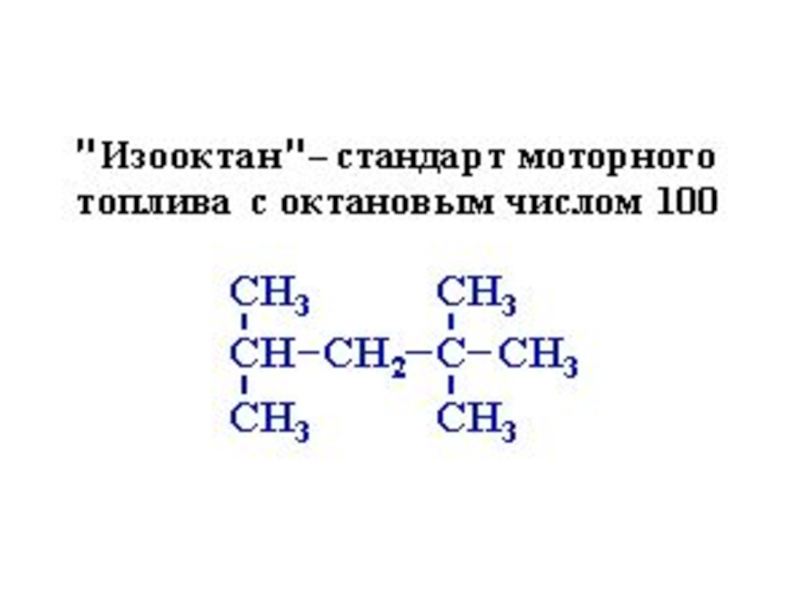
- 36. Слайд 36
- 37. Слайд 37
- 38. Слайд 38
- 39. Физические свойства Все алканы плохо растворимы в
- 40. Химические свойства 1- реакции замещения2- реакции дегидрирования3- реакции горения4 - реакции изомеризации5- термическое расщепление
- 41. Пример реакции замещения:Взаимодействие декана с бромомС10Н22 +
- 42. При дегидрировании алканов образуются алкены и другие
- 43. Все алканы горят с образованием углекислого газа
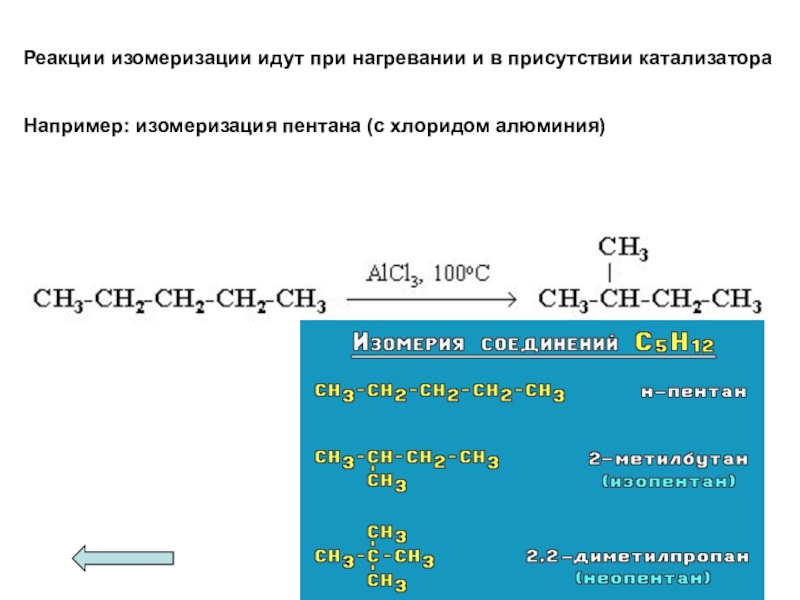
- 44. Реакции изомеризации идут при нагревании и в присутствии катализатораНапример: изомеризация пентана (с хлоридом алюминия)
- 45. Термическое расщепление1- крекинг (400-500 оС)Алкан
- 46. Слайд 46
Слайд 2
Первые попытки классификации веществ на органические и неорганические были предприняты еще
из истории
Слайд 3
Лавуазье в конце 18 века первым высказал причину резкого отличия в
Слайд 4
В начале 19 века назрела необходимость выделить химию веществ растительного и
Органическая химия - это химия соединений углерода
Слайд 23Основные положения теории строения А.М. Бутлерова.
1. атомы связаны между собой в
Слайд 24
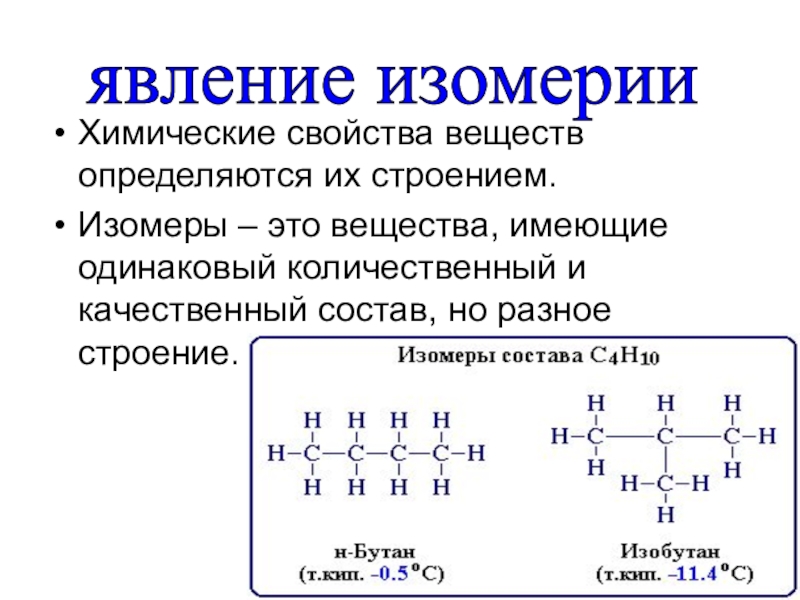
Химические свойства веществ определяются их строением.
Изомеры – это вещества, имеющие одинаковый
явление изомерии
Слайд 28
Общая формула
Гомологический ряд
Гомологи
Номенклатура
Строение – свойства - применение
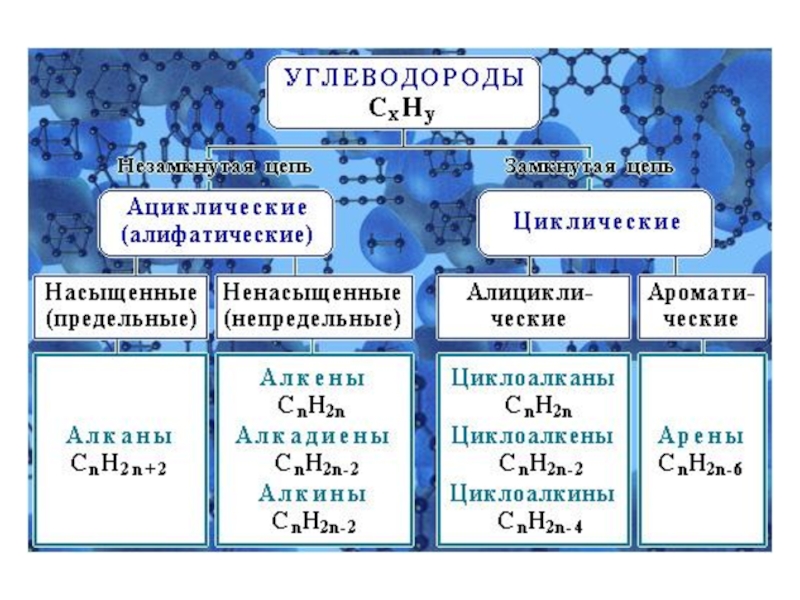
предельные углеводороды
алканы
Слайд 29Алканы – углеводороды с общей формулой: СnH2n+2,
в молекулах которых атомы
Слайд 30Гомологический ряд
Метан
Этан
Пропан
Бутан
Ряд соединений, обладающих подобным строением и свойствами и
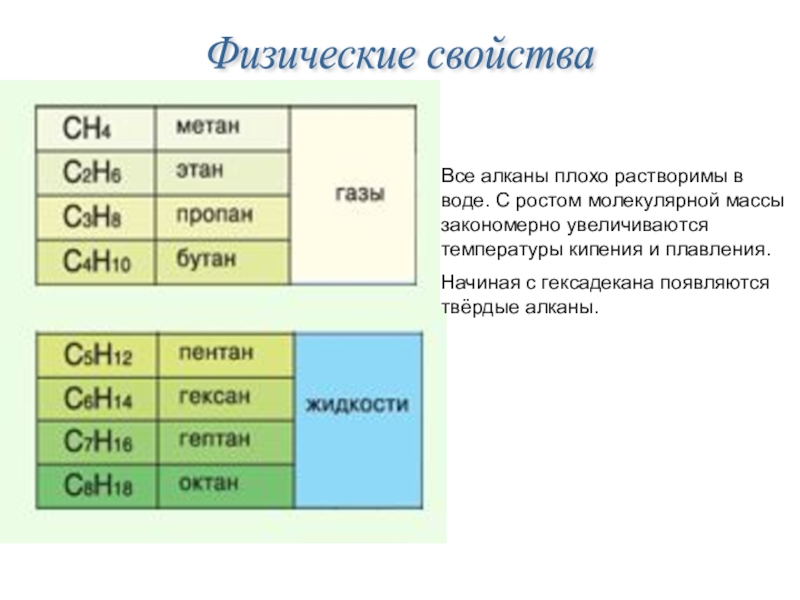
Слайд 39Физические свойства
Все алканы плохо растворимы в воде. С ростом молекулярной
Начиная с гексадекана появляются твёрдые алканы.
Слайд 40Химические свойства
1- реакции замещения
2- реакции дегидрирования
3- реакции горения
4 - реакции
5- термическое расщепление
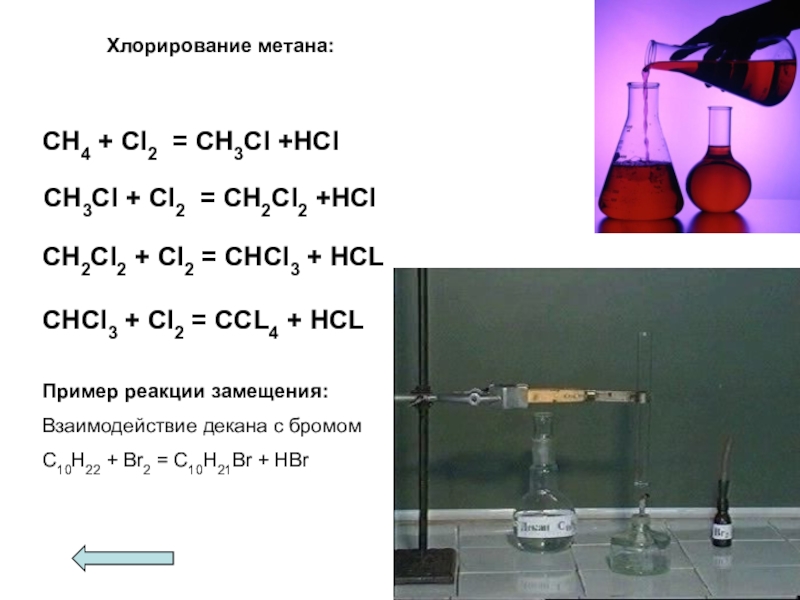
Слайд 41Пример реакции замещения:
Взаимодействие декана с бромом
С10Н22 + Br2 = С10Н21Br +
CH4 + Cl2 = CH3Cl +HCl
CH3Cl + Cl2 = CH2Cl2 +HCl
CH2Cl2 + Cl2 = CHCl3 + HCL
CHCl3 + Cl2 = CCL4 + HCL
Хлорирование метана:
Слайд 42При дегидрировании алканов образуются алкены и другие непредельные углеводороды.
Например, дегидрирование пентана:
С5Н10
пентен
Слайд 43Все алканы горят с образованием углекислого газа и воды
2С4Н10 + 13О2
Например: горение бутана
Слайд 44Реакции изомеризации идут при нагревании и в присутствии катализатора
Например: изомеризация пентана
Слайд 45Термическое расщепление
1- крекинг (400-500 оС)
Алкан новый алкан и алкен
С20Н42
2- пиролиз метана при 1000о С
СН4 С + 2Н2
3- получение ацетилена при нагревании до 1500оС
2СН4 С2Н2 + 3Н2