- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад Понятие о кислотах
Содержание
- 1. Презентация Понятие о кислотах
- 2. ПОНЯТИЕ О КИСЛОТАХ
- 3. Цель: Сформировать знания о кислотах,
- 4. Страна кислот Город Информаций
- 5. Серная кислота
- 6. Хлороводородная (соляная) кислота
- 7. Азотная кислота
- 8. H3BO3Борная кислота
- 9. Кремниевая кислотаH2SiO3
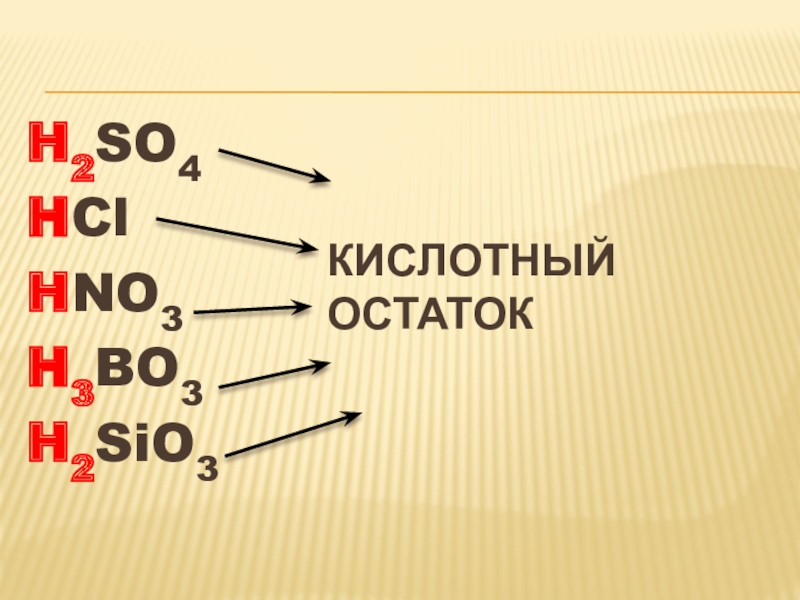
- 10. H2SO4 HCl HNO3 H3BO3 H2SiO3 Кислотный остаток
- 11. Кислоты - сложные вещества, молекулы которых состоят из атомов водорода и кислотных остатков.
- 12. H2SO4 HCl HNO3 H3BO3 H2SiO3 Валентность кислотного остатка равна числу атомов водорода в составе кислоты
- 13. Страна кислот Город Классификаций
- 14. По какому признаку кислоты разделены на
- 15. По какому признаку кислоты разделены на группы?
- 16. H2SO4 HCl HNO3 H3BO3 H2SiO3
- 17. классифицируйте кислотыHNO2H2CO3H2SH2SO3HAlO2H3PO4HIа) бескислородные, кислородсодержащиеб) одноосновные, двухосновные, трехосновные
- 18. Проверяем:1. Бескислородные: H2S, HI 2. Кислородсодержащие:
- 19. Страна кислотГород Номенклатурный
- 20. Названия кислот: HCl – хлороводороднаяHBr - бромоводороднаяHNO3 – азотнаяHNO2 - азотистаяH2SO4 – сернаяH2SO3 - сернистая
- 21. Характеристика кислотH2SHFH3PO4HNO3
- 22. Проверяем:HF - фтороводородная, бескислородная, одноосновная.H3PO4 - фосфорная, кислородсодержащая, трехосновная.HNO3 - азотная, кислородсодержащая, одноосновная.
- 23. Страна кислотГород Экспериментов
- 24. Правила техники безопасности Внимание! Работать
- 25. Индикаторы – органические вещества, которые
- 26. Лабораторный опыт Действие кислот на
- 27. ИГРА «Найди кислоты» Среди формул
- 28. Игра «Третий лишний»В каждом ряду найдите лишнюю
- 29. Подведем итог урока:- Кто сможет выбрать формулу
- 30. СПАСИБО ЗА УРОК!
ПОНЯТИЕ О КИСЛОТАХ
Слайд 3 Цель:
Сформировать знания о кислотах, их составе, способах классификации
и названия представителей класса кислот; умение экспериментально определять кислоты среди других веществ.
Слайд 11
Кислоты - сложные вещества, молекулы которых состоят из атомов водорода
и кислотных остатков.
Слайд 12H2SO4
HCl
HNO3
H3BO3
H2SiO3
Валентность кислотного остатка равна числу атомов
водорода в составе кислоты
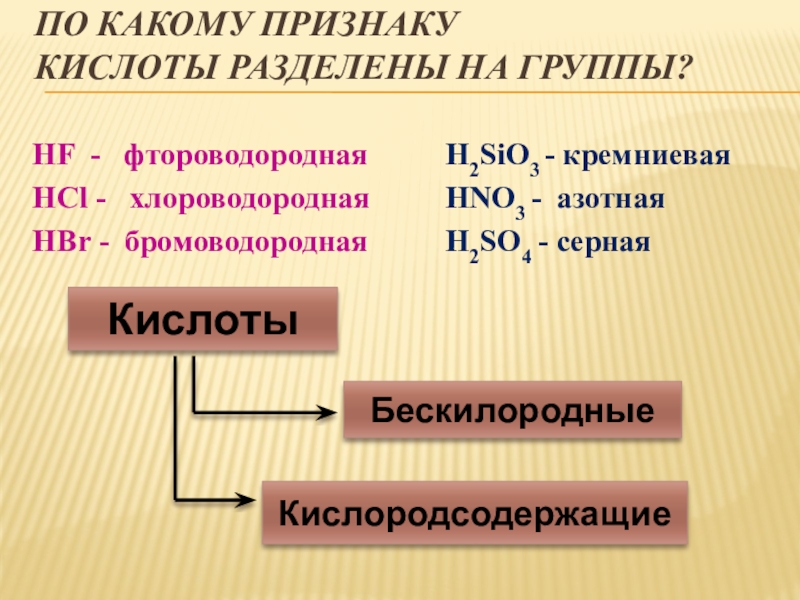
Слайд 14По какому признаку
кислоты разделены на группы?
HF - фтороводородная
HCl -
хлороводородная
HBr - бромоводородная
HBr - бромоводородная
H2SiO3 - кремниевая
HNO3 - азотная
H2SO4 - серная
Кислоты
Бескилородные
Кислородсодержащие
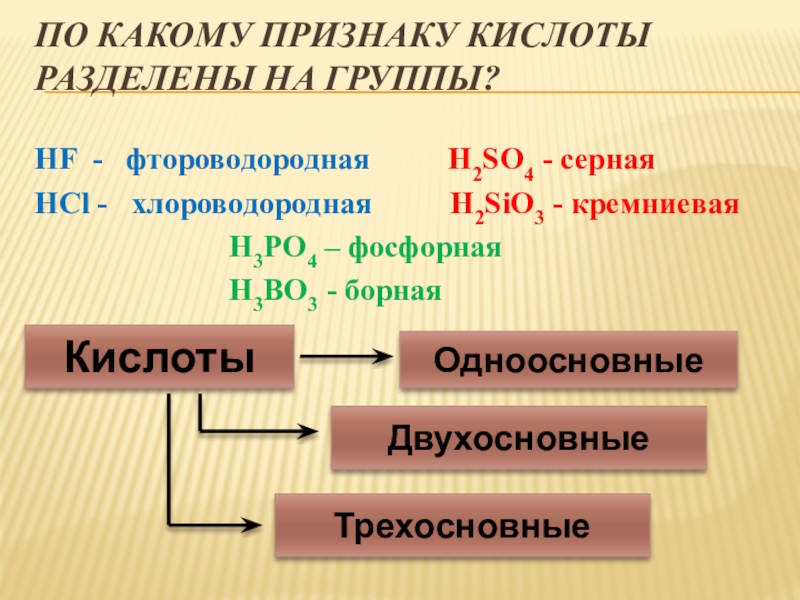
Слайд 15По какому признаку кислоты разделены на группы?
HF - фтороводородная
H2SO4 - серная
HCl - хлороводородная H2SiO3 - кремниевая
H3PO4 – фосфорная
H3BO3 - борная
HCl - хлороводородная H2SiO3 - кремниевая
H3PO4 – фосфорная
H3BO3 - борная
Кислоты
Одноосновные
Двухосновные
Трехосновные
Слайд 17 классифицируйте кислоты
HNO2
H2CO3
H2S
H2SO3
HAlO2
H3PO4
HI
а) бескислородные, кислородсодержащие
б) одноосновные, двухосновные, трехосновные
Слайд 18 Проверяем:
1. Бескислородные: H2S, HI
2. Кислородсодержащие: HNO2, H2CO3, H2SO3, HAlO2,
H3PO4
1. Одноосновные: HNO2, HAlO2, HI
2. Двухосновные: H2CO3, H2S, H2SO3
3. Трехосновные: H3PO4
1. Одноосновные: HNO2, HAlO2, HI
2. Двухосновные: H2CO3, H2S, H2SO3
3. Трехосновные: H3PO4
Слайд 20Названия кислот:
HCl – хлороводородная
HBr - бромоводородная
HNO3 – азотная
HNO2 - азотистая
H2SO4 –
серная
H2SO3 - сернистая
H2SO3 - сернистая
Слайд 22Проверяем:
HF - фтороводородная, бескислородная, одноосновная.
H3PO4 - фосфорная, кислородсодержащая, трехосновная.
HNO3 - азотная,
кислородсодержащая, одноосновная.
Слайд 24Правила техники безопасности
Внимание! Работать с кислотами необходимо
аккуратно, так как можно получить ожог или отравление. При попадании кислоты на кожу надо смыть ее струей воды , а затем обработать поврежденную поверхность 2%-м раствором питьевой соды.
Слайд 25
Индикаторы – органические вещества, которые изменяют свою окраску
в присутствии кислот и некоторых других веществ.
Слайд 26 Лабораторный опыт
Действие кислот на индикаторы
Задание 1:
проведите опыт,
согласно инструкции;
сделайте вывод о распознавании кислот среди других растворов.
Задание 2:
Определите, в какой из двух предложенных пробирок находится раствор кислоты.
сделайте вывод о распознавании кислот среди других растворов.
Задание 2:
Определите, в какой из двух предложенных пробирок находится раствор кислоты.
Слайд 27 ИГРА «Найди кислоты»
Среди формул различных соединений «спрятаны» формулы
кислот. Необходимо отыскать эти формулы.
H2O, SO, HBr, Na2CO3, Mg, Ba, H2CO3, Ca, NaOH, H3PO4, P2O5, PH3, NaCl, CO2, HCl, K2O, H2SiO3, Ag, H2SO4
H2O, SO, HBr, Na2CO3, Mg, Ba, H2CO3, Ca, NaOH, H3PO4, P2O5, PH3, NaCl, CO2, HCl, K2O, H2SiO3, Ag, H2SO4
Слайд 28Игра «Третий лишний»
В каждом ряду найдите лишнюю формулу, ответ мотивируйте:
H2SO4,
SO3, H3PO4.
HCl, H2SO4, H3PO4
H2SO3, H2SiO3, H2SO4
HNO3, H2SO4, H2CO3
HCl, H2SO4, H3PO4
H2SO3, H2SiO3, H2SO4
HNO3, H2SO4, H2CO3
Слайд 29Подведем итог урока:
- Кто сможет выбрать формулу кислоты среди других веществ?
-
Кто сможет назвать и классифицировать кислоты?
- Кто сможет экспериментально определить кислоту?
- Я хотел бы узнать о кислотах …
- Кто сможет экспериментально определить кислоту?
- Я хотел бы узнать о кислотах …