- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме водород
Содержание
- 1. Презентация по теме водород
- 2. 1вариант
- 3. Слайд 3
- 4. Начало всех начал – водород!
- 5. положение в периодической таблице Применение
- 6. Химический элементПорядковый номер Группа – Период – Электронная формула Степени окисления: Относительная атомная масса
- 7. Слайд 7
- 8. Двойственное положение водорода в периодической таблице объясняется
- 9. ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДАГаз без цвета, запаха
- 10. Опыт Пилатра де РозьераКак-то он решил проверить,
- 11. Химические свойства
- 12. Водород в реакции с неметаллами и оксидами
- 13. В промышленности:конверсией водяных паров C +
- 14. Получение водородаВзаимодействие кальция с водой:Гидролиз гидридов:Действие разбавленных кислот на металлы:
- 15. Составьте уравнения реакций взаимодействия водорода со следующими
1вариант 2 вариант 1
Слайд 1Химический диктант
Выбрать свойства, характерные для:
I вариант – металлов
II вариант – неметаллов
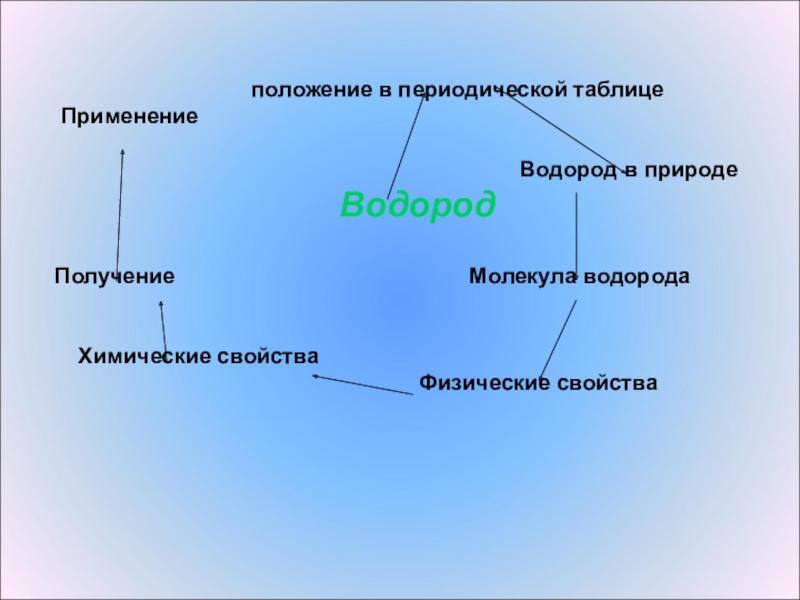
Слайд 5 положение в периодической таблице
Применение
Водород в природе
Водород
Получение Молекула водорода
Химические свойства
Физические свойства
Водород
Получение Молекула водорода
Химические свойства
Физические свойства
Слайд 6Химический элемент
Порядковый номер
Группа –
Период –
Электронная формула
Степени окисления:
Относительная атомная масса
Слайд 8Двойственное положение водорода в периодической таблице объясняется его сходством в строении
и свойствах со щелочными металлами и элементами VII группы
Слайд 9 ФИЗИЧЕСКИЕ СВОЙСТВА ВОДОРОДА
Газ без цвета, запаха и вкуса
Мало растворим в
воде
Легче воздуха
Теплопроводен
Сжижается (температура кипения –252,7)
Температура плавления -259,15
В смеси с воздухом взрывоопасен
Легче воздуха
Теплопроводен
Сжижается (температура кипения –252,7)
Температура плавления -259,15
В смеси с воздухом взрывоопасен
Слайд 10Опыт Пилатра де Розьера
Как-то он решил проверить, что будет,
если вдохнуть
водород; до него никто
такого эксперимента не проводил.
Не заметив никакого эффекта,
ученый решил убедиться,
проник ли водород в легкие.
Он еще раз глубоко вдохнул
этот газ, а затем выдохнул его
на огонь свечи, ожидая увидеть
вспышку пламени. Однако водород
в легких экспериментатора
смешался с воздухом, и
произошел сильный взрыв.
такого эксперимента не проводил.
Не заметив никакого эффекта,
ученый решил убедиться,
проник ли водород в легкие.
Он еще раз глубоко вдохнул
этот газ, а затем выдохнул его
на огонь свечи, ожидая увидеть
вспышку пламени. Однако водород
в легких экспериментатора
смешался с воздухом, и
произошел сильный взрыв.
Слайд 12Водород в реакции с неметаллами и оксидами металлов является……… , а
с металлами он ……. .Т.е. проявляет …….. -…….. свойства
Слайд 13 В промышленности
:
конверсией водяных паров
C + H2O = CO +
H2
CH4 +H2O = CO + 3H2
разложением метана
CH4 = C + 2H2
электролизом воды
2H2O = 2H2 + O2
CH4 +H2O = CO + 3H2
разложением метана
CH4 = C + 2H2
электролизом воды
2H2O = 2H2 + O2
Слайд 14Получение водорода
Взаимодействие кальция с водой:
Гидролиз гидридов:
Действие разбавленных кислот на металлы:
Слайд 15Составьте уравнения реакций взаимодействия водорода со следующими веществами:
F2
Ca
Al2O3
оксидом
ртути (II)
оксидом вольфрама (VI)
оксидом вольфрама (VI)