- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме: Реакции ионного обмена.
Содержание
- 1. Презентация по теме: Реакции ионного обмена.
- 2. Электролитическая диссоциация; электролиты; неэлектролиты; ионы; степень
- 3. 1) глюкозы2) сахара3) спирта4) соли1. Проводит электрический ток раствор
- 4. 1) Соли2) Кислоты3) Сахара4) щелочи2. Не проводит электрический ток раствор
- 5. 1) Кристаллизация 2) Соединение3) Притяжение4) ассоциация3. процесс, обратный процессу диссоциации
- 6. 1) H2CO32) H2O3) NaOH4) H2S5) HNO36) HNO27) H2SO48) KCL9) Ca(OH)2Укажите сильные электролиты
- 7. 1) HNO22) C6H12O63) NH4CL4) Ba(OH)25) HF6) NaOH7) BaSO4Укажите слабые элетролиты
- 8. Название вещества характеристика
- 9. 1. Катион2. Анион3. Молекулу4. Отрицательный ионАтом , отдавая электрон, превращается в
- 10. 1. катион2. Анион3. Молекулу4. Положительный ионАтом, принимая электрон, превращается в
- 11. 1. HCL + AqNO32) Na2S + CuSO43)
- 12. Формулы реагентов
- 13. + 2-2H
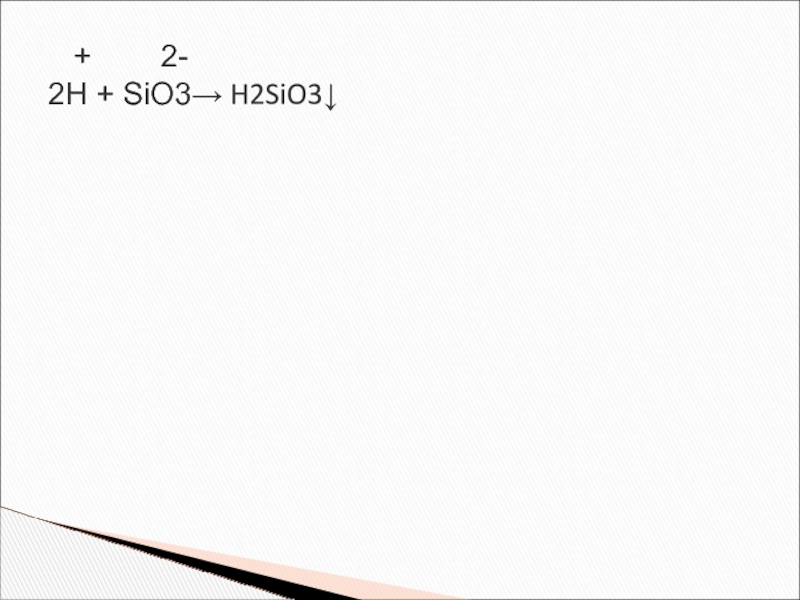
- 14. + 2- 2H + SiO3→ H2SiO3↓
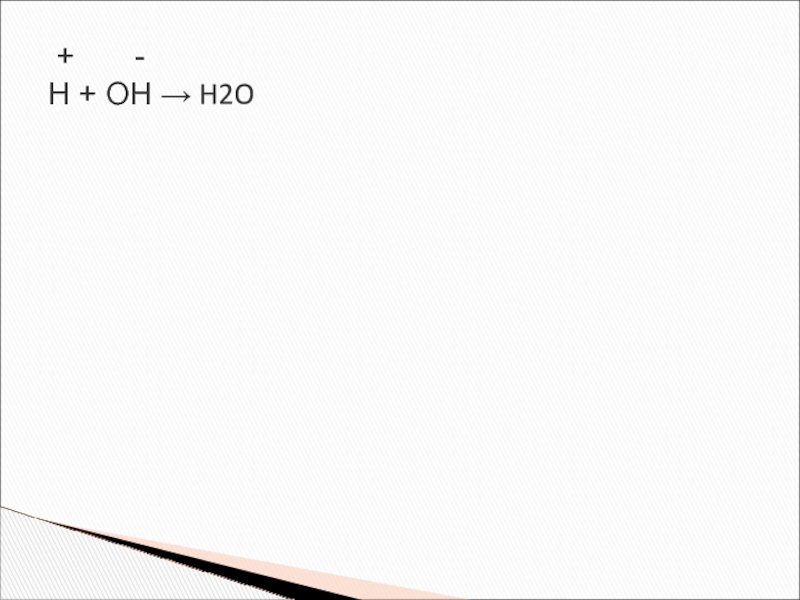
- 15. + - H + OH → H2O
- 16. 1) K2CO3 + HNO3→2) AL(OH)3 + BaCL2→3)
- 17. Краткое ионное уравнение
- 18. 1. Какая масса нитрата магния образуется при
Слайд 2 Электролитическая диссоциация;
электролиты;
неэлектролиты;
ионы;
степень э.д.;
кислоты с точки
основания с точки зрения ТЭД;
соли с точки зрения ТЭД.
Работа с понятиями:
Слайд 51) Кристаллизация
2) Соединение
3) Притяжение
4) ассоциация
3. процесс, обратный процессу диссоциации
Слайд 8Название вещества характеристика вещества
А) нитрат калия
Б) угольная кислота 2) слабый электролит
В) сахар 3) сильный электролит
Г) гидроксид лития
Установите соответствие между названием вещества и его характеристикой
Слайд 111. HCL + AqNO3
2) Na2S + CuSO4
3) BaCL2 + HNO3
4) NH4CL
ответ подтвердить уравнениями
Реакция в растворе не идет между
Слайд 12Формулы реагентов причина взаимодействия
А) KNO3
Б) AqNO3 + HCL→ 2) выделение газа
В) Na2S + HCL→ 3) образование слабого
Г) KOH + HCL→ электролита
4) реакция не идет
Ответ подтвердите уравнениями.
Установите соответствие между формулами реагентов и причинами их взаимодействия
Слайд 13 + 2-
2H + SO3 →H2O +
Для краткого ионного уравнения составить
молекулярное и полное ионное уравнения
Слайд 161) K2CO3 + HNO3→
2) AL(OH)3 + BaCL2→
3) MqO + HCL→
4) HNO2
5) CuCL2 + K2SO4→
Составить уравнения реакций ионного обмена между:
Слайд 17Краткое ионное уравнение исходные вещества
А) H2S +2OH→S +2H2O 1) Na2S + HCL →
2- + 2) Na2S + CuCI2 →
Б) S + 2H → H2S 3) H2S + Cu(OH)2 →
2+ 2- 4) H2S + CuCL2 →
В) Cu + S → CuS 5) H2S + NaOH →
2+ +
Г) H2S + Cu →CuS + 2H
Установите соответствие между сокращенным ионным уравнением и исходными веществами
Слайд 181. Какая масса нитрата магния образуется при взаимодействии 20г. оксида магния
2. Какой объем (при н.у.) углекислого газа выделится при действии раствора, содержащего 30г соляной кислоты, на 25г карбоната кальция?
3. Вычислите массу соли, полученную при действии на 5,35г гидроксида железа (III) с раствором, содержащим 10г азотной кислоты.
Решить задачи: