- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Коррозия металлов
Содержание
- 1. Презентация по теме Коррозия металлов
- 2. Коррозия (от лат. corrodere - разъедать)- самопроизвольное
- 3. Причиной возникновения и протекания процессов коррозии является
- 4. Виды коррозииХимическаяЭлектрохимическаяобразование ржавчиныкоррозия полотенцесушителя
- 5. Химическая коррозия - это разрушение металлов (сплавов)
- 6. Чаще всего коррозии подвергаются изделия из железа.
- 7. Посмотрите видео и сделайте вывод о роли кислорода в процессе коррозии железа.
- 8. Электрохимическая коррозия - это разрушение более активного
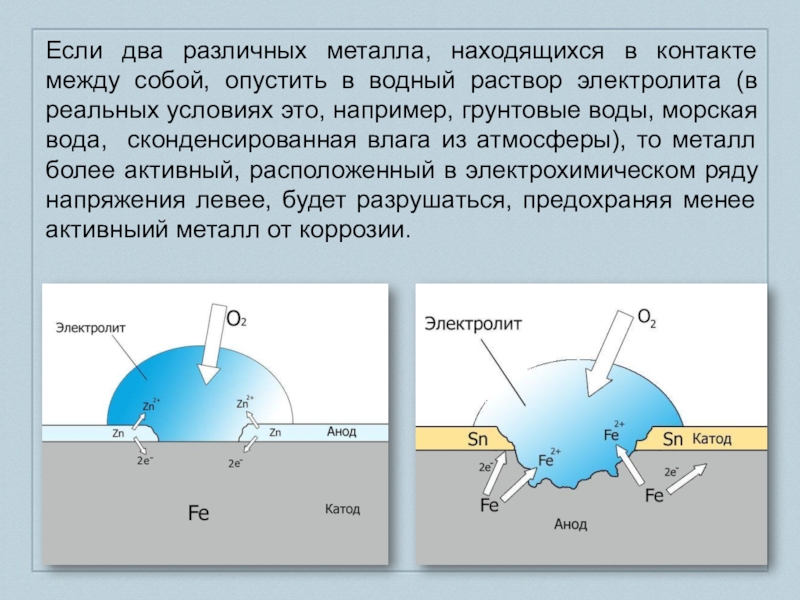
- 9. Если два различных металла, находящихся в контакте
- 10. Способы защиты металлов от коррозииНанесение защитных покрытий
- 11. б) Металлические покрытия. Предохраняемый металл можно покрыть
- 12. 2. Использование нержавеющих сталей, содержащих специальные добавки.
- 13. 3. Подавление влияния коррозийной среды.а) Введение в
- 14. 4.Электрохимические методы.а) Создание контакта с более
- 15. б) Катодная защита. Защищаемая конструкция или деталь присоединяется к отрицательному полюсу источника электроэнергии.
- 16. Ресурсы:Учебник: «Химия» 8 класс, О.С. Габриелянhttp://www.school-collection.edu.ru/catalog/rubr/d05469af-69bd-11db-bd13-0800200c9c09/75748/?interface=pupil&class=51&subject=31http://www.okorrozii.com/korrozia-radiatorov-batarei.htmlКартинки: Яндекс;http://chemistry-chemists.com/N3_2012/S1/ChemistryAndChemists_3_2012-S1-12.html
Слайд 2Коррозия (от лат. corrodere - разъедать)- самопроизвольное разрушение металлов и сплавов
коррозия меди
коррозия серебра
коррозия железа
Слайд 3Причиной возникновения и протекания процессов коррозии является неустойчивость материалов к определенным
Ежегодно коррозия наносит огромнейший ущерб народному хозяйству каждой страны. В промышленно развитых странах убытки от коррозии за год составляют в среднем около 3 - 5% от внутреннего валового продукта. А потери металла достигают 12%. Ущерб от коррозии складывается не только от стоимости материалов, но и от затрат на изготовление пришедших в негодность конструкций, оборудования и различных изделий.
Слайд 5Химическая коррозия - это разрушение металлов (сплавов) – окисление, в результате
Окружающая среда:
газообразные вещества – окислители (например, O2); , жидкие вещества – неэлектролиты (например, H2О); высокая температура.
Сущность коррозии:
окислительно-восстановительный процесс.
Слайд 6Чаще всего коррозии подвергаются изделия из железа. Особенно сильно корродирует металл
Коррозия железа может быть описана упрощенным уравнением:
4Fe + 3O2 + 2H2О = 2Fe2O3·H2О (4Fe + 3O2 + 6H2О = 4 Fe(OH)3)
Гидратированный оксид железа Fе2O3·H2О и является тем, что люди называют ржавчиной. Это рыхлый порошок светло-коричневого цвета. Ржавый металл быстро теряет твёрдость и прочность по мере продвижения ржавчины в глубокие слои, кроме того, ржавчина придаёт изделиям из металла неэстетичный вид. Процесс коррозии будет продолжаться до тех пор, пока поверхность не будет окончательно разъедена ржавчиной, если вовремя не принять меры.
Слайд 8Электрохимическая коррозия - это разрушение более активного металла, находящегося в контакте
Окружающая среда содержит:
а) H+,
б) OH-,
в) H2O и O2 и др.
Сущность коррозии:
окислительно-восстановительный процесс, при этом возникает электрический ток за счет работы гальванического элемента.
Слайд 9Если два различных металла, находящихся в контакте между собой, опустить в
Слайд 10Способы защиты металлов от коррозии
Нанесение защитных покрытий на поверхность металла
а) Неметаллические
Слайд 11б) Металлические покрытия. Предохраняемый металл можно покрыть слоем другого металла: золота,
Один из самых старых способов - это лужение, или покрытие железного листа
слоем олова. Такое железо называют белой жестью.
Водосток из оцинкованного железа
Золочение куполов
Хромирование дисков
Слайд 122. Использование нержавеющих сталей, содержащих специальные добавки. Например, «нержавейка», из которой
Слайд 133. Подавление влияния коррозийной среды.
а) Введение в рабочую среду, где находятся
Такие вещества называют ингибиторами коррозии.
Ингибиторы - это вещества, которые замедляют протекание химической реакции.
Ингибиторы коррозии вводят в замкнутые системы охлаждения, в нефтепродукты и даже впрыскивают в газопроводы для снижения коррозии труб изнутри.
б) Деаэрация - удаление кислорода и других газов из жидкости.