- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Кальций и его соединения
Содержание
- 1. Презентация по теме Кальций и его соединения
- 2. О каком элементе идет речь? В
- 3. Общая характеристикаCa +20 2ē, 8ē, 8 ē,
- 4. История открытия кальция
- 5. Положение в периодической системе. Строение атомовЩелочноземельные
- 6. Природные соединения кальция: известняк CaCO3 и его применениеЦементСтеклоНегашеная известь CaOГашеная известь Ca(OH)2
- 7. Природные соединения кальция: мел CaCO3 и его применениеШкольные мелкиЗубная пастаМелки для портныхМел для побелки
- 8. Природные соединения кальция: мрамор CaCO3 и его применениеСкульптураНабережнаяИндийский мавзолей Тадж-МахалСтанции метро
- 9. Природные соединения кальция - минералыГипс CaSO4. 2H2OФлюорит
- 10. Кальций в живых организмахЯйца птицКораллыРаковины моллюсковРакушечный известнякСкелет животных
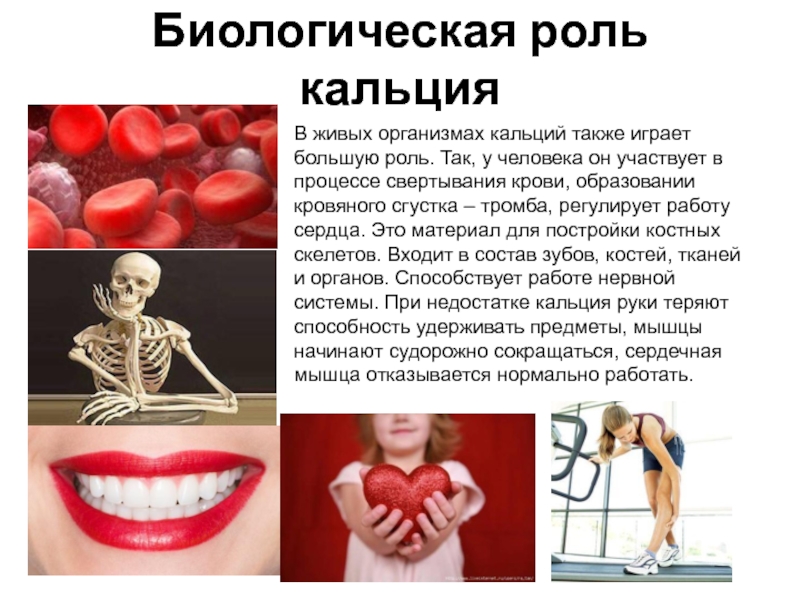
- 11. Биологическая роль кальцияВ живых организмах кальций также
- 12. Содержание кальция в продуктах питанияНорма в день1,5г:
- 13. Содержание магния в продуктах питаниягречневой крупе Гречневая
- 14. Секреты красивой улыбки
- 15. Кальций в строительствеСа(ОН)2+ CO2 = СаСОз +Н2ОCa(OH)2+SiO2 = CaSiO3+H2O
- 16. В интересной и причудливой форме встречается карбонат
- 17. Творения Микеланджело (мрамор)Скорчившийся мальчик. ЭрмитажОплакивание ХристаРаб, рвущий путы
- 18. Применение гипса Сульфат кальция встречается в природе
- 19. Химические свойства кальция2Са +О2 =2СаОСа + Cl2
- 20. Домашнее задание 1.параграф 12, знать формулы,
- 21. РефлексияКак вы считаете, интересной ли была для вас сегодняшняя встреча? Что вам запомнилось больше всего?Ваши предложения.
Слайд 1Кальций, его соединения
Солохина Любовь Викторовна,
учитель химии МБОУ СОШ № 10
г.
Слайд 2О каком элементе идет речь?
В проезде ученическом
Есть дом
Слайд 3Общая характеристика
Ca +20 2ē, 8ē, 8 ē, 2ē
Название элемента происходит от
Слайд 4История открытия кальция
Хэмфри Дэви в 1808 г. в 1808 г. выделил металлический кальций электролитическим методом.
Слайд 5Положение в периодической системе.
Строение атомов
Щелочноземельные металлы в периодической системе находятся
Являются сильными восстановителями, отдают 2 ē, во всех соединениях проявляют степень окисления +2.
Mg +12 2ē, 8ē, 2ē
Ca +20 2ē, 8ē, 8 ē, 2ē
Sr +38 2ē, 8ē, 18 ē, 8ē, 2ē
Ba +56 2ē, 8ē, 18 ē, 18 ē, 8ē, 2ē
Слайд 6Природные соединения кальция:
известняк CaCO3 и его применение
Цемент
Стекло
Негашеная известь CaO
Гашеная известь
Слайд 7Природные соединения кальция:
мел CaCO3 и его применение
Школьные мелки
Зубная паста
Мелки для
Мел для побелки
Слайд 8Природные соединения кальция:
мрамор CaCO3 и его применение
Скульптура
Набережная
Индийский мавзолей Тадж-Махал
Станции метро
Слайд 9Природные соединения кальция - минералы
Гипс CaSO4. 2H2O
Флюорит CaF2
Доломит
В виде солей кальций
Аргонит
Слайд 10Кальций в живых организмах
Яйца птиц
Кораллы
Раковины моллюсков
Ракушечный известняк
Скелет животных
Слайд 11Биологическая роль кальция
В живых организмах кальций также играет большую роль. Так,
Слайд 12Содержание кальция в продуктах питания
Норма в день1,5г: 1 стакан молока +
Помните! Кальций усваивается в нашем организме только в присутствии жиров: на каждые 0, 06 г кальция нужно съесть 1г жира.
Молочные продукты
Салат
Рыба
Петрушка
Слайд 13Содержание магния в продуктах питания
гречневой крупе
Гречневая крупа
Пшённая крупа
Шпинат
Арбуз
Фасоль , горох
Орехи фундук
Слайд 16В интересной и причудливой форме встречается карбонат кальция в пещерах
Сталактит,
Сталактит, или капельник
Сталагмит
Сталагнат
Са(ОН)2 + СО2 = СаСО3 +Н2О
СаСО3 +Н2О + СО2 = Са(НСО3)2
Слайд 17Творения Микеланджело (мрамор)
Скорчившийся мальчик. Эрмитаж
Оплакивание Христа
Раб, рвущий путы
Слайд 18Применение гипса
Сульфат кальция встречается в природе в виде минерала гипса
Слайд 19Химические свойства кальция
2Са +О2 =2СаО
Са + Cl2 = СаCl2
Са + S=
3Са + N2 = Са3N2
Са + H2 = СаH2
Са + H2O = Са(OH)2 + H2
5Са + Nb2O5 = 5СаO + 2Nb
Слайд 20Домашнее задание
1.параграф 12, знать формулы, названия, применение соединений кальция.
2. Попробуйте сочинить стихотворение или рассказ про кальций и его соединения и прочитать нам его на следующем уроке.
Слайд 21Рефлексия
Как вы считаете, интересной ли была для вас сегодняшняя встреча?
Что
Ваши предложения.