- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по теме Генетическая связь
Содержание
- 1. Презентация по теме Генетическая связь
- 2. Алиса (в Стране Чудес Чеширскому коту):– Скажите,
- 3. От простого – к сложномуСостав Строение Свойства
- 4. H3C-O-CH3CH3-CH2-CH36CУГЛЕРОД12,011Основные классы органических веществH2C=CH─CH2─CH3HC≡C─CH2─CH3H2C=CH─CH=CH2CH3─CH2─OHCH3─CH2─NH2CH3─CH2─NO2CH4
- 5. Стратегия синтеза«Я хочу воспеть хвалу сотворению молекул
- 6. СO + H2Ru, 1000 атм, 1500CThO2, 600
- 7. СnH2n+2Схема образования σ-связей в молекуле метанаМодели молекул
- 8. СH3Cl – МЕТИЛХЛОРИД CH4 МЕТАНС – САЖА
- 9. СnH2nСхема образования σ- связей с участием sp2-гибридных
- 10. C2H4 ЭтиленПолимеризация H2O, H+ ГидратацияCl2 ХлорированиеОкисление ЭТИЛОВЫЙ
- 11. СnH2n-2Схема образования σ- связей и π –
- 12. C2H2 HСl, Hg2+H2O, Hg2+Реакция КучероваСакт, 6000СтримеризацияСИНТЕЗЫ НА ОСНОВЕ АЦЕТИЛЕНАСuCl2, HCl, NH4ClдимеризацияROHHCN, СuCl, HCl, 800 CВолокна
- 13. Слайд 13
- 14. Схема образования π-связей в молекуле бензолаДелокализация электронной
- 15. БЕНЗОЛH2/Pt, 1800 Cгидрирование СИНТЕЗЫ НА ОСНОВЕ БЕНЗОЛАНИТРОБЕНЗОЛ
- 16. СИНТЕЗЫ НА ОСНОВЕ МЕТАНОЛАСH3OH ВИНИЛМЕТИЛОВЫЙ ЭФИРДИМЕТИЛАНИЛИНC6H5N(CH3)2ДИМЕТИЛОВЫЙ ЭФИРCH3–O–CH3МЕТИЛАМИНСН3NH2ВИНИЛАЦЕТАТМЕТИЛХЛОРИДСН3Сl СuO, tHClNH3МЕТИЛТИОЛСН3SHH2S, tС6H5NH2+ COH+, t
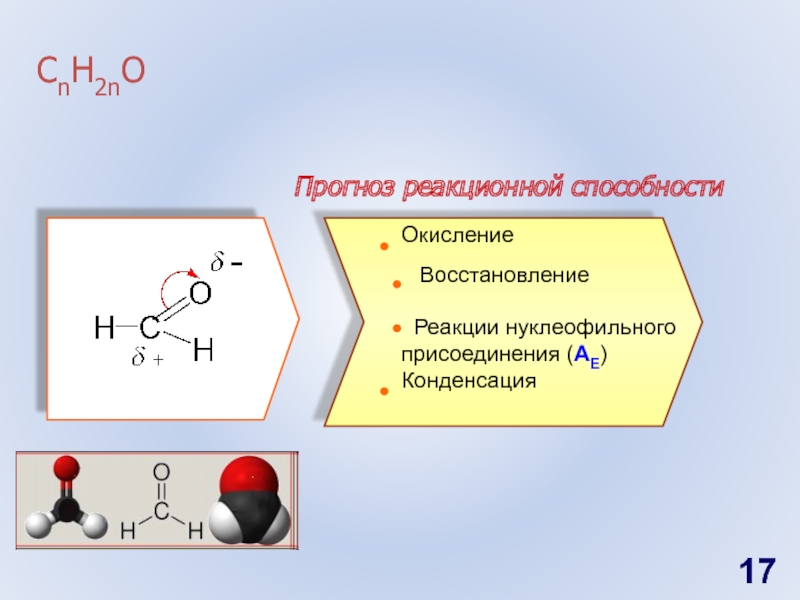
- 17. СnH2nO Прогноз реакционной способностиОкисление Восстановление Реакции нуклеофильного присоединения (AE)Конденсация
- 18. СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДАМЕТАНОЛСH3OH[O] [H] 1861 г. А.М. Бутлеров
- 19. CxHyOz Генетическая связь кислородсодержащих органических соединенийАЛЬДЕГИДЫ
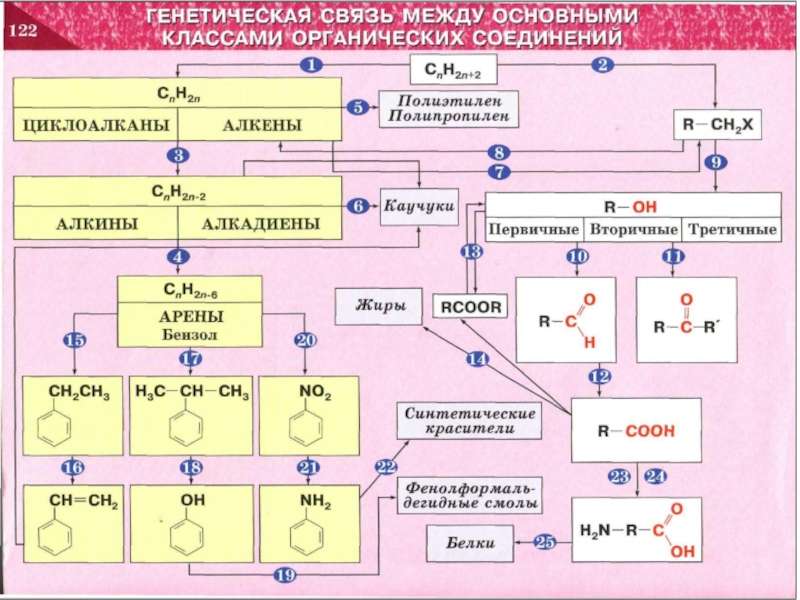
- 20. ГЕНЕТИЧЕСКАЯ СВЯЗЬ МЕЖДУ ОСНОВНЫМИ КЛАССАМИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
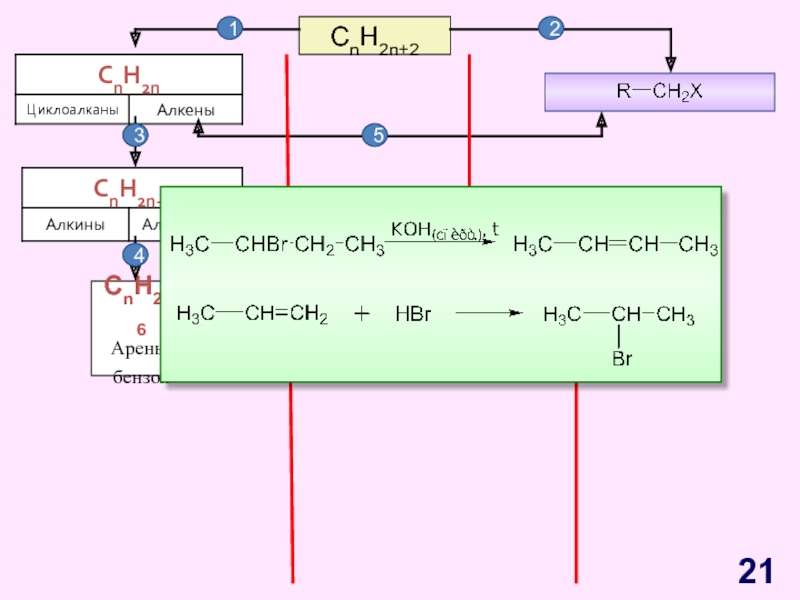
- 21. CnH2n+2CnH2n-6Арены, бензол12345
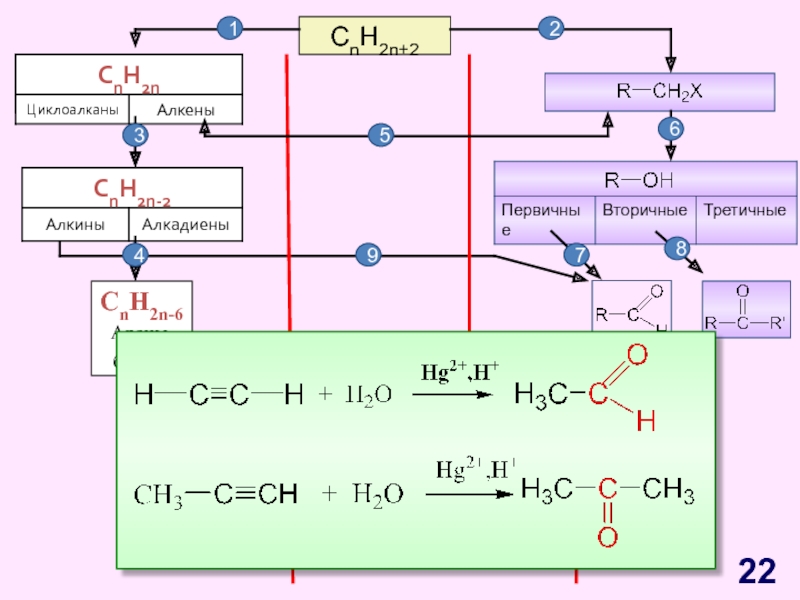
- 22. CnH2n+2CnH2n-6Арены, бензол123456789
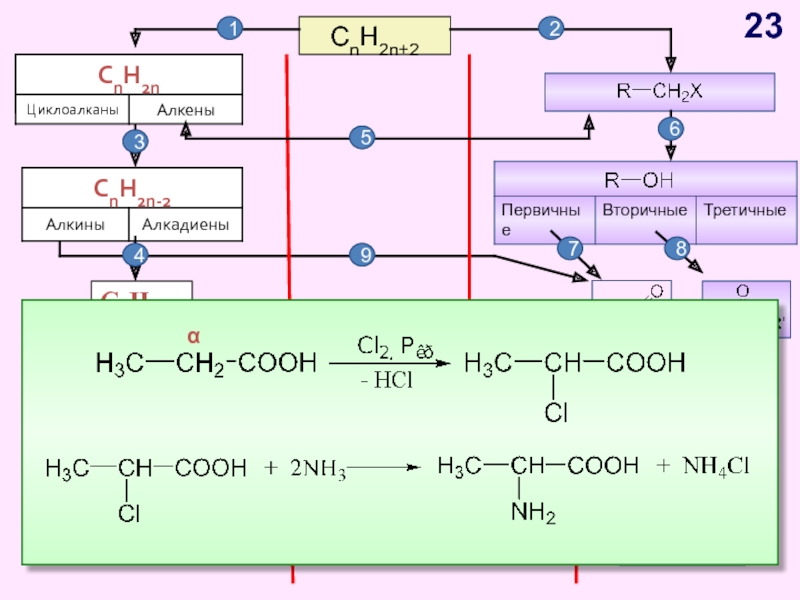
- 23. CnH2n+2CnH2n-6Арены, бензол1245367891011α
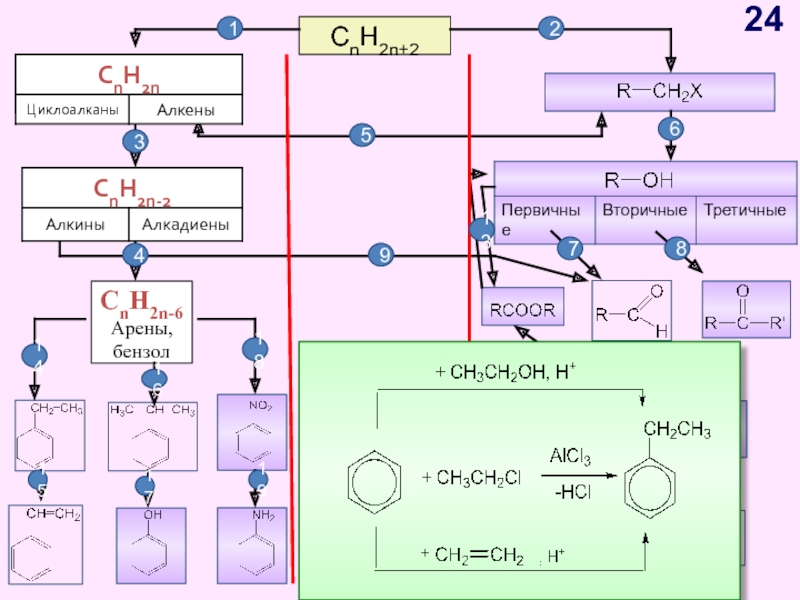
- 24. CnH2n+2CnH2n-6Арены, бензол12345678910111213141517191618
- 25. CnH2n+2CnH2n-6Арены, бензолПолиэтиленПолипропилен12Каучуки3567891011121314418161719152021Катализатор Циглера – Натта (1963 г)
- 26. CnH2n+2CnH2n-6Арены, бензолПолиэтиленПолипропиленКаучукиЖирыФенолформаль-дегидные смолы123456920211213781011181416171519222323
- 27. CnH2n+2CnH2n-6Арены, бензолПолиэтиленПолипропиленКаучукиЖирыСинтетические красителиФенолформаль-дегидные смолы12345206978131210111418211615171922232324
- 28. Применение анилина АНИЛИНН.Н. Зинин(1812 – 1880)Лекарственные веществаКрасителиВзрывчатые
- 29. CnH2n+2CnH2n-6Арены, бензолПолиэтиленПолипропиленКаучукиЖирыСинтетические красителиФенолформаль-дегидные смолыБелки1236520232542113781418221210112324161715199
- 30. Спасибо за внимание !
- 31. Слайд 31
Слайд 2Алиса (в Стране Чудес Чеширскому коту):
– Скажите, а куда мне отсюда
Чеширский кот:
– Это зависит от того, куда Вы
хотите придти?
Слайд 4H3C-O-CH3
CH3-CH2-CH3
6
C
УГЛЕРОД
12,011
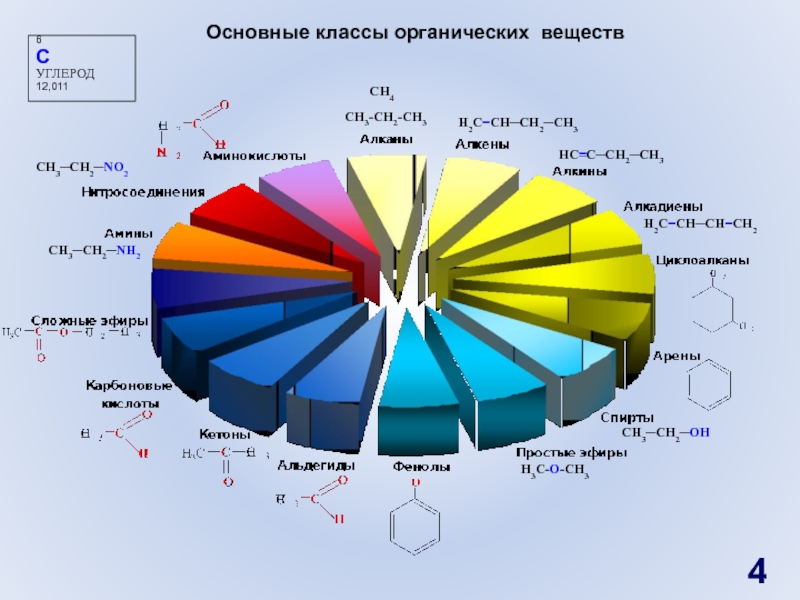
Основные классы органических веществ
H2C=CH─CH2─CH3
HC≡C─CH2─CH3
H2C=CH─CH=CH2
CH3─CH2─OH
CH3─CH2─NH2
CH3─CH2─NO2
CH4
Слайд 5Стратегия синтеза
«Я хочу воспеть хвалу сотворению молекул – химическому синтезу…
…Я глубоко
Роальд Хоффман
(Нобелевская премия по химии 1981 г)
Выбор исходного сырья
Построение углеродного остова молекулы
Введение, удаление или замена функциональной группы
Защита группы
Стереоселективность
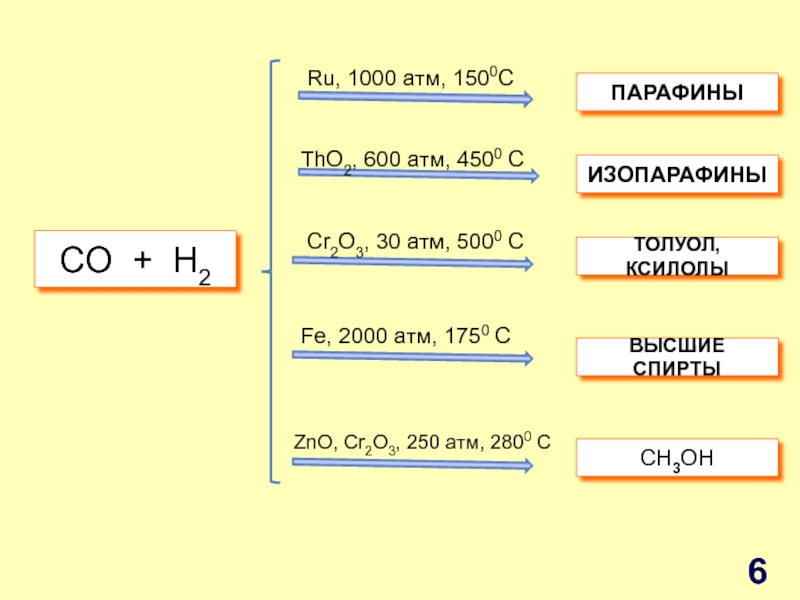
Слайд 6СO + H2
Ru, 1000 атм, 1500C
ThO2, 600 атм, 4500 C
Cr2O3, 30
Fe, 2000 атм, 1750 C
ZnO, Cr2O3, 250 атм, 2800 C
ПАРАФИНЫ
ИЗОПАРАФИНЫ
ТОЛУОЛ, КСИЛОЛЫ
ВЫСШИЕ СПИРТЫ
СH3OH
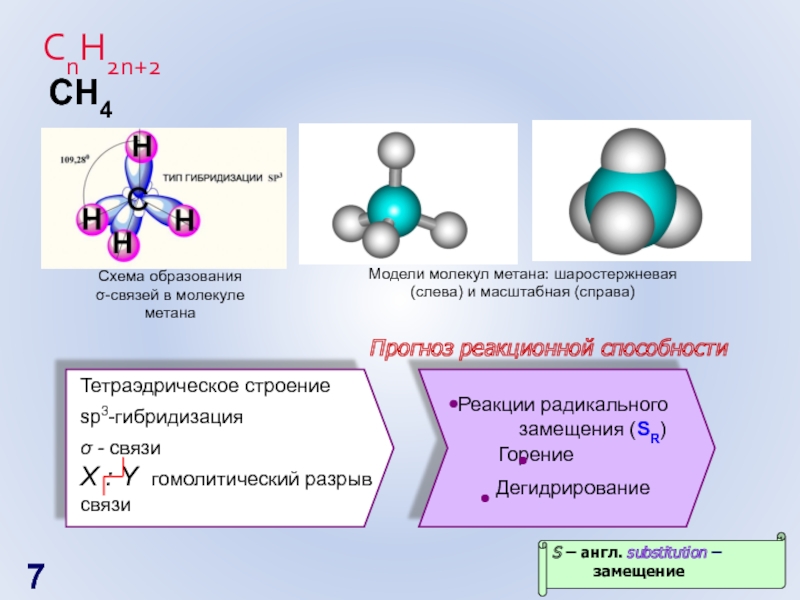
Слайд 7СnH2n+2
Схема образования σ-связей в молекуле метана
Модели молекул метана: шаростержневая (слева) и
СH4
Тетраэдрическое строение
sp3-гибридизация
σ - связи
X : Y гомолитический разрыв связи
Реакции радикального
замещения (SR)
Горение
Дегидрирование
Прогноз реакционной способности
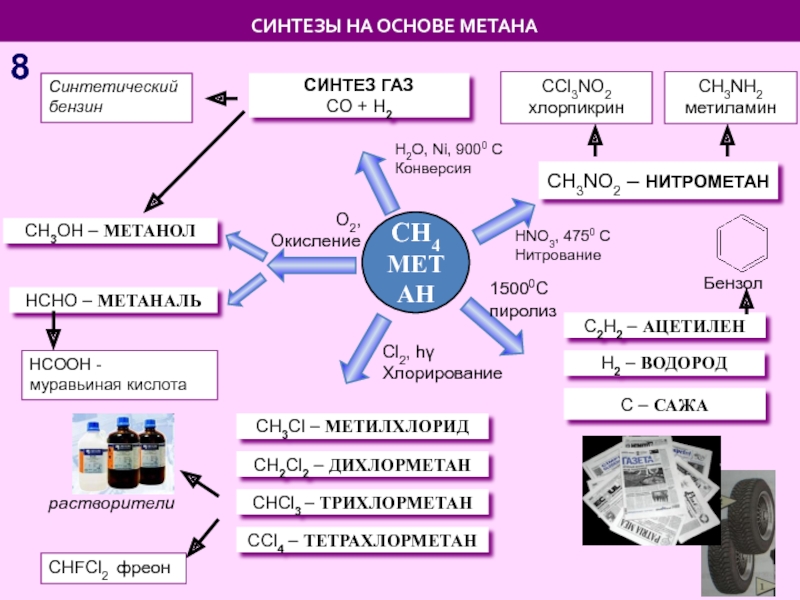
Слайд 8СH3Cl – МЕТИЛХЛОРИД
CH4
МЕТАН
С – САЖА
С2Н2 – АЦЕТИЛЕН
СH2Cl2
СHCl3 – ТРИХЛОРМЕТАН
СCl4 – ТЕТРАХЛОРМЕТАН
Н2 – ВОДОРОД
СИНТЕЗ ГАЗ
СO + H2
Сl2, hγ
Хлорирование
15000С пиролиз
Н2О, Ni, 9000 C
Конверсия
О2,
Окисление
СH3OH – МЕТАНОЛ
HCHO – МЕТАНАЛЬ
растворители
Бензол
СHFCl2 фреон
HCOOH -
муравьиная кислота
Синтетический бензин
СИНТЕЗЫ НА ОСНОВЕ МЕТАНА
СH3NO2 – НИТРОМЕТАН
СCl3NO2
хлорпикрин
СH3NH2 метиламин
HNO3, 4750 C
Нитрование
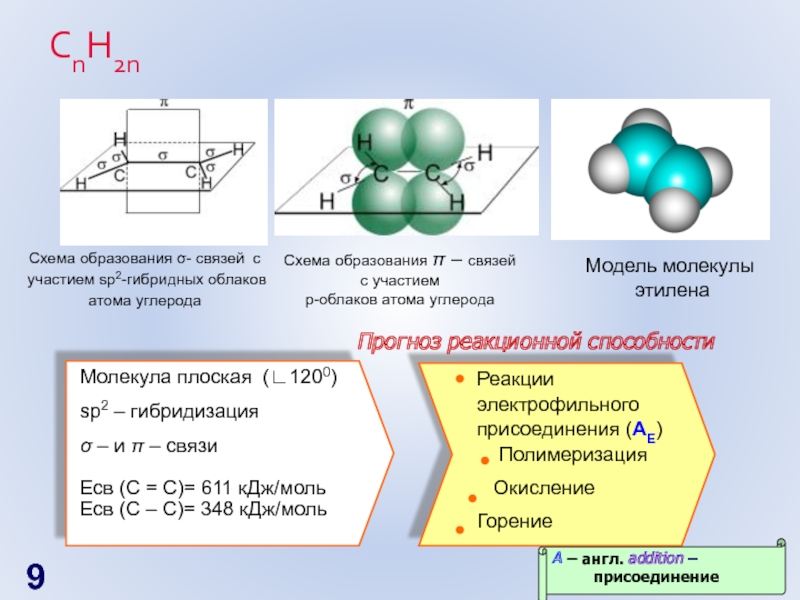
Слайд 9СnH2n
Схема образования σ- связей с
участием sp2-гибридных облаков
атома углерода
Схема образования π
с участием
p-облаков атома углерода
Модель молекулы
этилена
Реакции электрофильного присоединения (AE)
Полимеризация
Окисление
Горение
Молекула плоская (∟1200)
sp2 – гибридизация
σ – и π – связи
Есв (С = С)= 611 кДж/моль
Есв (С – С)= 348 кДж/моль
Прогноз реакционной способности
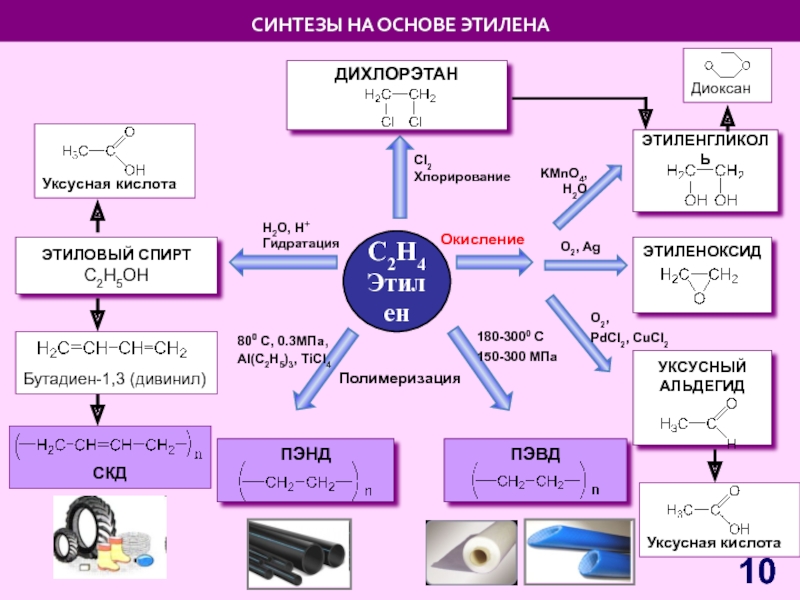
Слайд 10C2H4
Этилен
Полимеризация
H2O, H+ Гидратация
Cl2
Хлорирование
Окисление
ЭТИЛОВЫЙ СПИРТ
С2Н5OH
СИНТЕЗЫ НА ОСНОВЕ ЭТИЛЕНА
O2,
KMnO4,
H2O
O2,
PdCl2, CuCl2
180-3000 С
150-300 МПа
800 С, 0.3МПа, Al(C2H5)3, TiCl4
Уксусная кислота
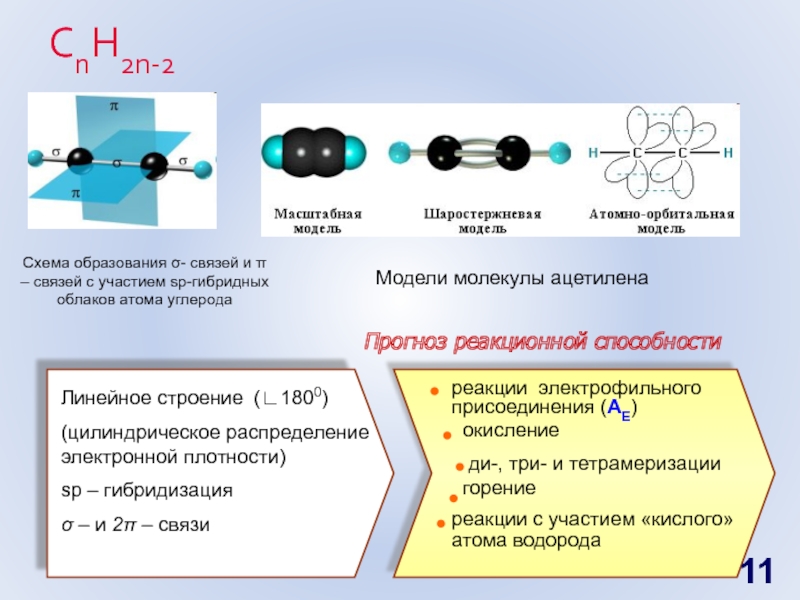
Слайд 11СnH2n-2
Схема образования σ- связей и π – связей с участием sp-гибридных
Модели молекулы ацетилена
реакции электрофильного присоединения (AE)
окисление
ди-, три- и тетрамеризации
горение
реакции с участием «кислого» атома водорода
Линейное строение (∟1800)
(цилиндрическое распределение электронной плотности)
sp – гибридизация
σ – и 2π – связи
Прогноз реакционной способности
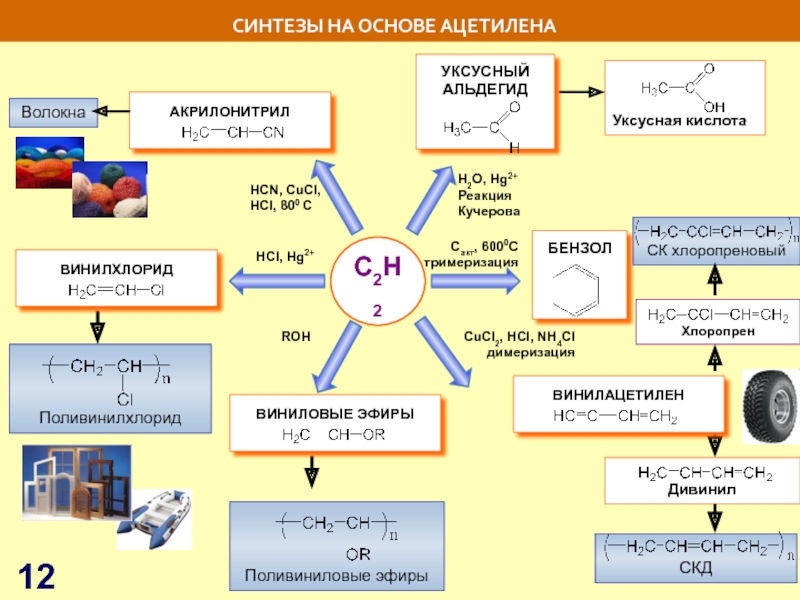
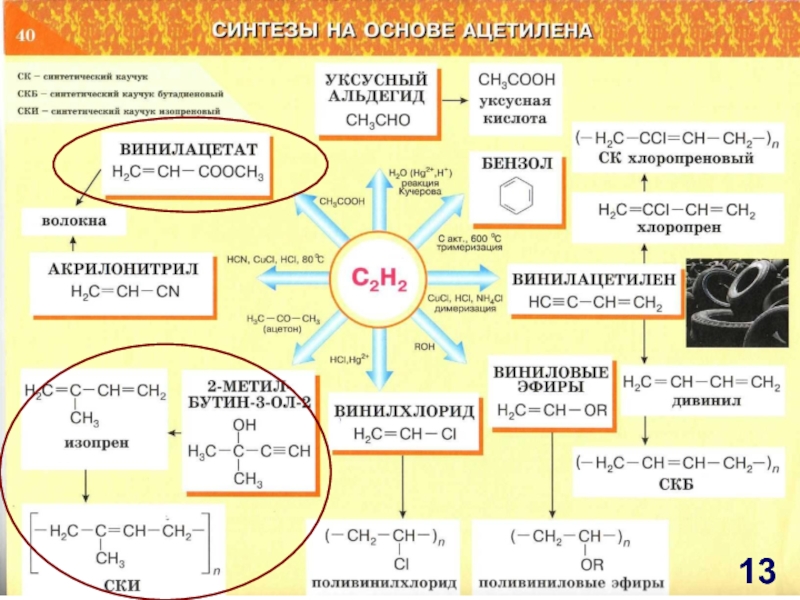
Слайд 12C2H2
HСl, Hg2+
H2O, Hg2+
Реакция
Кучерова
Сакт, 6000С
тримеризация
СИНТЕЗЫ НА ОСНОВЕ АЦЕТИЛЕНА
СuCl2, HCl, NH4Cl
димеризация
ROH
HCN,
HCl, 800 C
Волокна
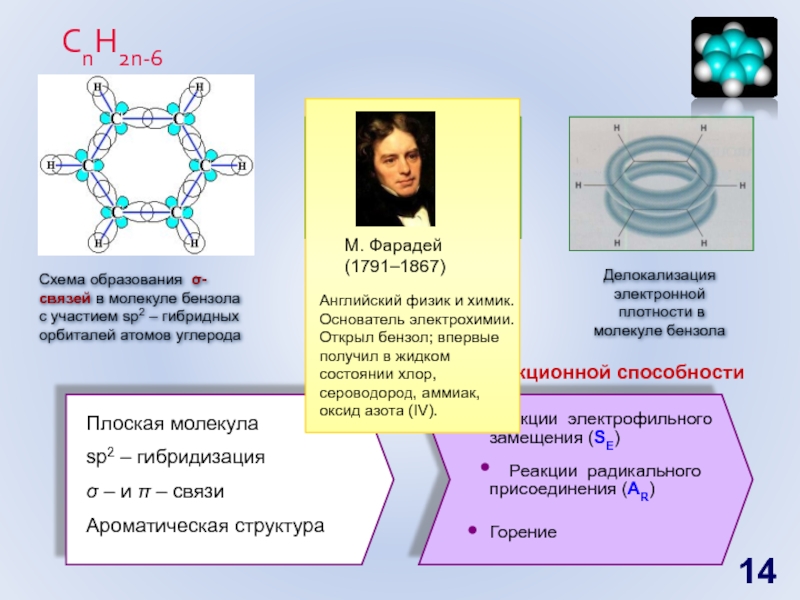
Слайд 14Схема образования π-связей в молекуле бензола
Делокализация электронной
плотности в молекуле бензола
Схема образования σ-связей в молекуле бензола с участием sp2 – гибридных орбиталей атомов углерода
СnH2n-6
Прогноз реакционной способности
Плоская молекула
sp2 – гибридизация
σ – и π – связи
Ароматическая структура
Реакции электрофильного замещения (SE)
Реакции радикального присоединения (АR)
Горение
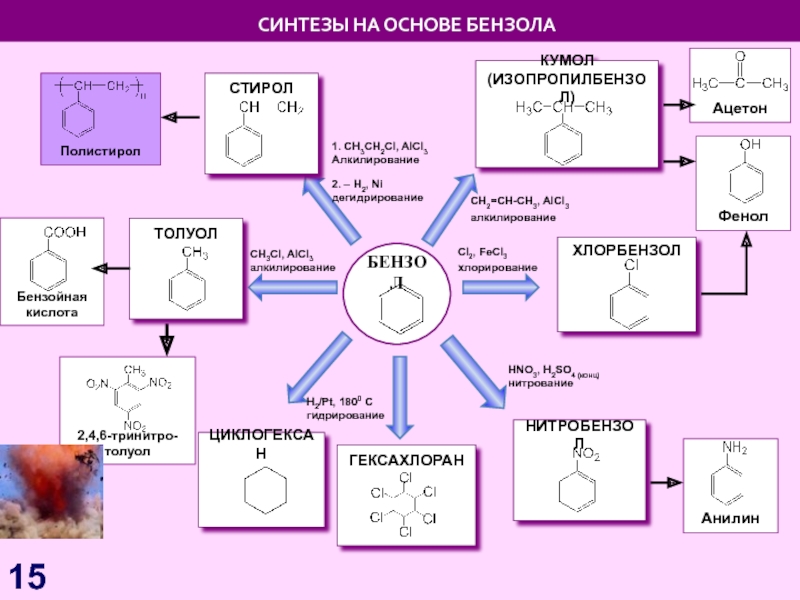
Слайд 15БЕНЗОЛ
H2/Pt, 1800 C
гидрирование
СИНТЕЗЫ НА ОСНОВЕ БЕНЗОЛА
НИТРОБЕНЗОЛ
Сl2, FeCl3 хлорирование
HNO3,
CH3Cl, AlCl3
алкилирование
2,4,6-тринитро-толуол
СТИРОЛ
1. СH3CH2Cl, AlCl3
Алкилирование
2. – H2, Ni
дегидрирование
СH2=CH-CH3, AlCl3 алкилирование
КУМОЛ
(ИЗОПРОПИЛБЕНЗОЛ)
ГЕКСАХЛОРАН
Слайд 16
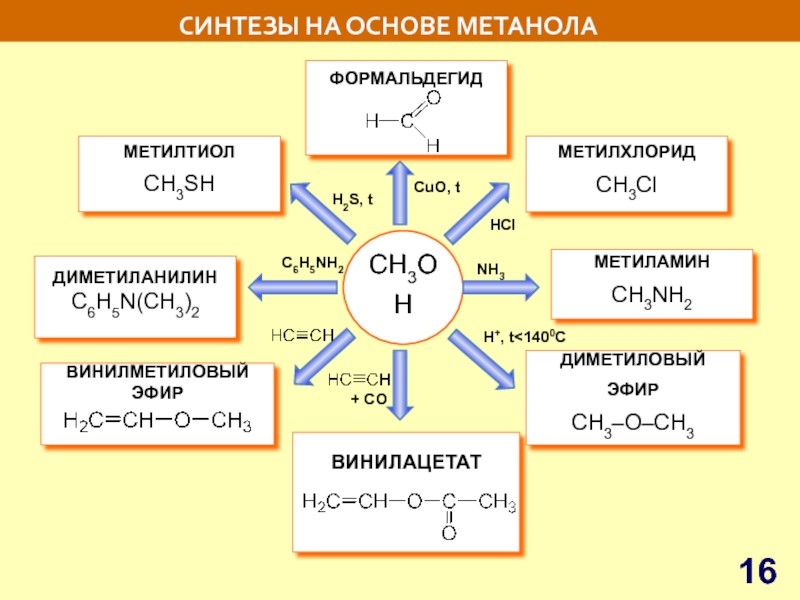
СИНТЕЗЫ НА ОСНОВЕ МЕТАНОЛА
СH3OH
ВИНИЛМЕТИЛОВЫЙ
ЭФИР
ДИМЕТИЛАНИЛИН
C6H5N(CH3)2
ДИМЕТИЛОВЫЙ ЭФИР
CH3–O–CH3
МЕТИЛАМИН
СН3NH2
ВИНИЛАЦЕТАТ
МЕТИЛХЛОРИД
СН3Сl
СuO, t
HCl
NH3
МЕТИЛТИОЛ
СН3SH
H2S, t
С6H5NH2
+ CO
H+,
Слайд 17СnH2nO
Прогноз реакционной способности
Окисление
Восстановление
Реакции нуклеофильного присоединения (AE)
Конденсация
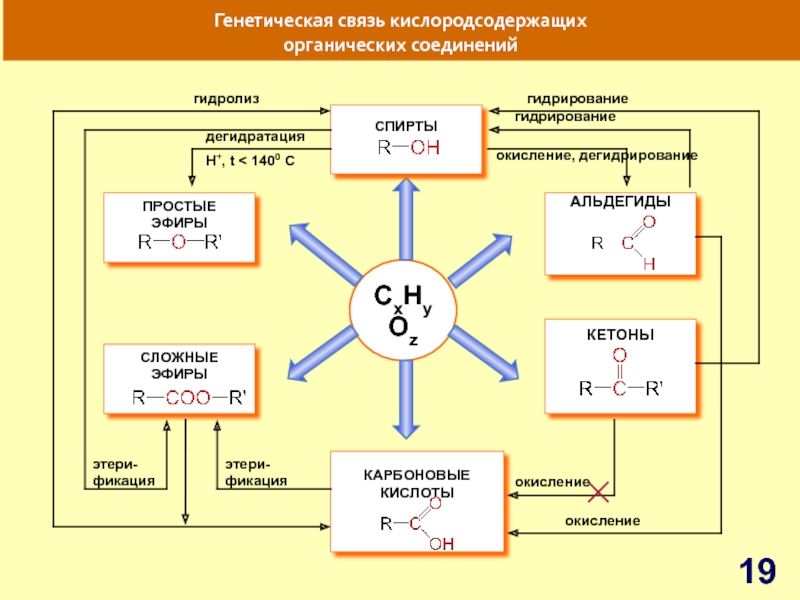
Слайд 19CxHyOz
Генетическая связь кислородсодержащих
органических соединений
АЛЬДЕГИДЫ
КАРБОНОВЫЕ
КИСЛОТЫ
КЕТОНЫ
СЛОЖНЫЕ
ЭФИРЫ
ПРОСТЫЕ
ЭФИРЫ
СПИРТЫ
гидролиз
дегидратация
гидрирование
гидрирование
окисление,
этери-
фикация
этери-
фикация
окисление
окисление
H+, t < 1400 C
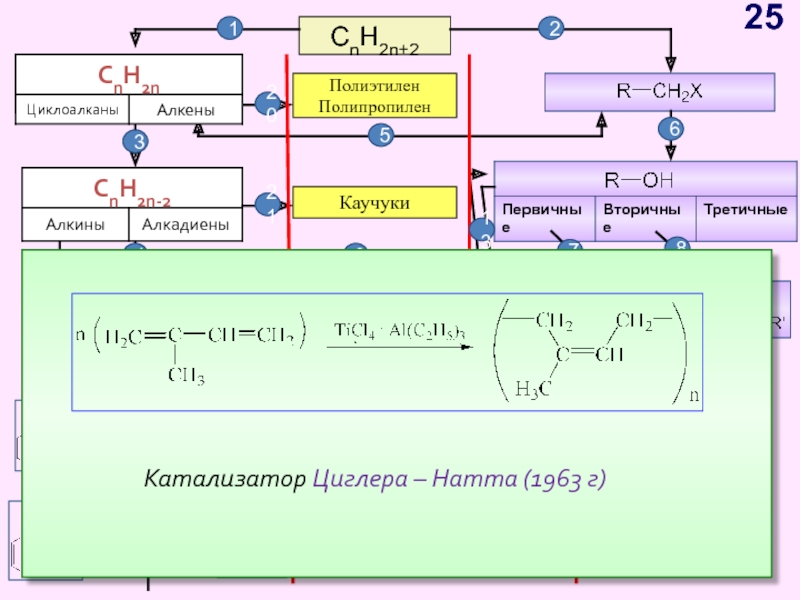
Слайд 25CnH2n+2
CnH2n-6
Арены,
бензол
Полиэтилен
Полипропилен
1
2
Каучуки
3
5
6
7
8
9
10
11
12
13
14
4
18
16
17
19
15
20
21
Катализатор Циглера – Натта (1963 г)
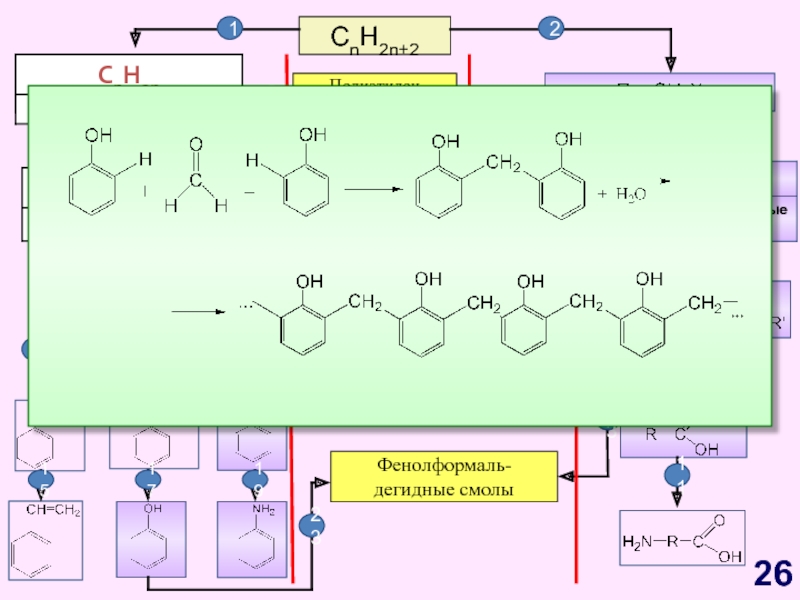
Слайд 26CnH2n+2
CnH2n-6
Арены,
бензол
Полиэтилен
Полипропилен
Каучуки
Жиры
Фенолформаль-
дегидные смолы
1
2
3
4
5
6
9
20
21
12
13
7
8
10
11
18
14
16
17
15
19
22
23
23
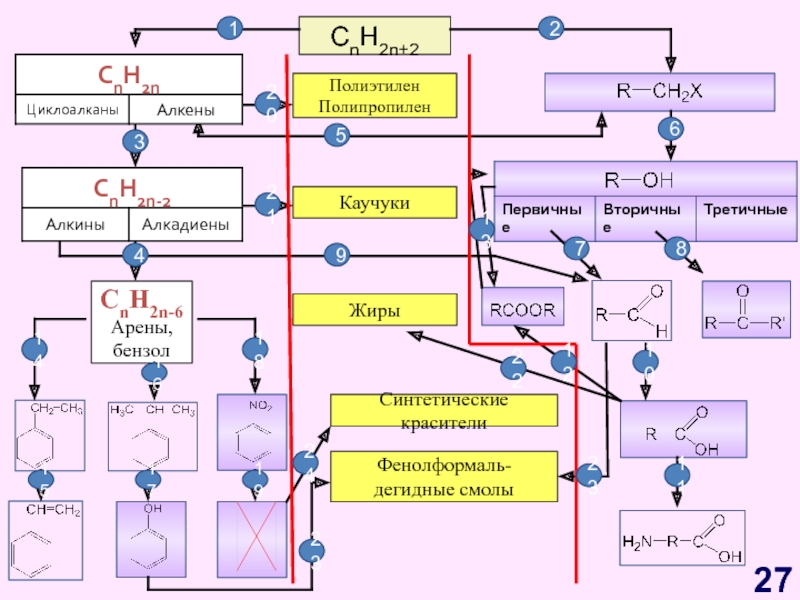
Слайд 27CnH2n+2
CnH2n-6
Арены,
бензол
Полиэтилен
Полипропилен
Каучуки
Жиры
Синтетические красители
Фенолформаль-
дегидные смолы
1
2
3
4
5
20
6
9
7
8
13
12
10
11
14
18
21
16
15
17
19
22
23
23
24
Слайд 28
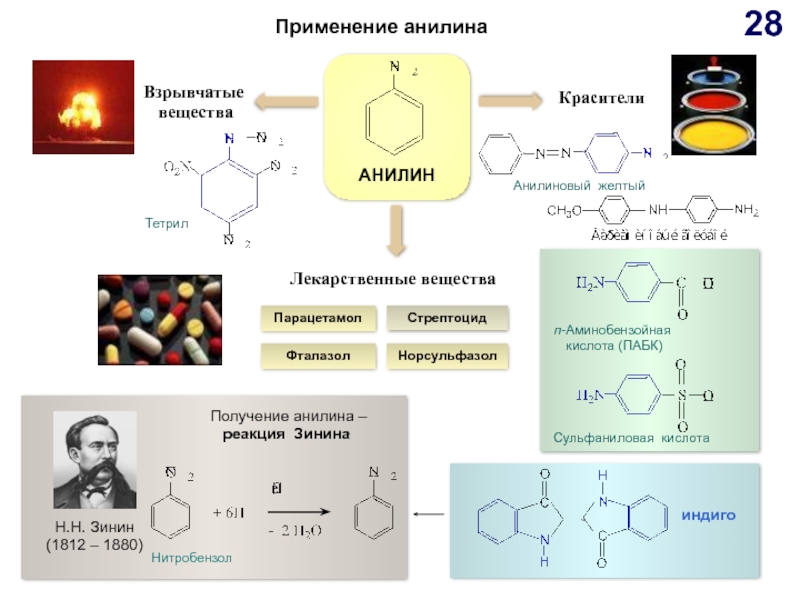
Применение анилина
АНИЛИН
Н.Н. Зинин
(1812 – 1880)
Лекарственные вещества
Красители
Взрывчатые
вещества
Cтрептоцид
Норсульфазол
Фталазол
Получение анилина
реакция Зинина
Тетрил
Анилиновый желтый
Нитробензол
п-Аминобензойная
кислота (ПАБК)
Сульфаниловая кислота
индиго
Парацетамол



![Презентация по теме Генетическая связь СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДАМЕТАНОЛСH3OH[O] [H] 1861 г. А.М. Бутлеров СИНТЕЗЫ НА ОСНОВЕ ФОРМАЛЬДЕГИДАМЕТАНОЛСH3OH[O] [H] 1861 г. А.М. Бутлеров](/img/tmb/1/89045/633657776c423fa10b38b0c1270501ae-800x.jpg)