- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по органической химии 10 класс к уроку Аминокислоты
Содержание
- 1. Презентация по органической химии 10 класс к уроку Аминокислоты
- 2. Аминокислотами называются азотосодержащие органические вещества, молекулы которых содержат
- 3. Слайд 3
- 4. Слайд 4
- 5. История химии аминокислот связаны с тремя открытиями.В
- 6. ИСТОРИЯ ОТКРЫТИЯВ 1896 г. Французские химики-органики Луи
- 7. История открытияВ 1909 г. Японский ученый К.Икеда
- 8. История открытия аминокислот Первая аминокислота
- 9. Слайд 9
- 10. Большинство микроорганизмов и растения создают все необходимые
- 11. Слайд 11
- 12. В клетках и тканях живых организмов встречается
- 13. Способы получения
- 14. Физические свойстваПо физическим свойствам аминокислоты резко отличаются
- 15. Химические свойства1. Кислотные свойстваа) Взаимодействие со щелочамиNH2 –CH2 –COOH
- 16. Аминокислоты – амфотерные вещества.3. Аминокислоты взаимодействуют друг
- 17. ПрименениеАминокислоты, преимущественно α-аминокислоты, необходимы для синтеза белков
- 18. ПРИМЕНЕНИЕ АМИНОКИСЛОТНаибольший интерес представляют 20 L-α-аминокислот (аланин,
- 19. Использование аминокислот Аминокислоты находят
- 20. Слайд 20
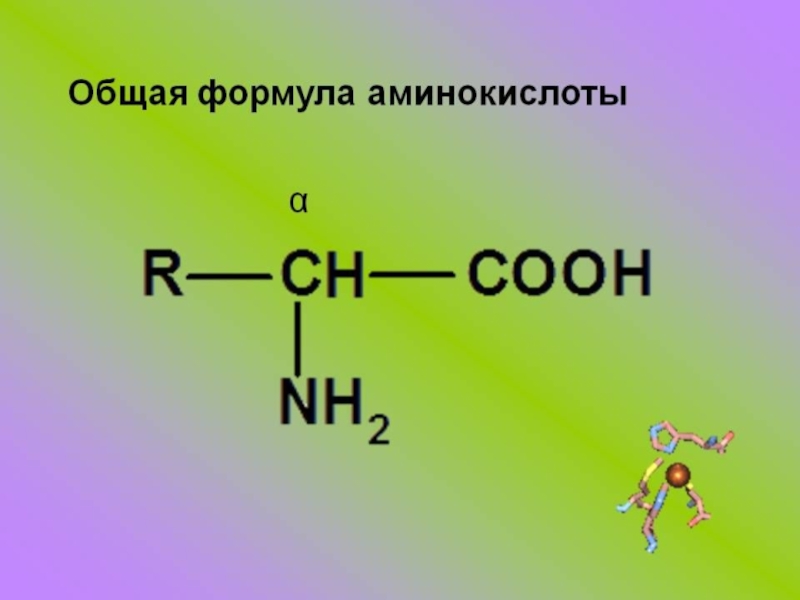
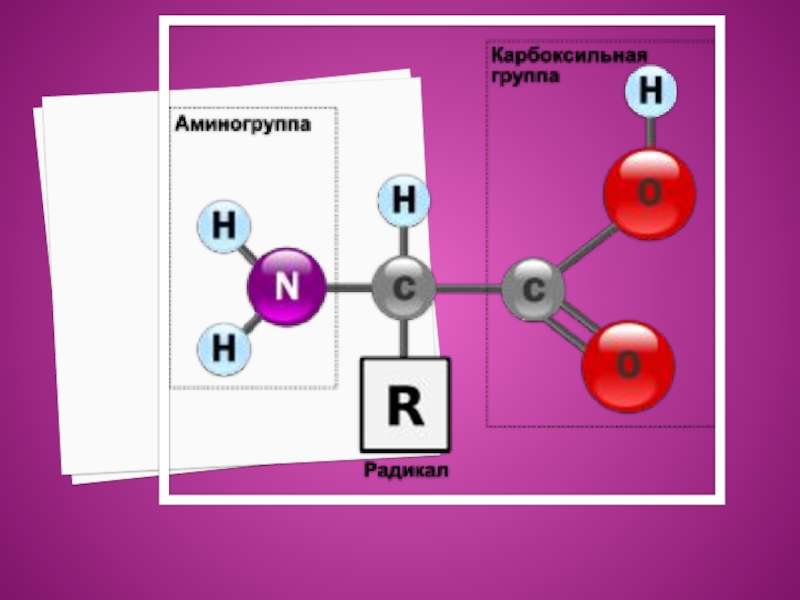
Аминокислотами называются азотосодержащие органические вещества, молекулы которых содержат карбоксильную группу – COOH и аминогруппу – NH2.NH2 –CH2 –COOH NH2 –CH2 –CH2 –COOHаминоуксусная кислота β-аминопропиновая кислотаCH3-CH-COOH α-аминопропиновая кислота | NH2
Слайд 2Аминокислотами называются азотосодержащие органические вещества, молекулы которых содержат карбоксильную группу – COOH
и аминогруппу – NH2.
NH2 –CH2 –COOH NH2 –CH2 –CH2 –COOH
аминоуксусная кислота β-аминопропиновая кислота
CH3-CH-COOH α-аминопропиновая кислота | NH2
NH2 –CH2 –COOH NH2 –CH2 –CH2 –COOH
аминоуксусная кислота β-аминопропиновая кислота
CH3-CH-COOH α-аминопропиновая кислота | NH2
Слайд 5История химии аминокислот связаны с тремя открытиями.
В 1806 г. открыто первое
аминокислотное производное — амид аспарагин.
В 1810 г. открыта первая аминокислота — цистин, которая была выделена из объекта небелковой природы — мочевых камней.
В 1820 г. аминокислота глицин впервые выделена из белкового гидролизата и более или менее тщательно очищена.
В 1810 г. открыта первая аминокислота — цистин, которая была выделена из объекта небелковой природы — мочевых камней.
В 1820 г. аминокислота глицин впервые выделена из белкового гидролизата и более или менее тщательно очищена.
Слайд 6ИСТОРИЯ ОТКРЫТИЯ
В 1896 г. Французские химики-органики Луи Никола Вокслен и Пьер
Жан Робике исследовали состав сока некоторых растений. Из сока спаржи им удалось выделить белое кристаллическое вещество, названное ими аспарагином. Эта была первая аминокислота, выделенная химиками из природных объектов.
Предприимчивые японцы давно заметили, что добавление в пищу приправы из сушеных водорослей усиливает ее вкус и аромат.
Предприимчивые японцы давно заметили, что добавление в пищу приправы из сушеных водорослей усиливает ее вкус и аромат.
Слайд 7История открытия
В 1909 г. Японский ученый К.Икеда выяснил, что причина такого
действия кроется в содержании в водорослях глутаминовой кислоты. Открытие было запатентовано и теперь во всем мире используют глутаминовую кислоту в качестве пищевой добавки, усиливающей вкус и аромат продукта (Е620).
HOOC-CH2-CH2-CHNH2-COOH
HOOC-CH2-CH2-CHNH2-COOH
Слайд 8
История открытия аминокислот
Первая аминокислота — аспарагин — была открыта в 1806, последняя из
аминокислот, обнаруженных в белках, — треонин — была идентифицирована в 1938. Каждая аминокислота имеет тривиальное (традиционное) название, иногда оно связано с источником выделения. Например, аспарагин впервые обнаружили в аспарагусе (спарже), глутаминовую кислоту — в клейковине (от англ. gluten — глютен) пшеницы, глицин был назван так за его сладкий вкус (от греч. glykys — сладкий).
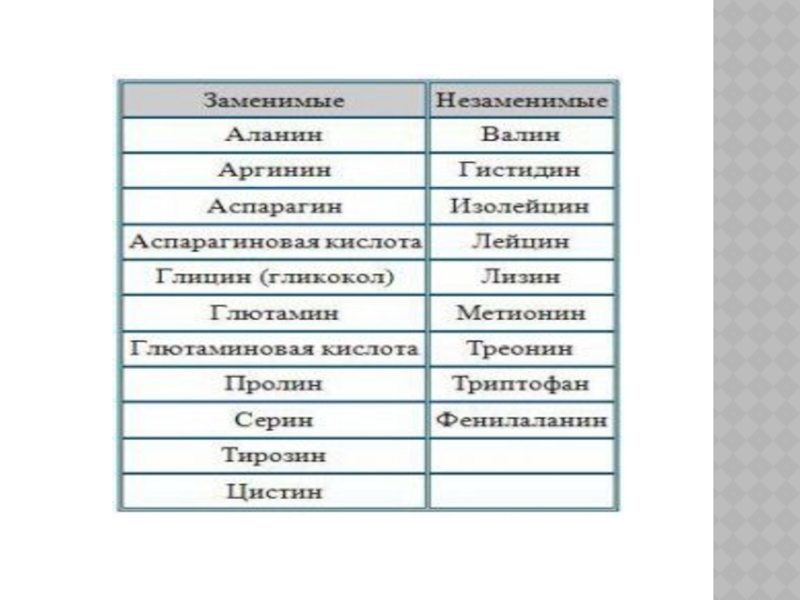
Слайд 10Большинство микроорганизмов и растения создают все необходимые им аминокислоты из более
простых молекул. В отличие от них животные организмы не могут синтезировать некоторые из аминокислот, в которых они нуждаются. Такие аминокислоты они должны получать в готовом виде, то есть с пищей. Поэтому, исходя из пищевой ценности, аминокислоты делят на незаменимые и заменимые. К числу незаменимых для человека аминокислот относятся валин, треонин, триптофан, фенилаланин, метионин, лизин, лейцин, изолейцин, а для детей незаменимыми являются также гистидин и аргинин. Недостаток любой из незаменимых аминокислот в организме приводит к нарушению обмена веществ, замедлению роста и развития.
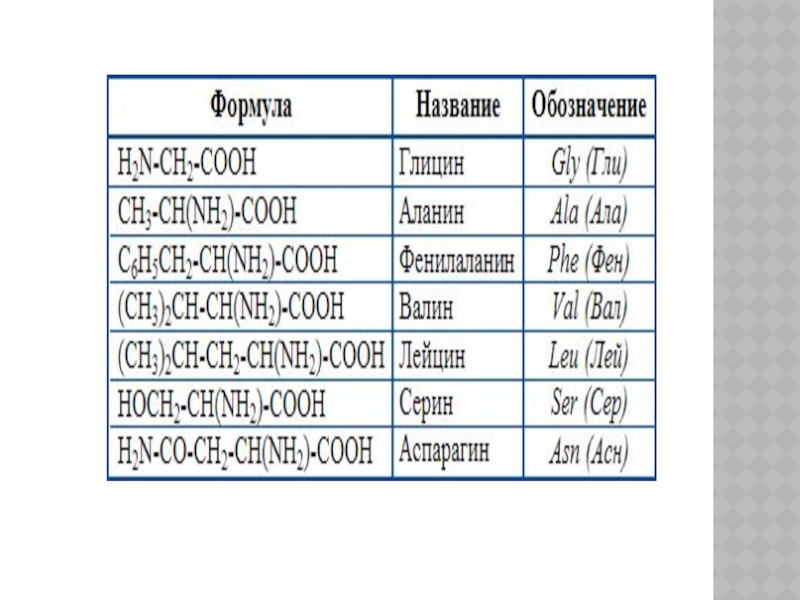
Слайд 12В клетках и тканях живых организмов встречается около 300 различных аминокислот,
но только 20 из них служат звеньями (мономерами), из которых построены пептиды и белки всех организмов (поэтому их называют белковыми аминокислотами). Последовательность расположения этих аминокислот в белках закодирована в последовательности нуклеотидов соответствующих генов . Остальные аминокислоты встречаются как в виде свободных молекул, так и в связанном виде. Многие из аминокислот встречаются лишь в определенных организмах, а есть и такие, которые обнаруживаются только в одном из великого множества описанных организмов.
Слайд 13Способы получения
Гидролиз белковых веществ.
Действием на галогенокислоты аммиака.
CH3–COOH + CI2→ CH2CI –COOH
Уксусная к-та →хлоруксусная к-та
CH2CI–COOH + NH3→ CH2NH2 –COOH
Слайд 14Физические свойства
По физическим свойствам аминокислоты резко отличаются от соответствующих кислот и оснований. Все
они кристаллические вещества, лучше растворяются в воде, чем в органических растворителях, имеют достаточно высокие температуры плавления; многие из них имеют сладкий вкус. Эти свойства отчётливо указывают на солеобразный характер этих соединений. Особенности физических и химических свойств аминокислот обусловлены их строением — присутствием одновременно двух противоположных по свойствам функциональных групп: кислотной и основной.
Слайд 15Химические свойства
1. Кислотные свойства
а) Взаимодействие со щелочами
NH2 –CH2 –COOH + NaOH →NH2 –CH2 –COONa +
H2O
б) Взаимодействие со спиртами
NH2 –CH2 –COOH + C2H5OH →
NH2 –CH2 –COOC2H5 + H2O
2. Основные свойства
Взаимодействие с кислотами
NH2 –CH2 –COOH + HCl → NH3Cl–CH2 –COOH
б) Взаимодействие со спиртами
NH2 –CH2 –COOH + C2H5OH →
NH2 –CH2 –COOC2H5 + H2O
2. Основные свойства
Взаимодействие с кислотами
NH2 –CH2 –COOH + HCl → NH3Cl–CH2 –COOH
Слайд 16Аминокислоты – амфотерные вещества.
3. Аминокислоты взаимодействуют друг с другом
NH2 –CH2 –COOH + NH2 –CH2 –COOH
→
NH2 –CH2 –CO-NH–CH2 –COOH + Н2О
дипептид
-СО–NH – пептидная группа (амидная группа)
NH2 –CH2 –CO-NH–CH2 –COOH + Н2О
дипептид
-СО–NH – пептидная группа (амидная группа)
Слайд 17Применение
Аминокислоты, преимущественно α-аминокислоты, необходимы для синтеза белков в живых организмах. Нужные
для этого аминокислоты человек и животные получают в виде пищи, содержащей различные белки. Последние подвергаются в пищеварительном тракте расщеплению на отдельные аминокислоты, из которых затем синтезируются белки, свойственные данному организму. Некоторые аминокислоты применяются в медицинских целях. Многие аминокислоты служат для подкормки животных.
Производные аминокислот используются для синтеза волокна, например капрона.
Производные аминокислот используются для синтеза волокна, например капрона.
Слайд 18ПРИМЕНЕНИЕ АМИНОКИСЛОТ
Наибольший интерес представляют 20 L-α-аминокислот (аланин, аргинин, аспарагин и другие),
входящих в состав белковых молекул. Смеси L-аминокислот, а также индивидуальные аминокислоты (например, метионин) применяют в медицине для парэнтерального питания больных с заболеваниями пищеварительных и других органов, при нарушениях обмена веществ и др.; лизин, метионин, треонин, триптофан - в животноводстве для обогащения кормов; глутамат натрия и лизин - в пищевой промышленности, γ-аминомасляная кислота (аминалон) - медиатор в центральной нервной системе, применяется как лекарственное средство при сосудистых заболеваниях головного мозга. Ароматические аминокислоты используют в синтезе красителей и лекарственных средств.
Слайд 19Использование аминокислот
Аминокислоты находят широкое применение в качестве пищевых добавок.
Например, лизином, трипто-фаном, треонином и метионином обогащают корма сель-скохозяйственных животных, добавление натриевой соли глутаминовой кислоты (глутамата натрия) придает ряду продуктов мясной вкус. В смеси или отдельно аминокислоты применяют в медицине, в том числе при нарушениях обмена веществ и заболеваниях органов пищеварения, при некоторых заболеваниях центральной нервной системы. Аминокислоты используются при изготовлении лекарственных препаратов, красителей, в парфюмерной промышленности, в производ-стве моющих средств, синтетических волокон и пленки и т. д.
Для хозяйственных и медицинских нужд аминокислоты получают с помощью микроорганизмов путем так называемого микробиологического синтеза (лизин, триптофан, треонин); их выделяют также из гидролизатов природных белков (пролин, цистеин, аргинин, гистидин).
Для хозяйственных и медицинских нужд аминокислоты получают с помощью микроорганизмов путем так называемого микробиологического синтеза (лизин, триптофан, треонин); их выделяют также из гидролизатов природных белков (пролин, цистеин, аргинин, гистидин).