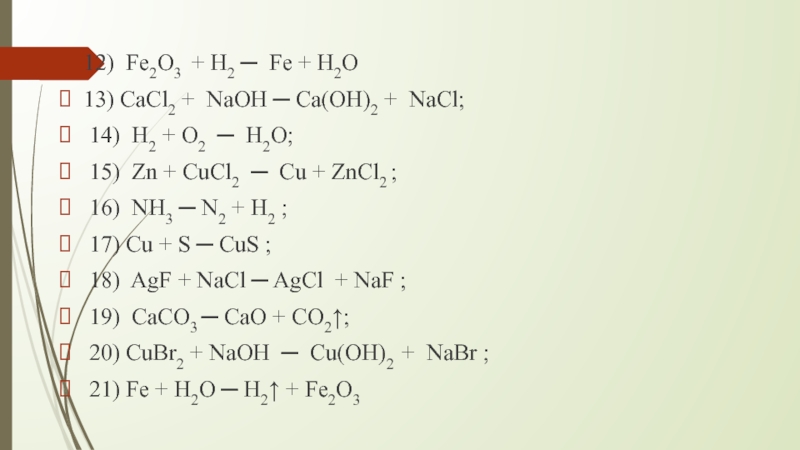- Главная
- Разное
- Образование
- Спорт
- Естествознание
- Природоведение
- Религиоведение
- Французский язык
- Черчение
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Математика
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, фоны, картинки для презентаций
- Экология
- Экономика
Презентация, доклад по химии урок-практикум Составление химических уравнений
Содержание
- 1. Презентация по химии урок-практикум Составление химических уравнений
- 2. Химические уравнения Химическое уравнение - это условная
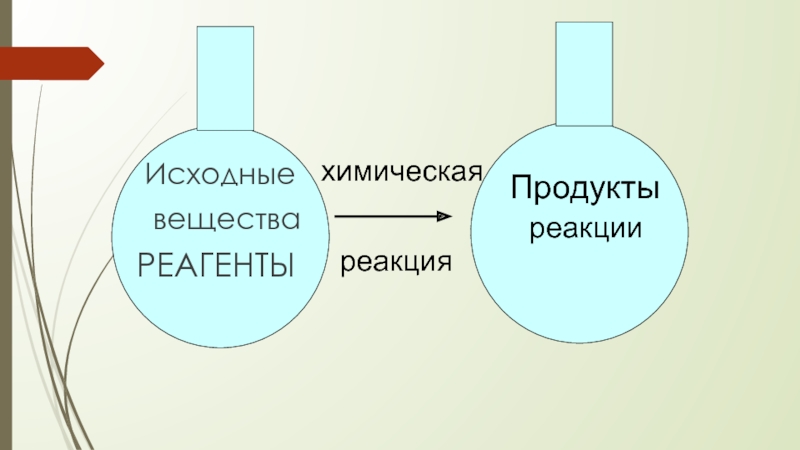
- 3. Исходные веществаРЕАГЕНТЫхимическаяреакцияПродуктыреакции
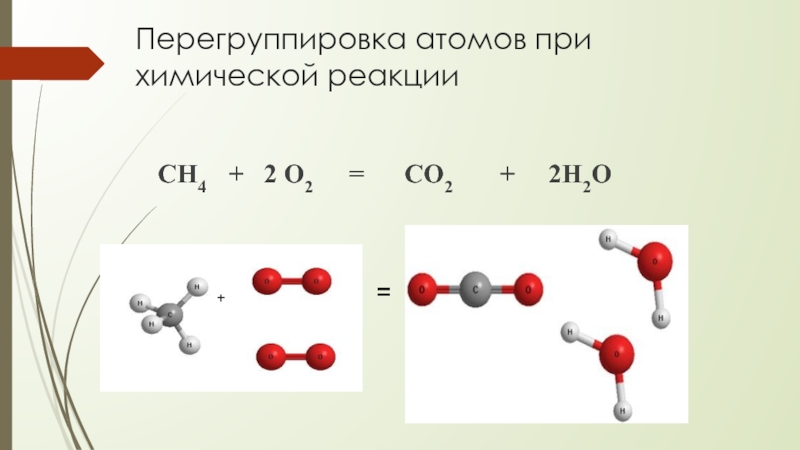
- 4. Перегруппировка атомов при химической реакции
- 5. Алгоритм составления уравнений химических реакций образования бинарных соединений
- 6. Правила составления химических уравнений 1. В левой
- 7. 2. В правой части (после стрелки)
- 8. Алгоритм расстановки коэффициентов в уравнении химической реакции.
- 9. 4. Пересчитать количество атомов, при необходимости
- 10. Новые вещества не получаются из ничего
- 11. 1.Составьте уравнения химических реакций по описанию
- 12. оксид азота (V) реагирует с водой и
- 13. 2.Расставьте коэффициенты в уравнениях реакций:NO +
- 14. 12) Fe2O3 + H2 ─ Fe +
Химические уравнения Химическое уравнение - это условная запись химической реакции посредством химических знаков и формул. Основой при составлении химических уравнений служит Закон сохранения массы веществ: «Масса веществ, вступивших в химическую реакцию. Равна массе образовавшихся веществ».М.В.Ломоносов (1748 год),
Слайд 2Химические уравнения
Химическое уравнение - это условная запись химической реакции посредством
химических знаков и формул.
Основой при составлении химических уравнений служит Закон сохранения массы веществ: «Масса веществ, вступивших в химическую реакцию. Равна массе образовавшихся веществ».М.В.Ломоносов (1748 год),
то есть число атомов каждого элемента в левой и правой частях уравнения должно быть одинаково!
При составлении уравнений химических реакций необходимо знать, что молекулы простых веществ: водорода(H2), азота(N2), кислорода(O2), фтора(F2), хлора(Cl2), брома(Br2), йода(I2)
состоят из двух атомов!
Основой при составлении химических уравнений служит Закон сохранения массы веществ: «Масса веществ, вступивших в химическую реакцию. Равна массе образовавшихся веществ».М.В.Ломоносов (1748 год),
то есть число атомов каждого элемента в левой и правой частях уравнения должно быть одинаково!
При составлении уравнений химических реакций необходимо знать, что молекулы простых веществ: водорода(H2), азота(N2), кислорода(O2), фтора(F2), хлора(Cl2), брома(Br2), йода(I2)
состоят из двух атомов!
Слайд 6Правила составления химических уравнений
1. В левой части уравнения записать
формулы реагентов. Затем поставить стрелку.
а) N2 + H2 →
б) Al(OH)3 →
в) Mg + HCl →
г) СaO + HNO3→
а) N2 + H2 →
б) Al(OH)3 →
в) Mg + HCl →
г) СaO + HNO3→
Слайд 7 2. В правой части (после стрелки) записать формулы веществ, образующихся
в результате реакции (продуктов)
а) N2 + H2 → NH3
б) Al(OH)3 → Al2O3 +H2O
в) Mg + HCl → MgCl2 + H2
г) СaO + HNO3→ Ca(NO3)2 +H2O
а) N2 + H2 → NH3
б) Al(OH)3 → Al2O3 +H2O
в) Mg + HCl → MgCl2 + H2
г) СaO + HNO3→ Ca(NO3)2 +H2O
Слайд 8Алгоритм расстановки коэффициентов в уравнении химической реакции.
1. Подсчитать количество атомов
каждого элемента в правой и левой части.
2. Определить, у какого элемента количество атомов меняется, найти Н.О.К.
3. Разделить Н.О.К. на индексы – получить коэффициенты. Поставить коэффициенты перед формулами.
2. Определить, у какого элемента количество атомов меняется, найти Н.О.К.
3. Разделить Н.О.К. на индексы – получить коэффициенты. Поставить коэффициенты перед формулами.
Слайд 9 4. Пересчитать количество атомов, при необходимости действия повторить.
5. Начинать лучше
с атомов О или любого другого неметалла (если только О не находится в составе нескольких веществ).
Слайд 10 Новые вещества не получаются из ничего и не могут обратиться
в ничто.
При химических реакциях происходит перегруппировка атомов
Масса веществ, вступивших в реакцию равна массе образовавшихся веществ
При составлении уравнений нужно соблюдать закон сохранения массы веществ
При химических реакциях происходит перегруппировка атомов
Масса веществ, вступивших в реакцию равна массе образовавшихся веществ
При составлении уравнений нужно соблюдать закон сохранения массы веществ
Выводы:
Слайд 11 1.Составьте уравнения химических реакций по описанию и расставьте коэффициенты:
серная кислота
взаимодействует с гидроксидом калия с образованием сульфата калия и воды;
хлорид серебра разлагается на свету и при этом образуются серебро и хлор (Cl2);
магний взаимодействует с соляной кислот с образованием хлорида магния и газа водорода (H2↑);
натрий активно реагирует с водой и при этом образуются гидроксид натрия и газ-водород;
хлорид меди(II) взаимодействует с железом с образованием хлорида железа (II) и меди;
гидроксид железа (III) разлагается при нагревании на оксид железа (III) и воду;
сульфат лития реагирует с хлоридом бария и при этом получается хлорид лития и сульфат бария;
хлорид серебра разлагается на свету и при этом образуются серебро и хлор (Cl2);
магний взаимодействует с соляной кислот с образованием хлорида магния и газа водорода (H2↑);
натрий активно реагирует с водой и при этом образуются гидроксид натрия и газ-водород;
хлорид меди(II) взаимодействует с железом с образованием хлорида железа (II) и меди;
гидроксид железа (III) разлагается при нагревании на оксид железа (III) и воду;
сульфат лития реагирует с хлоридом бария и при этом получается хлорид лития и сульфат бария;
Слайд 12оксид азота (V) реагирует с водой и получается азотная кислота;
нитрат калия
разлагается при нагревании с образованием нитрита калия и кислорода-газа (O2↑);
сульфид натрия + азотная кислота ─ сероводород + нитрат натрия;
оксид кальция + оксид кремния (IV) ─ силикат кальция;
фосфорная кислота + гидроксид лития ─ вода + фосфат лития;
силикат калия + азотистая кислота ─ кремниевая кислота + нитрит калия;
сернистая кислота + гидроксид цинка ─ вода + сульфит цинка;
сульфат железа (III) ─ оксид железа (III) + оксид серы (VI);
бромид бария + нитрит серебра ─ бромид серебра + нитрит бария.
сульфид натрия + азотная кислота ─ сероводород + нитрат натрия;
оксид кальция + оксид кремния (IV) ─ силикат кальция;
фосфорная кислота + гидроксид лития ─ вода + фосфат лития;
силикат калия + азотистая кислота ─ кремниевая кислота + нитрит калия;
сернистая кислота + гидроксид цинка ─ вода + сульфит цинка;
сульфат железа (III) ─ оксид железа (III) + оксид серы (VI);
бромид бария + нитрит серебра ─ бромид серебра + нитрит бария.
Слайд 13 2.Расставьте коэффициенты в уравнениях реакций:
NO + O2 ─ NO2;
HCl
+ O2 ─ H2O + Cl2;
PCl3 + Cl2 ─ PCl5;
Fe + H2O ─ Fe3O4 + H2;
CH4 + I2 ─ CH3I + HI ;
Zn + HCl ─ H2↑ + ZnCl2;
CaCl2 + Na2CO3 ─ CaCO3 + NaCl;
NaBr + Cl2 ─ NaCl + Br2;
Ca + HCl ─ CaCl2 + H2↑ ;
Mg + O2 ─ MgO;
H2S + O2 ─ H2O + SO2 ;
PCl3 + Cl2 ─ PCl5;
Fe + H2O ─ Fe3O4 + H2;
CH4 + I2 ─ CH3I + HI ;
Zn + HCl ─ H2↑ + ZnCl2;
CaCl2 + Na2CO3 ─ CaCO3 + NaCl;
NaBr + Cl2 ─ NaCl + Br2;
Ca + HCl ─ CaCl2 + H2↑ ;
Mg + O2 ─ MgO;
H2S + O2 ─ H2O + SO2 ;
Слайд 1412) Fe2O3 + H2 ─ Fe + H2O
13) CaCl2 + NaOH
─ Ca(OH)2 + NaCl;
14) H2 + O2 ─ H2O;
15) Zn + CuCl2 ─ Cu + ZnCl2 ;
16) NH3 ─ N2 + H2 ;
17) Cu + S ─ CuS ;
18) AgF + NaCl ─ AgCl + NaF ;
19) CaCO3 ─ CaO + CO2↑;
20) CuBr2 + NaOH ─ Cu(OH)2 + NaBr ;
21) Fe + H2O ─ H2↑ + Fe2O3
14) H2 + O2 ─ H2O;
15) Zn + CuCl2 ─ Cu + ZnCl2 ;
16) NH3 ─ N2 + H2 ;
17) Cu + S ─ CuS ;
18) AgF + NaCl ─ AgCl + NaF ;
19) CaCO3 ─ CaO + CO2↑;
20) CuBr2 + NaOH ─ Cu(OH)2 + NaBr ;
21) Fe + H2O ─ H2↑ + Fe2O3